Перейти к:
Отогенный синус-тромбоз и гемофилия А: клинический случай
https://doi.org/10.25207/1608-6228-2023-30-3-85-94
Аннотация
Введение. Пациенты с гемофилией защищены от тромбозов за счет дефицита одного из факторов свертывания, поэтому тромботические осложнения у них встречаются редко. В настоящее время в литературе имеется мало описаний спонтанных венозных тромбозов у взрослых пациентов, страдающих гемофилией. Еще меньше сообщений о тромбоэмболических осложнениях в педиатрической практике. На сегодня нет четких рекомендаций по тактике ведения тромботических осложнений у детей, страдающих гемофилией, что требует дальнейшего изучения данной проблемы и разработки схем профилактики и лечения, в том числе и отогенных синус-тромбозов у этой категории пациентов.
Описание клинического случая. Мальчик 7 лет поступил переводом из соматического стационара в отделение реанимации и интенсивной терапии детского стационара государственного бюджетного учреждения здравоохранения Тюменской области «Областная больница № 2», в структуре которого имеется оториноларингологическое отделение, с диагнозом острого правостороннего неперфоративного гнойного среднего оти та, острого правостороннего мастоидита, тромбоза правого сигмовидного синуса. Из анамнеза известно, что ребенок страдает гемофилией А средней степени тяжести (уровень VIII фактора — 5 %), по поводу которой в течение последнего года получает заместительную терапию VIII фактора. При поступлении результаты общего анализа крови без особенностей, отмечено незначительное повышение острофазовых показателей: С-реактивного белка, фибриногена, присутствовали признаки гипокоагуляции. Ввиду отрицательной динамики ребенку была проведена антромастоидотомия на фоне усиления заместительной терапии. В ходе оперативного вмешательства выявлено наличие грануляционной ткани с включениями геморрагических тромбов в антрум и адитусе. В послеоперационном периоде параллельно с заместительной терапией ребенок получал антибактериальную и антикоагулянтную терапию.
Заключение. Ведение пациентов с отогенным синус-тромбозом на фоне наследственного дефицита фактора VIII является сложной задачей, так как, с одной стороны, требует хирургического вмешательства и назначения антикоагулянтной терапии с целью профилактики дальнейшего тромбообразования, с другой стороны — усиления заместительной терапии с целью уменьшения рисков геморрагических осложнений. Описанный клинический случай демонстрирует необходимость меж дисциплинарного подхода к диагностике и лечению пациента с отогенным тромбозом латерального синуса на фоне гемофилии А, который минимизирует риски интраоперационных осложнений и сопровождается благоприятным исходом.
Ключевые слова
Для цитирования:
Вешкурцева И.М., Извин А.И., Кузнецова Н.Е., Кудымов С.А., Синяков А.Ю., Кузнецова Т.Б. Отогенный синус-тромбоз и гемофилия А: клинический случай. Кубанский научный медицинский вестник. 2023;30(3):85-94. https://doi.org/10.25207/1608-6228-2023-30-3-85-94
For citation:
Veshkurtseva I.M., Izvin A.I., Kuznetsova N.E., Kudymov S.A., Sinyakov A.Yu., Kuznetsova T.B. Otogenic Sinus Thrombosis and Hemophilia: A Clinical Case. Kuban Scientific Medical Bulletin. 2023;30(3):85-94. (In Russ.) https://doi.org/10.25207/1608-6228-2023-30-3-85-94
ВВЕДЕНИЕ
Отогенный тромбоз латерального синуса (сигмовидного, поперечного, яремной вены) — редкое, но серьезное внутричерепное осложнение острого или хронического среднего отита, мастоидита. По частоте он занимает третье-четвертое место в структуре внутричерепных осложнений среднего отита. Тромбоз интракраниальных сосудов встречается чаще у мальчиков младшего школьного возраста [1][2]. Несвоевременная диагностика и неадекватная терапия ассоциированы с тяжелыми неврологическими последствиями с рисками инвалидизации пациента, опасностью развития таких жизнеугрожающих состояний, как отек головного мозга, эмболия легочной артерии, сепсис с риском летального исхода и высокими показателями летальных исходов, которые в педиатрической популяции могут составлять от 1 до 29%1 [1–3]. Согласно данным детского оториноларингологического отделения нашего стационара за период с 2009 по 2021 г., тромбозы церебральных сосудов (сигмовидного, поперечного синусов, луковицы яремной вены) выявлены у 21 ребенка, что составило 0,2% от общего количества детей с патологией уха за изученный период и 12,2% всех отогенных осложнений. Вероятность развития тромбоза у пациентов, страдающих гемофилией, очень низка и составляет 1 случай на 27 000 пациентов с данной патологией, что связано с дефицитом одного из факторов свертывания [4][5]. Основными причинами тромботических осложнений у пациентов, страдающих гемофилией, являются врожденная или приобретенная тромбофилия, наличие систем постоянного венозного доступа, заместительная терапия факторами свертывания, хирургические вмешательства, избыточная масса тела, течение тяжелого инфекционного процесса [4][6–8]. В нашей практике мы наблюдали отогенный синус-тромбоз на фоне сопутствующей наследственной патологии — гемофилии А средней степени тяжести в одном случае, что составило 0,2% всех случаев отогенных тромбозов церебральных венозных синусов.
КЛИНИЧЕСКИЙ ПРИМЕР
Информация о пациенте
Пациент Л, 7 лет, мужского пола, поступил в отделение детской реанимации и интенсивной терапии государственного бюджетного учреждения здравоохранения Тюменской области «Областная клиническая больница № 2» (ГБУЗ ТО «ОКБ № 2») переводом из педиатрического отделения государственного бюджетного учреждения здравоохранения Тюменской области «Областная клиническая больница № 1» (ГБУЗ ТО «ОКБ № 1») с жалобами на сонливость, слабость, снижение аппетита, головную боль, кашель, насморк.
Анамнез заболевания
Из анамнеза известно, что до развития вышеперечисленных жалоб ребенок был болен в течение недели, лечился амбулаторно по поводу острого респираторного заболевания симптоматическими средствами. За сутки до госпитализации у мальчика появилась боль в правом ухе. При самостоятельном обращении в ГБУЗ ТО «ОКБ № 2» ребенок был осмотрен в приемном отделении детского стационара, выставлен диагноз острого респираторного заболевания, острого правостороннего катарального среднего отита. Назначена терапия системными антибактериальными средствами (цефиксим — по 200 мг 1 раз в день перорально) местно — феназон + лидокаин (по 3 капли 2 раза в день в правое ухо), интраназально — ксилометазолин (0,05% р-р по 2 капли 2 раза в день в каждый носовой ход), пациент был отпущен домой. Вечером того же дня у мальчика появились головная боль, рвота с примесью крови, эпистаксис, ребенок был экстренно госпитализирован в педиатрическое отделение ГБУЗ ТО «ОКБ № 1».
Ребенку была назначена антибактериальная (цефтриаксон по 1 г 1 раз в день в/в струйно) и симптоматическая терапия (глюкозо-калиевая смесь: 10% глюкоза 500 мл + KCL 4% — 92 мл микроструйно; продолжены лидокаин + феназон по 3 капли 2 раза в день, ксилометазолин по 2 капли 2 раза в день). Ввиду эпистаксиса с заместительной целью при поступлении однократно был введен фактор VIII в дозе 700 ЕД. Мальчик был проконсультирован детским неврологом, гематологом, оториноларингологом, проведена компьютерная томография (КТ) головного мозга с контрастированием (рис. 1). По данным КТ головного мозга с контрастированием: признаки воспалительных изменений пирамиды правой височной кости, тромбоза правого сигмовидного синуса (неполная окклюзия?).
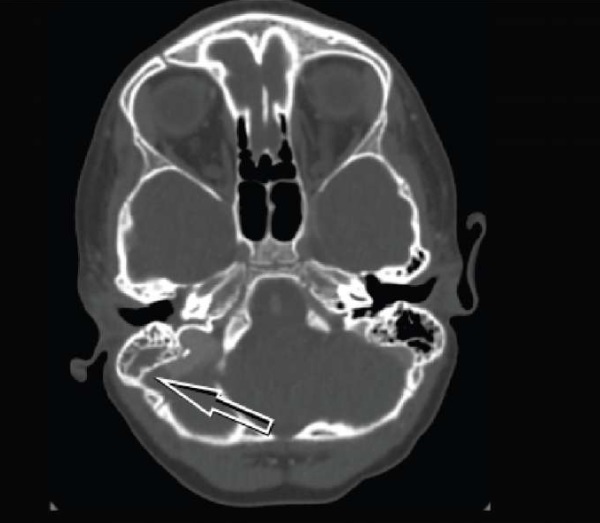
Рис. 1. Компьютерная томография головного мозга с контрастированием пациента Л. на момент поступления в ГБУЗ ТО «ОКБ № 1».
Примечание: фотография сделана авторами. Сокращения: ГБУЗ ТО «ОКБ № 1» — государственное бюджетное учреждение здравоохранения Тюменской области «Областная клиническая больница № 1».
Fig. 1. Patient L.: contrast CT of brain, upon admission to Regional Clinical Hospital No. 1.
Note: photo taken by the authors. Abbreviations: ГБУЗ ТО «ОКБ № 1» — Regional Clinical Hospital No. 1.
С диагнозом острого правостороннего неперфоративного гнойного среднего отита, острого правостороннего мастоидита, тромбоза правого сигмовидного синуса; наследственного дефицита фактора VIII: Гемофилия А, средней степени тяжести (уровень фактора свертывания крови VIII (FVIII) — 5% (норма 50–150%)) ребенок был переведен в отделение реанимации и интенсивной терапии ГБУЗ ТО «ОКБ № 2», имеющего в своей структуре детское оториноларингологическое отделение.
Анамнез жизни
Со слов законных представителей (матери) ребенок от 2-й доношенной беременности, 2-х срочных самостоятельных родов. Беременность протекала без особенностей. Вес при рождении 3190 г, рост 52 см, закричал сразу. Вакцинация туберкулезной вакциной (БЦЖ) в родильном доме. Грудное молоко получал до 1 года 8 месяцев. Профилактические прививки согласно национальному календарю. Из перенесенных заболеваний: частые острые респираторные вирусные инфекции (ОРВИ), дважды перенес острый катаральный двусторонний отит, острый верхнечелюстной синусит. При анализе анамнеза жизни стало известно, что в возрасте 6 лет после длительного кровотечения на фоне удаления 2-х зубов (73, 74) у ребенка верифицирован (ноябрь 2020 г.) диагноз гемофилии А средней степени тяжести, с этого же момента мальчик получает заместительную терапию FVIII по 500 МЕ 2 раза в неделю.
Аллергологический анамнез: со слов законных представителей (матери) аллергических заболеваний нет, непереносимости лекарственных препаратов и пищевых продуктов не выявлено.
Наследственный анамнез. Анализ генеалогического анамнеза выявил наличие у деда по материнской линии болезни Верльгофа с периодическими кровотечениями из слизистых оболочек.
Физикальная диагностика
При поступлении в отделение реанимации и интенсивной терапии состояние ребенка было расценено как тяжелое, отмечались умеренная оглушенность, сонливость, вялость, адинамичность. Масса тела 24 кг, рост 119 см, индекс массы тела 16,95 м². Кожные покровы физиологической окраски, умеренно сухие. Лимфоузлы интактные. Менингиальные симптомы отрицательные. Число дыханий 20 в минуту, сатурация 100% на атмосферном воздухе. Аскультативно дыхание везикулярное, проводится по всем полям, хрипов нет. Частота сердечных сокращений (ЧСС) 102 в минуту, артериальное давление (АД) на правой руке 100/60 мм рт. ст. Тоны сердца ясные, ритм правильный. Живот мягкий, безболезненный во всех отделах. Селезенка не пальпируется. Печень по краю реберной дуги. Мочеиспускание безболезненное, диурез достаточный, стул без патологических примесей. Локально были выявлены: умеренно затрудненное носовое дыхание, отечная и гиперемированная слизистая оболочка носа, слизистое отделяемое. Слизистая ротоглотки влажная, отечная, гиперемирована. Форма и размеры ушных раковин, околоушных и сосцевидных областей слева не изменены. Справа и слева сосцевидные отростки безболезненные при пальпации. Наружный слуховой проход справа, слева — не изменены, отделяемого в наружных слуховых проходах справа, слева не обнаружено. Барабанная перепонка справа гиперемирована за счет гемотимпанума, отечная, мутная, не выбухает, опознавательные знаки не различимы, слева — без патологических изменений.
Предварительный диагноз
Правосторонний неперфоративный гнойный средний отит. Гемотимпанум. Гемофилия А средней степени тяжести. Вторичная цефалгия, вторичная астения.
Временная шкала
Хронологические события развития заболевания у пациента Л. представлены на рисунке 2.

Рис. 2. Хронология развития заболевания у пациента Л.: ключевые события и прогноз.
Примечание: блок-схема временной шкалы выполнена авторами (согласно рекомендациям, разработанным международными организациями в области здравоохранения для клинических случаев). Сокращения: ОРВИ — острая респираторная вирусная инфекция; ОРЗ — острое респираторное заболевание; ОКБ № 1 — государственное бюджетное учреждение здравоохранения Тюменской области «Областная клиническая больница № 1»; FVIII — уровень фактора свертывания крови VIII; КТ — компьютерная томография; ОРИТ — отделение реанимации и интенсивной терапии; САК — субарахноидальное кровоизлияние.
Fig. 2. Patient L.: course of disease, key events and prognosis.
Note: performed by the authors (according to recommendations developed by international organizations in the field of healthcare for clinical cases). Abbreviations: ОРВИ — acute respiratory viral infection, ARVI; ОРЗ — acute respiratory disease, ARD; ОКБ № 1 — Regional Clinical Hospital No. 1, Tyumen; FVIII — level of coagulation factor VIII; КТ — computer tomography; ОРИТ — intensive care unit; САК — subarachnoid hemorrhage.
Диагностические процедуры
Лабораторные исследования
На момент поступления в отделение реанимации и интенсивной терапии при лабораторном обследовании не были выявлены воспалительные изменения со стороны общего анализа крови (ГБУЗ ТО «ОКБ № 2» от 20.04.2021 г.): лейкоциты — 8,21×109/л (референтные значения — (5,0–14,5)×109/л), абсолютное количество нейтрофилов — 6,39×109/л (референтные значения — 1,5–8,0×109/л). Отмечалось незначительное повышение острофазовых показателей: С-реактивного белка (СРБ) — 20 мг/мл (референтные значения — 0–10 мг/л), фибриногена (ф/г) — 5 г/л (референтные значения — 1,8–4 г/л), присутствовали признаки гипокоагуляции: активированное частичное тромбопластиновое время (АЧТВ) — 50 секунд (референтные значения — 26–40 сек) (табл. 1). Уровень D-димера не определялся, поскольку было убедительно показано, что тромбоз, особенно окклюзирующий, может протекать и без значимого повышения показателей D-димера. Увеличение концентрации данного маркера в крови может наблюдаться и при состояниях, не связанных с тромбозом (беременность, наличие гематомы, течение инфекционного процесса, послеоперационный период, наличие опухоли). С другой стороны, отсутствие повышения концентрации D-димеров не может являться поводом для исключения факта тромбоза у ребенка.
Таким образом, оценка концентрации D-димера может носить дополняющий характер, например в случаях, когда имеется клиническая картина венозного тромбоза, а по данным визуализации имеет место неспецифическая картина, на основании которой нельзя исключить тромбоз. Поэтому определение концентрации D-димеров как маркера наличия или отсутствия тромбоза у ребенка не рекомендовано1, 2 [3][9].
Таблица. Динамика показателей гемограммы, коагулограммы, СРБ пациента Л. (ГБУЗ ТО «ОКБ № 2»)
Table. Patient L.: dynamics of hemogram, coagulogram, C-reactive protein (Regional Clinical Hospital No. 2)
|
Показатели / дата |
20.04.2021 |
21.04.2021 |
23.04.2021 |
25.04.2021 |
28.04.2021 |
Референтные значения |
|
Лейкоциты ×109/л |
8,21 |
8,04 |
7,33 |
5,68 |
4,78 |
5,0–14,5 |
|
Нейтрофилы ×109/л |
6,39 |
4,97 |
4,7 |
3,58 |
1,95 |
1,5–8,0 |
|
Тромбоциты ×109/л |
248 |
273 |
297 |
281 |
295 |
180–320 |
|
АЧТВ, сек. |
50,0 |
43,8 |
33,6 |
28,8 |
48,1 |
26–40 |
|
МНО |
1,3 |
1,23 |
1,31 |
1,24 |
1,1 |
0,8–1,3 |
|
ПВ, сек |
17 |
16 |
17 |
16 |
13,8 |
11–17 |
|
Ф/Г, г/л |
5 |
4,5 |
5 |
3 |
2,36 |
1,8–4 |
|
СРБ, мг/л |
20 |
20 |
- |
1 |
- |
0–10 |
Примечание: таблица составлена авторами. Сокращения: ГБУЗ ТО «ОКБ № 2» — государственное бюджетное учреждение здравоохранения Тюменской области «Областная клиническая больница № 2»; АЧТВ — активированное частичное тромбопластиновое время, МНО — международное нормализованное отношение, ПВ — протромбиновое время, Ф/Г — фибриноген, СРБ — С-реактивный белок.
Note: compiled by the authors. Abbreviations: ГБУЗ ТО «ОКБ № 2» — Regional Clinical Hospital No. 2; АЧТВ — activated partial thromboplastin time, МНО — international normalized ratio, ПВ — prothrombin time, Ф/Г — fibrinogen, СРБ — C-reactive protein.
Инструментальные исследования
Электрокардиография от 20.04.2021 г. (ГБУЗ ТО «ОКБ № 2»): Синусовая брадикардия, 77 в минуту. Неполная блокада правой ножки пучка Гиса. Умеренные нарушения обменных процессов в миокарде.
УЗИ органов брюшной полости и забрюшинного пространства от 20.04.2021 г. (ГБУЗ ТО «ОКБ № 2»): без патологии.
Консультации специалистов (ГБУЗ ТО «ОКБ № 2»):
Детский оториноларинголог: Острый неперфоративный средний отит справа. Латентный правосторонний мастоидит. Тромбоз правого сигмовидного синуса.
Гематолог: Наследственный дефицит фактора VIII. Гемофилия А, средней степени тяжести.
Нейрохирург: Данных за острую нейрохирургическую патологию на момент осмотра нет. Отогенный тромбоз правого сигмовидного синуса. На момент осмотра показаний для экстренного нейрохирургического оперативного вмешательство нет.
Детский невролог: Тромбоз правого сигмовидного синуса.
Детский офтальмолог: Данных за офтальмологическую патологию нет.
Клинический диагноз
Острый неперфоративный гнойный средний отит справа. Острый правосторонний мастоидит. Тромбоз правого сигмовидного синуса. Острый катарально-отечный полисинусит. Острый назофарингит. Гемофилия А, средней степени тяжести.
Дифференциальная диагностика
Проведена дифференциальная диагностика причин тромбоза церебральных сосудов.
- Причиной тромбоэмболических катастроф является наличие приобретенной тромбофилии, которая развивается на фоне патологии печени, заболеваний почек, миелопролиферативного синдрома, которые у нашего пациента выявлены не были.
- Наличие у пациентов центрального венозного катетера, порт-систем, Power-picc-катетер, катетеров по типу Groshong и Broviac, которые увеличивают вероятность тромботических осложнений. В нашем случае у ребенка не было ни установки центрального венозного катетера (ЦВК), ни системы постоянного венозного доступа.
- Проведение заместительной терапии FVIII при гемофилии А может рассматриваться как одна из причин развития тромботических осложнений, вероятность которых увеличивается при наслоении инфекционного процесса. В рассматриваемом нами случае при наличии острого гнойного отита, мастоидита нельзя было исключить и ятрогенный генез развития тромбоза сигмовидного синуса.
Медицинские вмешательства
21.04.2021 г. по экстренным показаниям мальчику был произведен парацентез правой барабанной перепонки, получено серозное отделяемое, кровотечения не наблюдалось. Была назначена системная антибактериальная терапия цефепимом (по 700 мг в/в капельно 3 раза в день), обладающим широким спектром действия и хорошим проникновением через гематоэнцефалический барьер.
Динамика и исходы
23.04.2021 г. из-за отрицательной динамики в виде нарастания отечности правой барабанной перепонки, выраженного болевого синдрома со стороны сосцевидного отростка, наличия скудного серозно-гнойного отделяемого из стомы было решено, несмотря на риски геморрагических осложнений на фоне наследственного дефицита FVIII, по жизненным показаниям провести антромастоидотомию. Ребенок был дистанционно проконсультирован гематологом, согласно рекомендациям которого заместительная терапия FVIII была усилена — по 500 МЕ за 30 минут до оперативного вмешательства, затем каждые 12 часов в течение 4 дней, далее по 500 МЕ 3 раза в неделю в течение 1 месяца. Определение уровня остаточной активности FVIII и тест восстановления в нашем случае не проводились. В этот же день под эндотрахеальным наркозом мальчику была произведена антромастоидотомия справа, выявлены заполненные грануляционной тканью с включениями геморрагических тромбов антрум и адитус, которые были удалены, сигмовидный синус «пульсирующий, живой». Был взят материал на микробиологическое и гистологическое исследования. Получены отрицательные результаты микробиологического исследования, гистологически — выявлена морфологическая картина гнойного воспаления. В послеоперационном периоде, согласно рекомендациям гематолога, ребенок получал заместительную терапию FVIII. Определение уровня FVIII в послеоперационном периоде не проводилось. Параллельно, в рамках терапии тромбоза правого сигмовидного синуса, была назначена антикоагулянтная терапия эноксапарином (по 0,2 мл — 20 мг 1 раз в день подкожно) off-label (с оформлением решения врачебной комиссии и информированного согласия законных представителей). На фоне хирургического вмешательства, заместительной, антикоагулянтной и антибактериальной терапии отмечалась стабилизация в состоянии ребенка, нормализация показателей СРБ, фибриногена.
При ежедневном введении VIII фактора (с 21.04.2021 по 25.04.2021 г.) показатели АЧТВ находились в пределах нормы — 33,0–28,8 сек. Однако при сокращении кратности введения заместительной терапии до трех раз в неделю (по рекомендации гематолога) вновь отмечались явления гипокоагуляции (АЧТВ — 48,1 сек.), что, с одной стороны, уменьшало в данной ситуации вероятность прогрессирования тромбообразования, однако, с другой стороны, увеличивало риски геморрагических осложнений у ребенка с наследственным дефицитом FVIII (табл.).
29.04.2021 г. было проведено контрольное КТ-исследование с контрастированием, выявлено состояние после правосторонней антромастоидотомии, не обнаружено очаговых изменений плотности вещества головного мозга, КТ-признаков субарахноидального кровоизлияния, внутримозговых, оболочечных гематом. Однако сохранялся частичный дефект наполнения правого сигмовидного синуса прежней протяженностью с увеличением его внутреннего диаметра (рис. 3).
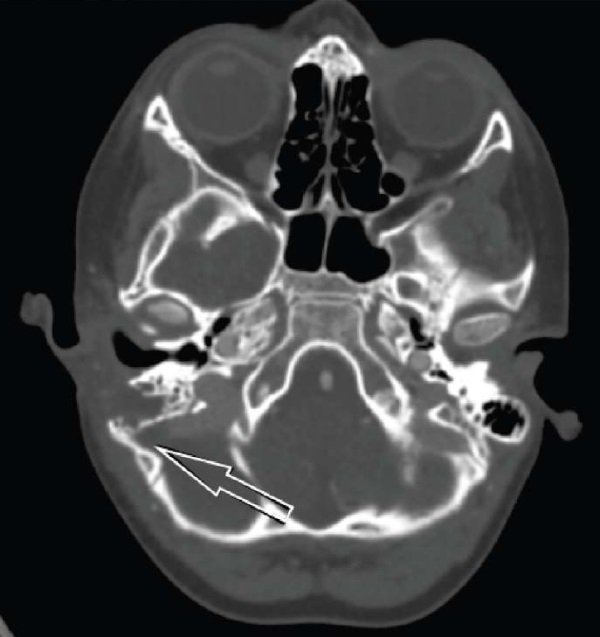
Рис. 3. Компьютерная томография головного мозга с контрастированием пациента Л. через 14 дней лечения в ГБУЗ ТО «ОКБ № 2».
Примечание: фотография выполнена авторами. Сокращение: ГБУЗ ТО «ОКБ № 2» — государственное бюджетное учреждение здравоохранения Тюменской области «Областная клиническая больница № 2».
Fig. 3. Patient L.: contrast CT of brain, after 14 days of treatment in Regional Clinical Hospital No. 2.
Note: photo taken by the authors. Abbreviations: ГБУЗ ТО «ОКБ № 2» — Regional Clinical Hospital No. 2
С учетом положительной динамики со стороны клиники и параклинических показателей 3.05.2021 г. ребенок был выписан на амбулаторное долечивание под наблюдение педиатра, детского оториноларинголога и гематолога.
Прогноз
Благодаря комплексной терапии ребенка с отогенным тромбозом сигмовидного синуса на фоне наследственного дефицита FVIII (гемофилии А) с использованием хирургических и медикаментозных методов лечения удалось разрешить инфекционный процесс и минимизировать риски развития как тромботических, так и геморрагических осложнений. Прогноз для пациента в контексте его здоровья, физической и социальной активности при соблюдении всех профилактических мероприятий в целом благоприятный. Законные представители ребенка обеспокоены наличием у мальчика наследственного дефицита FVIII и рисками как геморрагических, так и тромботических осложнений и готовы следовать всем рекомендациям, прописанным ребенку.
ОБСУЖДЕНИЕ
Гемофилия А — Х-сцепленное наследственное заболевание, вызванное нарушением синтеза FVIII. Гемофилия А встречается чаще, чем другие наследственные аномалии факторов свертывания крови, но реже, чем болезнь Виллебранда. Расчетная распространенность гемофилии А составляет 17,1 случая на 100 000 мужчин для всех степеней тяжести и 6,0 случая на 100 000 мужчин для тяжелого фенотипа [9]. Пациенты с гемофилией защищены от тромбозов за счет дефицита одного из факторов свертывания [4][10], поэтому тромботические осложнения у них встречаются редко. В настоящее время в литературе имеется мало описаний спонтанных венозных тромбозов у взрослых пациентов, страдающих гемофилией [4][5]. Еще меньше сообщений о тромбоэмболических осложнениях в педиатрической практике [7].
Одним из факторов риска развития тромбозов у пациентов с гемофилией является тромбофилия. Сочетание этих двух патологических состояний встречается редко. Полиморфизм генов, ассоциированных с тромбофилией, встречается в 3–6% случаев в общей популяции, однако у детей с синус-тромбозом может достигать 43–96% [11][12]. Литературные данные о полиморфизме генов, ассоциированных с тромбофилией, среди пациентов, страдающих гемофилией, существенно разнятся, эти показатели не отличаются от показателей в общей популяции [13], а по данным Т.Ю. Полянской и соавт., могут составлять 96,9% [14].
Описаны различные мутации, ассоциированные с тромбофилией, которые находят у больных гемофилией: мутация FV Лейден, мутация G20210A в гене протромбина, гипергомоцистеинемия, дефицит протеина С, протеина S, антитромбина III, сниженная активность активированного протеина С и др. [5][14]. По данным Т.Ю. Полянской и соавт., у 81,3 % пациентов с гемофилией наблюдается полиморфизм нескольких маркеров [14]. Сочетание гемофилии с тромбофилией ослабляет выраженность геморрагического синдрома [4]. Однако в нашем случае молекулярно-генетического исследования на наличие наследственной тромбофилии у ребенка не проводились. Причины приобретенной тромбофилии (патология печени, заболевания почек, миелопролиферативный синдром и др.) у нашего пациента выявлены не были. Еще одним фактором развития тромботических осложнений при гемофилии является наличие у пациента центрального венозного катетера или систем постоянного венозного доступа (порт-системы, Power-picc-катетер, катетеры по типу Groshong и Broviac)1 [3][4][8]. Тромбоэмболические события могут развиваться у 17,5% детей с центральными венозными катетерами, находящихся в критическом состоянии [15]. Центральные венозные катетеры, особенно нетуннельного типа, обычно устанавливают пациентам, находящимся в крайне тяжелом состоянии и, вероятно, уже исходно имеющим состояние гиперкоагуляции [16], что связано с увеличением активности факторов свертывания крови, особенно FVIII, во время тяжелого течения заболевания. По данным M. Cushman, активность VIII фактора >150 МЕ/дл в сыворотке крови связана с 2,6–4,8-кратным повышением вероятности развития тромбоза глубоких вен у взрослых пациентов [17]. В рассматриваемом нами случае у ребенка не было систем постоянного венозного доступа, центральный венозный катетер не устанавливался.
Введение VIII фактора свертывания крови с заместительной целью также может способствовать возникновению тромботических осложнений у пациентов с гемофилией А, которое может привести не только к нормализации его уровня в сыворотке крови, но и к состоянию гиперкоагуляции. FVIII является неферментативным кофактором активированного фактора свертывания крови IX (FIXa), который при протеолитической активации взаимодействует с FIXa с образованием прочного нековалентного комплекса, связывающего и активирующего фактор X (FX)2 [4][6][9][15][18]. Заместительная терапия концентратами FVIII или FIX факторов при гемофилии проводится при развитии геморрагического синдрома или при необходимости экстренных хирургических операций.
С 1972 г. в клиническую практику было внедрено профилактическое лечение пациентов с данной патологией, цель которого заключается в более раннем начале введения факторов свертывания для профилактики поражения суставов, минимизации рисков инвалидизации пациента, повышению их качества жизни и социальной адаптации. Введение FVIII или FIX с профилактической целью позволяет избежать значимого поражения суставов более чем у 95% детей с тяжелой и среднетяжелой гемофилией и у 100% детей с легкой формой заболевания [10]. В настоящее время такое лечение начинают в возрасте 1–2 лет, оно может продолжаться до 20 лет, а нередко и дольше. На сегодняшний день режим, которого необходимо придерживаться при гемофилии А, представляет собой введение 25–40 ME FVIII на 1 кг массы тела пациента (обычно 3 раза в неделю). Активность FVIII в плазме пациента с гемофилией А должна быть не ниже 1–2%. Это означает, что заболевание с точки зрения активности свертывающей системы должно быть переведено из тяжелой формы в среднетяжелую или легкую. В нашем случае ребенок получал FVIII в средней дозе 22 ME FVIII/кг (2 раза в неделю).
Профилактическая заместительная терапия может быть первичной или вторичной. В рассматриваемом нами клиническом случае ребенок получал первичную профилактику, которая проводится у детей, не имеющих признаков поражения суставов и хронического их воспаления (синовита), до первого кровоизлияния в сустав или после однократного кровоизлияния в один или два сустава. Первичная профилактика может проводиться до окончания роста ребенка или пожизненно [10][19]. В настоящее время продемонстрирована корреляция высокого уровня FVIII в плазме крови с развитием «катастрофического тромботического синдрома» с формированием тромбоэмболических событий нетипичной локализации: церебральные синусы, система портальной вены, сосуды кожи. При увеличении уровня FVIII на каждые 10 мкл/дл повышается риск первого тромботического события на 10% [18].
Еще одним фактором, который может увеличить вероятность развития тромботических осложнений у пациентов с гемофилией, является инфекционный процесс [5–7]. Тромбоз церебральных сосудов чаще развивается как осложнение острого или хронического гнойного среднего отита, мастоидита, составляя 12–19% всех отогенных внутричерепных осложнений. [1][2]. По данным ряда авторов, отогенный синус-тромбоз имеет полимикробную этиологию, при котором могут обнаруживаться такие микроорганизмы, как Streptococcus spp., Staphylococcus spp., P. aeruginosa, P. mirabilis, Fusobacterium necrophorum, H. influentiae и др. [2][20]. Согласно литературным данным, S. aureus, S. pyogenes, P. aeruginosa, E. coli, K. pneumoniae, H. influenzae увеличивают вероятность тромботических осложнений. Это связано с вызванной данными микроорганизмами системной воспалительной реакцией и высвобождением цитокинов: интерлейкина-6, интерлейкина-8 и фактора некроза опухоли альфа (ФНО-α), что ведет к повреждению эндотелия, активации и усилению агрегации тромбоцитов, увеличению прокоагулянтных белков, таких как тканевой фактор, и снижению активности антикоагулянтных механизмов, таких как фибринолиз. При этом и сами патогены часто способны модулировать систему свертывания крови путем выработки прокоагулянтных белков. Считается, что системные инфекции увеличивают вероятность развития тромбоза глубоких вен или тромбоэмболии легочной артерии в 2–20 раз [21]. В рассматриваемом нами случае при проведении микробиологического исследования материала из операционной раны были получены отрицательные результаты, что, однако, не говорит об отсутствии инфекционного агента.
Для уменьшения вероятности прогрессирования тромбообразования обязательным компонентом терапии тромбоза, в том числе и церебральных сосудов, является назначение антикоагулянтной терапии, своевременное использование которой, как известно, позволяет снизить риск фатальных исходов и тяжелой инвалидизации1, 2 [3][9]. Однако отношение к антитромботической терапии в педиатрической практике до сих пор неоднозначно [2][20][22]. Это связано и с несовершенством системы гемостаза у ребенка, что определяет особенности ответа детского организма на фармакологическое действие антитромботических препаратов, и с различными межлекарственными взаимодействиями этих препаратов, и с высокими рисками развития побочных эффектов, и с отсутствием детских лекарственных форм антитромботических средств1 [2][3][23][24].
На сегодняшний день нет четких рекомендаций по тактике антикоагулянтной терапии при синус-тромбозе у детей, страдающих гемофилией, что требует дальнейшего изучения данной проблемы и разработки схем профилактики и лечения тромботических осложнений у данной категории пациентов [7]. При наличии тромботических осложнений у детей с гемофилией R. Ko et al. [7] рекомендуют отменять или снижать дозу заместительной терапии только при повышении уровня фактора свертывания в сыворотке крови > 30% и, соответственно, при снижении рисков геморрагических осложнений. Однако в нашей ситуации доза FVIII даже была увеличена в связи с необходимостью проведения хирургического вмешательства и наличием высоких рисков кровотечения. При развитии синус-тромбозов у пациентов, в том числе и детского возраста, не страдающих гемофилией, антикоагулянтная терапия является предпочтительным методом лечения для предотвращения прогрессирования патологического процесса в виде образования новых тромбов и увеличения в размерах уже существующих, что в итоге уменьшает риски летальных исходов1 [3][25][26]. При этом лечение антикоагулянтными препаратами после постановки диагноза тромбоза церебральных сосудов необходимо начать незамедлительно [27]. Из антикоагулянтов возможно использование как нефракционированного (НФГ), так и низкомолекулярных гепаринов (НМГ).
Для НФГ характерны крайне непредсказуемые фармакокинетические и фармакодинамические показатели, зависящие от возраста ребенка, уровня эндогенного антитромбина и других показателей [3][24]. Тем не менее в настоящее время НФГ по-прежнему является препаратом выбора у детей для краткосрочной антикоагулянтной терапии, а также в ситуациях высокого риска кровотечения, когда необходимы управляемая гипокоагуляция с применением препаратов с коротким периодом полувыведения и наличие антидота (протамина сульфат)1 [3]. Ряд авторов при развитии тромбоза церебральных сосудов, в том числе и у детей, рекомендуют использовать НМГ как наиболее безопасные и более предсказуемые в своем терапевтическом эффекте препараты1 [3][25][27]. Более продолжительный период полувыведения, более предсказуемый антикоагулянтный эффект НМГ делает их более предпочтительными для длительного применения, в том числе и в амбулаторных условиях [24]. Наличие сопутствующей гемофилии у детей с тромботическими осложнениями не является противопоказанием к назначению антикоагулянтной терапии1 [3]. По данным литературы, используются как НФГ, так и НМГ1 [3][5][10].
В каждой конкретной ситуации необходимо соотносить пользу и риски от применения антитромботической терапии, т.к. использование антикоагулянтов и антиагрегантов у пациентов с гемофилией сопряжено с высокими рисками развития тяжелых геморрагических осложнений [10]. У детей, страдающих гемофилией, при развитии тромбозов предпочтение следует отдавать антикоагулянтам кратковременного действия [10]. У детей реканализация церебральных синусов наблюдается раньше, чем у взрослых, как правило, в течение двух недель от момента катастрофы. Через 3 месяца признаки реканализации наблюдаются примерно у 30% пациентов, а к 6 месяцам — уже у 50% детей, перенесших тромбоз центральных венозных синусов1 [3].
С хирургической точки зрения современной тенденцией является выполнение мастоидэктомии с удалением воспалительной ткани со стенок пазухи, чтобы получить эрадикацию инфекционного процесса. Своевременно выполненное оперативное вмешательство способствует дренажу и аэрации среднего уха, aditus, antrum и сосцевидного антрального отдела, снижает давление, оказываемое гнойным выпотом. Более агрессивные варианты, такие как хирургическое дренирование синуса с удалением тромба, обычно не рекомендуются [2]. В рассматриваемом нами случае дренирование синуса не проводилось из-за высоких рисков развития геморрагических осложнений у ребенка с наследственным дефицитом FVIII и из-за операционной находки в виде «живого, пульсирующего» сигмовидного синуса, что свидетельствовало о пристеночном расположении тромба и проходимости синуса. В представленном случае интенсивная терапия в течение 14 дней привела к неполной реканализации сигмовидного синуса. Однако, учитывая пристеночное расположение тромба в синусе, отсутствие признаков его роста и полной окклюзии, наличие у ребенка сопутствующей патологии в виде наследственного дефицита FVIII и отсутствие геморрагических осложнений на фоне антикоагулянтной терапии, полученные нами результаты были расценены как положительные.
ЗАКЛЮЧЕНИЕ
Ведение пациентов с отогенным синус-тромбозом на фоне наследственного дефицита фактора VIII является сложной задачей, так как, с одной стороны, требует хирургического вмешательства и назначения антикоагулянтной терапии с целью профилактики дальнейшего тромбообразования, с другой стороны — усиления заместительной терапии с целью уменьшения рисков геморрагических осложнений. Описанный клинический случай демонстрирует, что персонализированный подход к ведению пациента с тромбозом церебральных сосудов на фоне гемофилии А со взвешенным подходом к хирургическому вмешательству и медикаментозной терапией сопровождается благоприятным исходом.
1. Румянцев А.Г., Масчан А.А., Жарков П.А., Свирин П.В. Федеральные клинические рекомендации по диагностике, профилактике и лечению тромбозов у детей и подростков. 2015; 113 с.
2. Детская гематология: Сборник клинических рекомендаций. Под ред: А.Г. Румянцев, А.А. Масчан, Е.В. Жуковская и др. М.: ГЭОТАР-Медиа, 2015. 656 с. ISBN 978-5-9704-3475-8.
Список литературы
1. Constable J.D., Hajioff D. Paediatric otogenic cerebral venous sinus thrombosis: a multidisciplinary approach. J Laryngol Otol. 2022; 136(1): 3–7. DOI: 10.1017/S0022215121003145
2. Castellazzi M.L., di Pietro G.M., Gaffuri M., Torretta S., Conte G., Folino F., Aleo S., Bosis S., Marchisio P. Pediatric otogenic cerebral venous sinus thrombosis: a case report and a literature review. Ital. J. Pediatr. 2020; 46(1): 122. DOI: 10.1186/s13052-020-00882-9
3. Mitchell L.G., Male C. Outcome measures in interventional trials for prevention or treatment of venous thrombosis in the pediatric population. Semin. Thromb. Hemost. 2011; 37(7): 840–847. DOI: 10.1055/s-0031-1297176
4. Галстян Г.М., Полеводова О.А., Гавриш А.Ю., Полянская Т.Ю., Зоренко В.Ю., Сампиев М.С., Бирюкова Л.С., Модел С.В., Горгидзе Л.А., Савченко В.Г. Тромботические осложнения у больных гемофилией. Терапевтический архив. 2017; 89(7): 76–84. DOI: 10.17116/terarkh201789776-84
5. Darawshy F., Kalish Y., Hendi I., Abu Rmelieh A., Khoury T. Upper Limb Deep Vein Thrombosis in Patient with Hemophilia A and Heterozygosity for Prothrombin G20210A: A Case Report and Review of the Literature. Case. Rep. Hematol. 2017; 2017: 7290945. DOI: 10.1155/2017/7290945
6. Chhabra M., Hii Z.W.S., Rajendran J., Ponnudurai K., Fan B.E. Venous Thrombosis in Acquired Hemophilia: The Complex Management of Competing Pathologies. TH Open. 2019; 3(4): e325–e330. DOI: 10.1055/s-0039-1698414
7. Ko R.H., Thornburg C.D. Venous Thromboembolism in Children with Cancer and Blood Disorders. Front. Pediatr. 2017; 5: 12. DOI: 10.3389/fped.2017.00012
8. Галстян Г.М., Спирин М.В., Зозуля Н.И., Полянская Т.Ю., Зоренко В.Ю. Обеспечение долгосрочного сосудистого доступа у больных гемофилией. Гематология и трансфузиология. 2018; 63(2): 144–158. DOI: 10.25837/HAT.2018.34.2.005
9. Monagle P., Chan A.K.C., Goldenberg N.A., Ichord R.N., Journeycake J.M., Nowak-Göttl U., Vesely S.K. Antithrombotic therapy in neonates and children: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012; 141(2 Suppl): e737S–e801S. DOI: 10.1378/chest.11-2308
10. Connell N.T., Flood V.H., Brignardello-Petersen R., Abdul-Kadir R., Arapshian A., Couper S., Grow J.M., Kouides P., Laffan M., Lavin M., Leebeek F.W.G., O’Brien S.H., Ozelo M.C., Tosetto A., Weyand A.C., James P.D., Kalot M.A., Husainat N., Mustafa R.A. ASH ISTH NHF WFH 2021 guidelines on the management of von Willebrand disease. Blood Adv. 2021; 5(1): 301–325. DOI: 10.1182/bloodadvances.2020003264
11. Schneider S., Kapelushnik J., Kraus M., El Saied S., Levi I., Kaplan D.M. The association between otogenic lateral sinus thrombosis and thrombophilia — A long-term follow-up. Am. J. Otolaryngol. 2018; 39(3): 299–302. DOI: 10.1016/j.amjoto.2018.03.013
12. Scorpecci A., Massoud M., Giannantonio S., Zangari P., Lucidi D., Martines F., Foligno S., Di Felice G., Minozzi A., Luciani M., Marsella P. Otogenic lateral sinus thrombosis in children: proposal of an experience-based treatment flowchart. Eur. Arch. Otorhinolaryngol. 2018; 275(8): 1971–1977. DOI: 10.1007/s00405-018-5033-1
13. de Haan H.G., van Hylckama Vlieg A., Lotta L.A., Gorski M.M., Bucciarelli P., Martinelli I., Baglin T.P., Peyvandi F., Rosendaal F.R.; INVENT consortium. Targeted sequencing to identify novel genetic risk factors for deep vein thrombosis: a study of 734 genes. J. Thromb. Haemost. 2018; 16(12): 2432–2441. DOI: 10.1111/jth.14279
14. Полянская Т.Ю., Февралева И.С., Карпов Е.Е., Садыкова Н.В., Сампиев М.С., Голобоков А.В., Мишин Г.В., Петровский Д.Ю., Королева А.А., Галстян Г.М., Судариков А.Б., Зоренко В.Ю. Полиморфизм генов тромбофилии и их роль в развитии разных фенотипов заболевания и тромботических осложнений у больных гемофилией. Сибирский научный медицинский журнал. 2019; 39(1): 106–111. DOI: 10.15372/SSMJ20190115
15. Faustino E.V., Li S., Silva C.T., Pinto M.G., Qin L., Tala J.A., Rinder H.M., Kupfer G.M., Shapiro E.D.; Northeast Pediatric Critical Care Research Consortium. Factor VIII May Predict Catheter-Related Thrombosis in Critically Ill Children: A Preliminary Study. Pediatr. Crit. Care Med. 2015; 16(6): 497–504. DOI: 10.1097/PCC.0000000000000409
16. Ryan M.L., Van Haren R.M., Thorson C.M., Andrews D.M., Perez E.A., Neville H.L., Sola J.E., Proctor K.G. Trauma induced hypercoagulablity in pediatric patients. J. Pediatr. Surg. 2014; 49(8): 1295–1299. DOI: 10.1016/j.jpedsurg.2013.11.050
17. Cushman M. Epidemiology and risk factors for venous thrombosis. Semin. Hematol. 2007; 44(2): 62–69. DOI: 10.1053/j.seminhematol.2007.02.004
18. Kropf J., Cheyney S., Vachon J., Flaherty P., Vo M., Carlan S.J. Extensive catastrophic thromboses from elevation of factor VIII. Clin. Pract. 2020; 10(3): 1265. DOI: 10.4081/cp.2020.1265
19. Connell N.T., Flood V.H., Brignardello-Petersen R., Abdul-Kadir R., Arapshian A., Couper S., Grow J.M., Kouides P., Laffan M., Lavin M., Leebeek F.W.G., O’Brien S.H., Ozelo M.C., Tosetto A., Weyand A.C., James P.D., Kalot M.A., Husainat N., Mustafa R.A. ASH ISTH NHF WFH 2021 guidelines on the management of von Willebrand disease. Blood. Adv. 2021; 5(1): 301–325. DOI: 10.1182/bloodadvances.2020003264
20. Bergsma P., Kunz S., Kienle A.L., Brand Y. Case Report: Petrous Apicitis and Otogenic Thrombosis of the Cavernous Sinus in a 10-Year-Old Boy. Front. Surg. 2021; 8: 667817. DOI: 10.3389/fsurg.2021.667817
21. Beristain-Covarrubias N., Perez-Toledo M., Thomas M.R., Henderson I.R., Watson S.P., Cunningham A.F. Understanding Infection-Induced Thrombosis: Lessons Learned From Animal Models. Front. Immunol. 2019; 10: 2569. DOI: 10.3389/fimmu.2019.02569
22. Rodrigues S.G., Vieira D., Bernardo F., Coelho J., Ribeiro J.A., Palavra F., Robalo C., Levy A., Quintas S. Pediatric cerebral sinus venous thrombosis: clinical characterization of a Portuguese cohort. Acta. Neurol. Belg. 2022; 122(5): 1211–1218. DOI: 10.1007/s13760-021-01807-x
23. Coutinho G., Júlio S., Matos R., Santos M., Spratley J. Otogenic cerebral venous thrombosis in children: A review of 16 consecutive cases. Int. J. Pediatr Otorhinolaryngol. 2018; 113: 177–181. DOI: 10.1016/j.ijporl.2018.07.050
24. Male C. Anticoagulation in Pediatric Patients. Hamostaseologie. 2022; 42(1): 46–53. DOI: 10.1055/a-1703-0821
25. Stevens S.M., Woller S.C., Baumann Kreuziger L., Bounameaux H., Doerschug K., Geersing G.J., Huisman M.V., Kearon C., King C.S., Knighton A.J., Lake E., Murin S., Vintch J.R.E., Wells P.S., Moores L.K. Executive Summary: Antithrombotic Therapy for VTE Disease: Second Update of the CHEST Guideline and Expert Panel Report. Chest. 2021; 160(6): 2247–2259. DOI: 10.1016/j.chest.2021.07.056
26. Shlobin N.A., LoPresti M.A., Beestrum M., Lam S. Treatment of pediatric cerebral venous sinus thromboses: the role of anticoagulation. Childs. Nerv. Syst. 2020; 36(11): 2621–2633. DOI: 10.1007/s00381-020-04829-7
27. Ulivi L., Squitieri M., Cohen H., Cowley P., Werring D.J. Cerebral venous thrombosis: a practical guide. Pract. Neurol. 2020; 20(5): 356–367. DOI: 10.1136/practneurol-2019-002415
Об авторах
И. М. ВешкурцеваРоссия
Вешкурцева Изабелла Михайловна — кандидат медицинских наук, доцент; доцент кафедры клинической фармакологии и доказательной медицины Тюменский ГМУ; врач-клинический фармаколог детского стационара Областная клиническая больница № 2.
Ул. Одесская, д. 54, г. Тюмень, 625000; ул. Мельникайте, д. 75, г. Тюмень, 625039
А. И. Извин
Россия
Извин Александр Иванович — доктор медицинских наук, профессор; профессор кафедры оториноларингологии.
Ул. Одесская, д. 54, г. Тюмень, 625000
Н. Е. Кузнецова
Россия
Кузнецова Надежда Ефимовна — кандидат медицинских наук, доцент; доцент кафедры оториноларингологии.
Ул. Одесская, д. 54, г. Тюмень, 625000
С. А. Кудымов
Россия
Кудымов Сергей Александрович — заведующий отделением оториноларингологии детского стационара.
Ул. Мельникайте, д. 75, г. Тюмень, 625039
А. Ю. Синяков
Россия
Синяков Андрей Юрьевич — врач-оториноларинголог отделения оториноларингологии детского стационара.
Ул. Мельникайте, д. 75, г. Тюмень, 625039
Т. Б. Кузнецова
Россия
Кузнецова Татьяна Борисовна — ординатор кафедры анестезиологии и реанимации.
Ул. Лиговская, д.2, Санкт-Петербург, 194100
Рецензия
Для цитирования:
Вешкурцева И.М., Извин А.И., Кузнецова Н.Е., Кудымов С.А., Синяков А.Ю., Кузнецова Т.Б. Отогенный синус-тромбоз и гемофилия А: клинический случай. Кубанский научный медицинский вестник. 2023;30(3):85-94. https://doi.org/10.25207/1608-6228-2023-30-3-85-94
For citation:
Veshkurtseva I.M., Izvin A.I., Kuznetsova N.E., Kudymov S.A., Sinyakov A.Yu., Kuznetsova T.B. Otogenic Sinus Thrombosis and Hemophilia: A Clinical Case. Kuban Scientific Medical Bulletin. 2023;30(3):85-94. (In Russ.) https://doi.org/10.25207/1608-6228-2023-30-3-85-94
JATS XML








































