Перейти к:
Гериатрические факторы риска безопасности прямых оральных антикоагулянтов у пациентов с фибрилляцией предсердий 80 лет и старше: обсервационное когортное проспективное исследование
https://doi.org/10.25207/1608-6228-2025-32-3-15-35
Аннотация
Введение. Пожилой возраст коррелирует с наличием гериатрических синдромов, вклад которых в безопасность прямых оральных антикоагулянтов у пациентов с фибрилляцией предсердий активно изучается. В научной литературе основное внимание уделяется профилактике больших кровотечений, в то время как клинически значимые небольшие кровотечения возникают значительно чаще и могут оказывать существенное влияние на состояние больного. Цель исследования — оценить возможность гериатрических факторов прогнозировать риск развития клинически значимых небольших кровотечений на фоне приема прямых оральных антикоагулянтов у пациентов с неклапанной фибрилляцией предсердий в возрасте 80 лет и старше. Методы. В работе представлены результаты наблюдательного проспективного когортного исследования, включавшего 367 пациентов от 80 лет с фибрилляцией предсердий, получавших прямые оральные антикоагулянты. Исследование проводилось на базе многопрофильного стационара Москвы в период с января 2019 по декабрь 2022 года и отражало реальную клиническую практику. Проспективно проведена оценка медицинской документации на наличие клинически значимых небольших кровотечений, период наблюдения — 12 месяцев. Были сформированы группы: основная с клинически значимыми небольшими кровотечениями (n = 195), медиана возраста 84 [82; 87] года, и контрольная без клинически значимых небольших кровотечений (n = 172), медиана возраста — 84 [82; 88] года. Группы были сопоставимы по основным факторам риска кровотечений. Для определения гериатрических факторов риска выполнена комплексная гериатрическая оценка по четырем основным доменам: физического и психоэмоционального статуса, функциональных возможностей и выявления социальных проблем. Обработка статистических данных и их визуализация были выполнены в программной среде R, версия 4.4.0 (R Foundation for Statistical Computing, Вена, Австрия). Различия считали статистически значимыми при р < 0,05. Результаты. В результате анализа были выявлены факторы риска клинически значимых небольших кровотечений из всех четырех доменов комплексной гериатрической оценки: социальный (проживание в семье, количество проживающих в семье, официальный брак, посещение церкви), психоэмоциональный (гериатрическая шкала депрессии), физический и функциональный (тесты на равновесие, шкала Лоутон, применение вспомогательных средств, старческая астения по опроснику «Возраст не помеха», индекс хрупкости по шкале SPRINT (Systolic Blood Pressure Intervention Trial) (р < 0,05). В ходе многофакторного анализа была создана многофакторная логистическая регрессионная модель для прогнозирования клинически значимых небольших кровотечений и разработана прогностическая номограмма, позволяющая оценить вероятность развития клинически значимых небольших кровотечений (прогностическая точность 59,9 %, чувствительность 48,9 %, специфичность 72,4 %). Предикторами явились количество проживающих в семье, индекс Бартел, индекс Лоутон, тест «Встань и иди» и использование любого вспомогательного средства. Заключение. В исследовании было показано, что социально активные, эмоционально устойчивые, мобильные и крепкие пациенты имеют более высокий риск развития клинически значимых небольших кровотечений. Выявлены гериатрические факторы, которые могут являться предикторами клинически значимых небольших кровотечений на фоне приема прямых оральных антикоагулянтов у пациентов с фибрилляции предсердий старше 80 лет. С учетом активного внедрения технологий искусственного интеллекта в клиническую практику полученные данные могут быть интегрированы в системы поддержки врачебных решений.
Ключевые слова
Для цитирования:
Черняева М.С., Павлова А.О., Алферова П.А., Рожкова М.А., Трифонов М.И., Никеева Т.В., Егорова Л.А., Масленникова О.М., Ломакин Н.В., Сычев Д.А. Гериатрические факторы риска безопасности прямых оральных антикоагулянтов у пациентов с фибрилляцией предсердий 80 лет и старше: обсервационное когортное проспективное исследование. Кубанский научный медицинский вестник. 2025;32(3):15-35. https://doi.org/10.25207/1608-6228-2025-32-3-15-35
For citation:
Cherniaeva M.S., Pavlova A.O., Alferova P.A., Rozhkova M.A., Trifonov M.I., Nikeeva T.V., Egorova L.A., Maslennikova O.M., Lomakin N.V., Sychev D.A. Geriatric factors affecting the safety of direct oral anticoagulants in atrial fibrillation patients aged 80 years and older: An observational prospective cohort study. Kuban Scientific Medical Bulletin. 2025;32(3):15-35. https://doi.org/10.25207/1608-6228-2025-32-3-15-35
ВВЕДЕНИЕ
Фибрилляция предсердий (ФП) является распространенным заболеванием, которое встречается у 1–2 % общей популяции, при этом с увеличением возраста увеличивается число пациентов с ФП — от <0,5 % в возрасте 40–50 лет до 5–15 % в возрасте 80 лет. В ближайшие 50 лет ожидается увеличение количества пациентов с ФП практически в два раза. Главной опасностью данной патологии является высокий риск системных тромбоэмболий и ишемического инсульта, для профилактики которых препаратами выбора являются прямые пероральные антикоагулянты (ПОАК) [1][2]. Однако их использование может привести к кровотечениям, особенно у пожилых пациентов ввиду ряда возрастных изменений в организме. В частности, уменьшение печеночной перфузии и снижение активности отдельных изоформ цитохрома Р450 оказывают влияние на фармакокинетику ПОАК. Тогда как возрастное снижение числа функционирующих нефронов вызывает увеличение периода полувыведения этих препаратов. Наблюдается модификация рецепторной чувствительности и плотности их распределения, что оказывает непосредственное влияние на фармакодинамические свойства ПОАК1 [3–5].
Известно, что пожилой возраст коррелирует с наличием гериатрических синдромов, к которым относятся хронический болевой синдром, недержание мочи/кала, высокий риск падения, когнитивные нарушения, деменция, снижение мобильности, старческая астения и др. Старческая астения (с англ. frailty — хрупкость) является ведущим гериатрическим синдромом, который приводит к снижению физиологических резервов организма2.
Начиная с 2020 года в клинических рекомендациях Европейского общества кардиологов (ЕОК) по диагностике и лечению пациентов с ФП [6] шкала HAS-BLED (гипертония, нарушение функции почек/печени, инсульт, кровотечения в анамнезе или предрасположенность, нестабильное международное нормализованное отношение, пожилой возраст (> 65 лет), одновременный прием наркотиков/алкоголя с англ.: Hypertension, Abnormal renal/liver function, Stroke, Bleeding history or predisposition, Labile international normalized ratio, Elderly (> 65 years), Drugs/alcohol concomitantly) включает оценку хрупкости пациента, а к факторам риска геморрагических осложнений отнесены отдельные гериатрические синдромы, включая когнитивные нарушения или деменцию и высокий риск падений. Согласно актуализированным в 2024 году клиническим рекомендациям Европейского общества кардиологов (ЕОК) по лечению ФП [2] от оценки риска кровотечения с помощью шкалы HAS-BLED предложено вовсе отказаться, поскольку систематические обзоры и контрольные исследования в группах сравнения показали крайне противоречивые результаты и малую прогностическую ценность, однако делается акцент на оценку и контроль модифицируемых и потенциально модифицируемых факторов риска кровотечения, в числе которых сохраняются высокий риск падений, когнитивные нарушения или деменция. Тогда как в отношении влияния «хрупкости» или старческой астении на развитие кровотечений упоминаний нет ни в обновленных в 2024 г. рекомендациях ЕОК по лечению ФП [2], ни в клинических рекомендациях по лечению фибрилляции и трепетания предсердий Российского кардиологического общества [1]
Тем не менее результаты исследований у пожилых пациентов с ФП на фоне приема ПОАК показали, что риск падений и старческая астения повышают риск развития кровотечения [7–11]. Данные исследования в основном сфокусированы на изучении больших и внутричерепных кровотечений, где в отдельную группу не выделяли «клинически значимое небольшое кровотечение» (КЗНК, с англ.: clinically relevant non-major bleeding, CRNMB). Тем не менее частота КЗНК гораздо выше, чем больших кровотечений, и достигает 17,4 %, увеличиваясь с возрастом [12][13]. Данное осложнение нельзя недооценивать, так как оно становится причиной отмены приема ПОАК, что увеличивает риск тромбоэмболии и, как следствие, инвалидизации или смерти пациента. Кроме того, КЗНК может приводить к большому кровотечению или госпитализации пациента и дальнейшему медицинскому вмешательству [12]. Информации о вкладе других гериатрических синдромов в развитие кровотечений на фоне приема ПОАК нами не было найдено.
В этой связи в современных исследованиях недостаточно данных относительно вклада гериатрических синдромов в прогнозирование безопасности применения ПОАК в отношении развития КЗНК. Более того, средний возраст пациентов в исследованиях по изучению влияния гериатрических синдромов на безопасность ПОАК варьирует от 75 до 78 лет, тогда как количество пациентов старше 80 лет увеличивается во всем мире по мере увеличения продолжительности жизни [14][15]. Что и побудило нас к данному исследованию.
Цель исследования — оценить возможность гериатрических факторов прогнозировать риск развития клинически значимых небольших кровотечений на фоне приема прямых оральных антикоагулянтов у пациентов с неклапанной фибрилляцией предсердий в возрасте 80 лет и старше.
МЕТОДЫ
Дизайн исследования
В исследование реальной клинической практики по дизайну наблюдательного проспективного когортного исследования вошли 367 пациентов ≥ 80 лет с ФП, принимавших ПОАК, проходивших лечение в московской многопрофильной клинике с января 2019 по декабрь 2022 г.
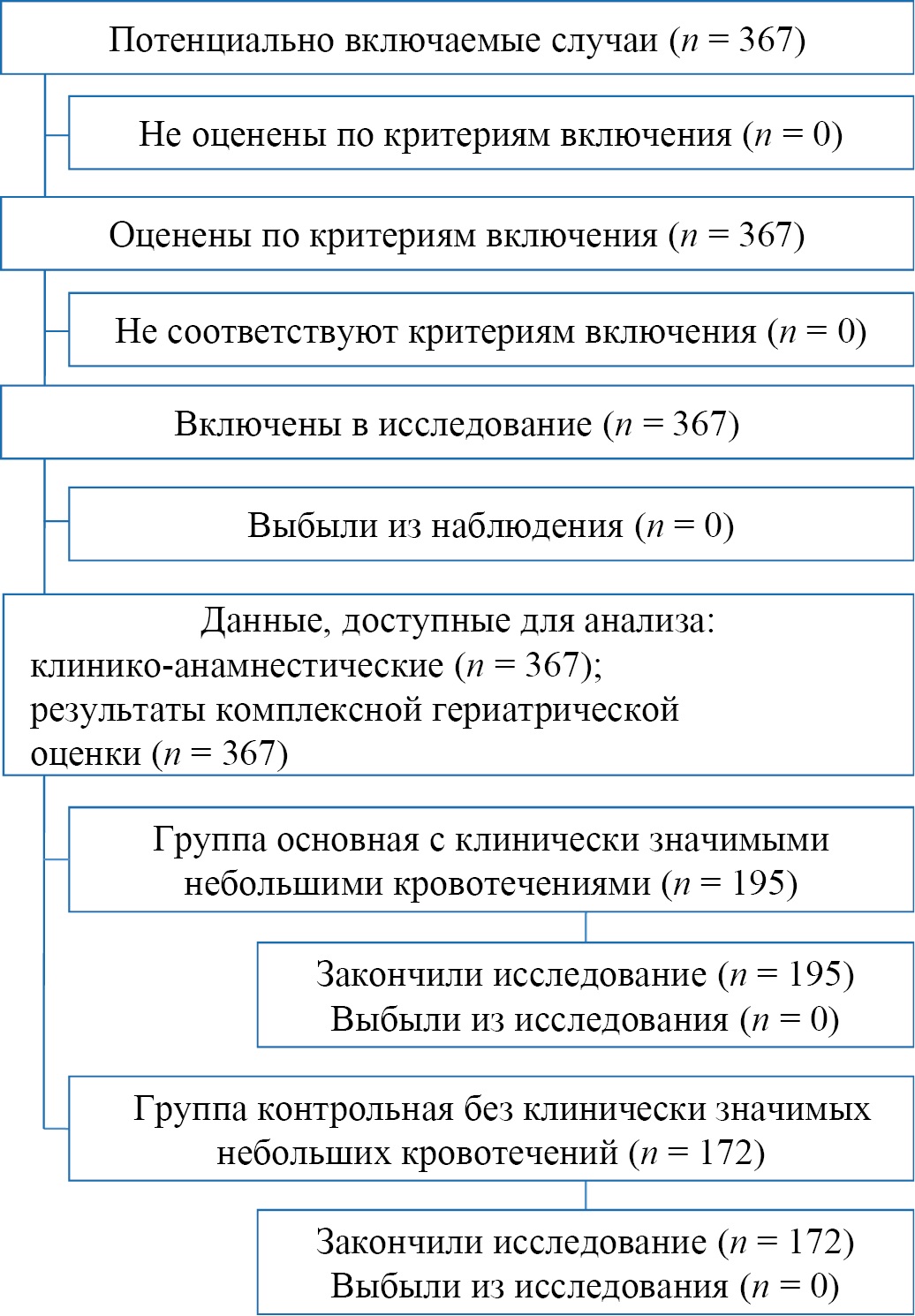
Рис. 1. Блок-схема дизайна исследования
Примечание: блок-схема выполнена авторами (согласно рекомендациям STROBE).
Fig. 1. Block diagram of the study design
Note: the block diagram was created by the authors (as per STROBE recommendations).
Условия проведения
Исследование проведено на базе клинической кафедры — клинической фармакологии и терапии имени академика Б. Е. Вотчала федерального государственного бюджетного образовательного учреждения дополнительного профессионального образования «Российская медицинская академия непрерывного профессионального образования» Министерства здравоохранения Российской Федерации (ФГБОУ ДПО РМАНПО Минздрава России). Включение в исследование пациентов осуществлялось с января 2019 по декабрь 2022 г. Далее осуществлялся проспективный анализ амбулаторных и стационарных медицинских карт пациентов для оценки частоты КЗНК при терапии ПОАК. Продолжительность мониторинга составила 1 год.
Критерии соответствия
Критерии включения
Пациенты с неклапанной ФП обоего пола; возраст на момент включения в исследование — 80 лет и старше; регулярный прием ПОАК продолжительностью не менее 1 года от момента включения в исследование; подписание добровольного информированного согласия на участие в исследование.
Критерии невключения
Возраст < 80 лет; клинически значимые заболевания сердца (в том числе кардиогенный шок, недавно перенесенный (менее одного месяца назад) инфаркт миокарда с осложнениями, атриовентрикулярная блокада III степени без искусственного водителя ритма, гипертрофическая кардиомиопатия, выраженный аортальный и митральный стеноз); выраженные заболевания печени (в том числе цирроз печени с асцитом); пациенты, получающие заместительную почечную терапию (программный гемодиализ, перитонеальный диализ, трансплантация почки в анамнезе); клинически значимое иммунологическое заболевание; неврологические заболевания (в том числе острое нарушение мозгового кровообращения и транзиторная ишемическая атака в анамнезе менее 3 месяцев назад); хирургическая операция (за исключением стоматологических или косметических операций), травмы, переломы в течение предыдущих 3 месяцев; наличие клинически значимых изменений лабораторных показателей, свидетельствующих о недиагностированном заболевании и требующих дополнительного обследования.
Критерии исключения
Нарушение пациентом процедур плана обследования и лечения; отказ пациента от участия в исследовании и отзыв информированного согласия.
Описание критериев соответствия (диагностические критерии)
Диагноз ФП установлен в соответствии с критериями клинических рекомендаций по лечению фибрилляции и трепетания предсердий Российского кардиологического общества [1]. Диагностика КЗНК у пациентов, получавших ПОАК, осуществлялась на основании критериев, разработанных Международным обществом по тромбозу и гемостазу (the International Society on Thrombosis and Haemostasis, ISTH) [12]. Перечень проведенных пациентам вмешательств регламентирован приказом Министерства здравоохранения Российской Федерации от 29 января 2016 года (приказ № 38н) «Порядок оказания медицинской помощи по профилю «гериатрия» с изменениями от 20 декабря 2019 года (приказ № 1067н)3.
Подбор участников в группы
Когорта исследования состояла из 367 пациентов ≥80 лет, которые последовательно включались в исследование при соответствии критериям отбора. По завершению годового мониторинга на основании данных о проявлении и рецидивировании КЗНК пациенты были разделены на 2 группы сравнения: в основную группу вошли пациенты с КЗНК (n = 195), в контрольную пациенты без КЗНК (n = 172).
Целевые показатели исследования
Основные показатели исследования
Для определения гериатрических факторов риска, влияющих на риск развития КЗНК на фоне приема ПОАК, пациентам была проведена комплексная гериатрическая оценка, которая включала в себя анализ по четырем основным доменам: физического и психоэмоционального статуса, функциональных возможностей и выявления социальных проблем4.
Дополнительные показатели исследования
В настоящем исследовании не проводилась оценка дополнительных показателей.
Методы измерения целевых показателей
Были использованы следующие валидированные карты, опросники, шкалы, тесты и расчетные индексы: карта комплексной гериатрической оценки5, опросник «Возраст не помеха», самооценка качества жизни и состояния здоровья по визуально-аналоговой шкале (ВАШ), шкала оценки базовой функциональной активности (шкала Бартел) (англ. Barthel Index for Activities of Daily Living, ADL) [16], шкала оценки инструментальной функциональной активности в повседневной жизни (шкала Лоутона) (англ. Lawton Instrumental activities of daily living Scale) [17], краткая шкала оценки питания (англ. Mini Nutritional assessment, MNA) [17][18], краткая батарея тестов физического функционирования (англ. The Short Physical Performance Battery, SPPB), тест «Встань и иди», тест на равновесие на одной ноге6. Также всем пациентам была проведена динамометрия для определения силы сжатия кисти, критерии низкой силы пожатия определялись в зависимости от пола и индекса массы тела в соответствии с клиническими рекомендациями по старческой астении2.
Индекс хрупкости рассчитывался по шкале Rockwood [19] и по шкале, которая использовалась для расчета в исследовании SPRINT (англ. Systolic Blood Pressure Intervention Trial — интервенционное исследование об изучении систолического артериального давления) [20].
Оценка психоэмоционального статуса была проведена с помощью следующих тестов, шкал и опросников7: скриниговый тест «Мини-ког» (англ. Mini-Cog), краткая шкала оценки психического статуса (англ. Mini-mental State Examination, MMSE), монреальская шкала оценки когнитивных функций (англ. Montreal Cognitive Assessment, Moca), тест на запоминание слов (англ. Word-List Recall), тест символы и цифры (англ. Digit Symbol Substitution Test, DSST), тест на повторение цифр (англ. Digit span), тест запоминания 10 слов (англ. Word-List Recall Test, WLТ), тест вербальных ассоциаций (литеральные/буквы и категориальные/животные ассоциации) (англ. Category fluency/animals), Бостонский тест называния (англ. Boston Naming Test), опросник функциональной активности (англ. Functional Activities Questionnaire, FAQ), когнитивная субшкала оценки болезни Альцгеймера (англ. Аlzheimer disease assessment scale-cognitive, ADAS-cog), гериатрическая шкала депрессии (англ. Geriatric Depression Scale, GDS) GDS –15 (англ. short form, короткая форма) и GDS-30 (англ. long form, длинная форма).
Переменные (предикторы, конфаундеры, модификаторы эффекта)
В настоящем исследовании факторы, влияющие на конечный результат, были отнесены к критериям исключения, что полностью исключает их наличие у пациентов исследуемой выборки.
Статистические процедуры
Принципы расчета размера выборки
Предварительный расчет выборки пациенток не производился.
Статистические методы
Статистический анализ и визуализация полученных данных проводились с использованием среды для статистических вычислений R 4.4.0 (R Foundation for Statistical Computing, Австрия). Описательные статистики представлены в виде абсолютной и относительной частот для качественных переменных, медианы (Ме) (1-й; 3-й квартили) — для количественных переменных. Для сравнения групп в отношении категориальных показателей использовались тест χ² Пирсона и точный тест Фишера (при минимальном ожидаемом количестве наблюдений в ячейках таблицы сопряженности <5). Для сравнения двух групп в отношении количественных и порядковых показателей использовался тест Манна — Уитни. В качестве меры силы количественных и бинарных показателей с бинарными исходами оценивались отношения шансов (ОШ) с соответствующими 95 % доверительного интервала (ДИ).
Пошаговый отбор предикторов в прогностические модели осуществлялся с использованием информационного критерия Акаике (Akaike information criterion, AIC). Отобранные предикторы включались в многофакторную логистическую регрессионную модель без взаимодействий. В качестве метрик качества модели оценивали псевдо-R2 Найджелкерке и коэффициент DXY Соммерса и C-индекс (area under the curve, AUC), в том числе оценивались метрики, скорректированные на потенциальное переобучение с использованием непараметрического бутсрепа (B = 1000). Для контроля мультиколлинеарности предикторов использовался фактор инфляции дисперсии (variance inflation factor, VIF). Производилось определение оптимального порогового значения для предсказанной вероятности с использованием J-статистики Юдена и оценка прогностической точности, чувствительности, специфичности и прогностической ценности положительного и отрицательного результата с соответствующими 95 % ДИ.
РЕЗУЛЬТАТЫ
Формирование выборки исследования
Формирование выборки проводилось сплошным методом на основании наличия/отсутствия критериев включения/невключения. Комплексная гериатрическая оценка проводилась всем участникам исследования после включения в исследование. Выявление КЗНК при терапии ПОАК проводилось на основе проспективного изучения амбулаторных и стационарных медицинских карт. Длительность наблюдения равнялась одному году. Разделение по группам зависело от наличия или отсутствия КЗНК. Отказавшихся от участия в исследовании пациентов не было ни в одной группе.
Характеристика выборки (групп) исследования
Подбор пациентов (n = 367) исследуемых групп осуществлялся с соблюдением критериев включения и невключения (Ме возраста 84 [ 82; 88] года) с неклапанной ФП. С целью профилактики тромбоэмболий все участники принимали ПОАК: ривароксабан (n = 238/367, относительная доля равна 64,9 %), апиксабан (n = 95/367, относительная доля 25,9 %) или дабигатрана этексилат (n = 34/367, относительная доля 9,2 %). Основная группа включала 195 пациентов с КЗНК — Ме возраста 84 [ 82; 87] года, из них 66,7 % — женщины. В контрольной группе состояли 172 пациента без КЗНК — Ме возраста 84 [ 82; 88] года, из них 72,7 % — женщины. Между группами не выявлено существенных различий по полу, возрасту, риску ишемического инсульта по шкале CHA2DS2-VASc (англ. Congestive heart failure; Hypertension; Age; Diabetes mellitus; Prior Stroke or TIA or Thromboembolism; Vascular disease; Age 65–74 years; Sex category), риску кровотечений по шкале HAS-BLED, индексу массы тела и основным факторам риска кровотечений в соответствии с критериями клинических рекомендаций по лечению фибрилляции и трепетания предсердий Российского кардиологического общества [1][20].
Основные результаты исследования
Анализ гериатрических факторов риска развития клинически значимых небольших кровотечений
Для оценки социального домена были изучены 24 параметра, среди которых: наличие инвалидности, наличие партнера или супруга, детей, семейный статус, круг общения и социальных контактов, жилищные условия, финансовые возможности, рабочая активность, профессия, образование, религиозность, потребность в амбулаторной, стационарной, плановой и неотложной медицинской помощи, лекарственное обеспечение по социальным льготам. В результате было выявлено, что пациенты с КЗНК в сравнении с пациентами без КЗНК имели более высокую социальную активность. Так, пациенты с КЗНК в сравнении с пациентами без КЗНК статистически значимо чаще проживали в семье (p = 0,031), одинокое проживание было статистически значимо ассоциировано со снижением шансов наличия КЗНК в 1,65 (95 % ДИ: 1,08; 2,51) раза по отношению к проживающим в семье (p = 0,025). Пациенты с КЗНК в сравнении с пациентами без КЗНК характеризовались статистически значимо бóльшим количеством людей, проживающих в семье (p = 0,003), увеличение количества проживающих в семье на каждого человека было статистически значимо ассоциировано с увеличением шансов наличия КЗНК в среднем в 1,22 (95 % ДИ: 1,03; 1,47) раза (p = 0,025). Пациенты с КЗНК в сравнении с пациентами без КЗНК статистически значимо чаще состояли в браке (p = 0,014) и чаще посещали церковь (p = 0,046), регулярное посещение церкви (мечети, синагоги, буддийского храма, молитвенного дома) было ассоциировано с увеличением шансов наличия КЗНК в 3,75 (95 % ДИ: 1,23; 11,5) раза (p = 0,025) (табл. 1).
Таблица 1. Гериатрические факторы риска: социальный домен
Table 1. Geriatric risk factors: social domain
|
Характеристика |
Все пациенты (n = 367) |
Клинически значимые небольшие кровотечения |
Уровень статистической значимости, p |
|
|
Нет (n = 172) |
Есть (n = 195) |
|||
|
Инвалидность, n (%) |
304/359 (84,7%) |
141/169 (83,4%) |
163/190 (85,8%) |
0,536 |
|
• I группа, n (%) |
19/359 (5,3%) |
9/169 (5,3%) |
10/190 (5,3%) |
0,999 |
|
• II группа, n (%) |
223/359 (62,1%) |
100/169 (59,2%) |
123/190 (64,7%) |
0,39 |
|
• III группа, n (%) |
62/359 (17,3%) |
32/169 (18,9%) |
30/190 (15,8%) |
0,495 |
|
Тип проживания |
||||
|
• одинокое, n (%) |
155/363 (42,7%) |
84/171 (49,1%) |
71/192 (37%) |
0,034 |
|
• в семье, n (%) |
206/363 (56,7%) |
86/171 (50,3%) |
120/192 (62,5%) |
0,021 |
|
• интернат, дом инвалидов, n (%) |
2/363 (0,6%) |
1/171 (0,6%) |
1/192 (0,5%) |
0,728 |
|
Количество проживающих в семье, человек, Me (Q1; Q3) |
1 (1; 2) |
1 (1; 2) |
2 (1; 2) |
0,003 |
|
Семейное положение |
||||
|
• женат/замужем, n (%) |
81/362 (22,4%) |
31/171 (18,1%) |
50/191 (26,2%) |
0,103 |
|
• вдовец/вдова, n (%) |
257/362 (71%) |
130/171 (76%) |
127/191 (66,5%) |
0,039 |
|
• разведен / проживает отдельно от супруга, n (%) |
18/362 (5%) |
5/171 (2,9%) |
13/191 (6,8%) |
0,155 |
|
• холост / не замужем, n (%) |
4/362 (1,1%) |
4/171 (2,3%) |
0/191 (0%) |
0,047 |
|
• брак без регистрации, n (%) |
2/362 (0,6%) |
1/171 (0,6%) |
1/191 (0,5%) |
0,999 |
|
Наличие детей, n (%) |
334/364 (91,8%) |
156/171 (91,2%) |
178/193 (92,2%) |
0,729 |
|
Количество детей, человек, Me (Q1; Q3) |
1 (1; 2) |
1 (1; 2) |
1 (1; 2) |
0,645 |
|
Образование |
||||
|
• нет официального образования, n (%) |
2/362 (0,6%) |
0/170 (0%) |
2/192 (1%) |
0,501 |
|
• начальное / неполное начальное, n (%) |
45/362 (12,4%) |
24/170 (14,1%) |
21/192 (10,9%) |
0,442 |
|
• среднее/неполное среднее, n (%) |
70/362 (19,3%) |
28/170 (16,5%) |
42/192 (21,9%) |
0,252 |
|
• среднее специальное, n (%) |
98/362 (27,1%) |
48/170 (28,2%) |
50/192 (26%) |
0,710 |
|
• высшее / неполное высшее, n (%) |
129/362 (35,6%) |
61/170 (35,9%) |
68/192 (35,4%) |
0,993 |
|
• высшее + ученая степень, n (%) |
18/362 (5%) |
9/170 (5,3%) |
9/192 (4,7%) |
0,975 |
|
Частота вызова врача на дом из поликлиники, случаев, Me (Q1; Q3) |
0 (0; 2) |
1 (0; 2,8) |
0 (0; 2) |
0,118 |
|
Частота обращения в поликлинику, случаев, Me (Q1; Q3) |
4 (1; 10) |
4 (1,0; 9,8) |
4 (1,0; 10,5) |
0,344 |
|
Частота вызова СМП, случаев, Me (Q1; Q3) |
1 (0; 3) |
1 (0; 2) |
1 (0; 3) |
0,557 |
|
Итого все случаи обращения за мед. помощью, случаев, Me (Q1; Q3) |
8 (4; 14) |
8 (4; 14) |
8 (4; 14) |
0,959 |
|
Частота госпитализаций, случаев, Me (Q1; Q3) |
1 (1; 2) |
1 (1; 2) |
1 (1; 2) |
0,812 |
|
Экстренная причина госпитализации, n (%) |
27/342 (7,9%) |
10/161 (6,2%) |
17/181 (9,4%) |
0,276 |
|
Получает лекарственные средства по льготе, n (%) |
241/348 (69,3%) |
109/162 (67,3%) |
132/186 (71%) |
0,458 |
|
Продолжает работать, n (%) |
8/361 (2,2%) |
3/169 (1,8%) |
5/192 (2,6%) |
0,728 |
|
Возраст прекращения работы, лет, Me (Q1; Q3) |
60 (55; 69) |
60 (55; 70) |
60 (55; 68) |
0,887 |
|
Материальные возможности |
||||
|
• низкие, n (%) |
36/363 (9,9%) |
18/170 (10,6%) |
18/193 (9,3%) |
0,825 |
|
• средние, n (%) |
324/363 (89,3%) |
150/170 (88,2%) |
174/193 (90,2%) |
0,661 |
|
• высокие, n (%) |
3/363 (0,8%) |
2/170 (1,2%) |
1/193 (0,5%) |
0,602 |
|
Религия/вероисповедание |
||||
|
• неверующий, n (%) |
39/362 (10,8%) |
19/170 (11,2%) |
20/192 (10,4%) |
0,940 |
|
• православие, n (%) |
268/362 (74%) |
121/170 (71,2%) |
147/192 (76,6%) |
0,334 |
|
• ислам, n (%) |
10/362 (2,8%) |
4/170 (2,4%) |
6/192 (3,1%) |
0,755 |
|
• христианство (кроме православия), n (%) |
41/362 (11,3%) |
23/170 (13,5%) |
18/192 (9,4%) |
0,275 |
|
• другое, n (%) |
2/362 (0,6%) |
2/170 (1,2%) |
0/192 (0%) |
0,219 |
|
• отказ отвечать, n (%) |
2/362 (0,6%) |
1/170 (0,6%) |
1/192 (0,5%) |
0,999 |
|
Частота посещения церкви |
||||
|
• никогда, n (%) |
167/363 (46%) |
80/170 (47,1%) |
87/193 (45,1%) |
0,796 |
|
• иногда, n (%) |
176/363 (48,5%) |
86/170 (50,6%) |
90/193 (46,6%) |
0,528 |
|
• регулярно, n (%) |
20/363 (5,5%) |
4/170 (2,4%) |
16/193 (8,3%) |
0,025 |
|
Частота посещения гостей дома пациента |
||||
|
• ни разу, n (%) |
97/364 (26,6%) |
39/171 (22,8%) |
58/193 (30,1%) |
0,157 |
|
• 1–2 раза за год, n (%) |
115/364 (31,6%) |
57/171 (33,3%) |
58/193 (30,1%) |
0,557 |
|
• 1–2 раза в месяц, n (%) |
102/364 (28%) |
50/171 (29,2%) |
52/193 (26,9%) |
0,692 |
|
• 1–2 раза в неделю, n (%) |
46/364 (12,6%) |
24/171 (14%) |
22/193 (11,4%) |
0,54 |
|
• ежедневно, n (%) |
4/364 (1,1%) |
1/171 (0,6%) |
3/193 (1,6%) |
0,626 |
|
Частота посещения пациентом друзей или родственников |
||||
|
• ни разу, n (%) |
141/364 (38,7%) |
66/171 (38,6%) |
75/193 (38,9%) |
0,999 |
|
• 1–2 раза за год, n (%) |
121/364 (33,2%) |
60/171 (35,1%) |
61/193 (31,6%) |
0,534 |
|
• 1–2 раза в месяц, n (%) |
66/364 (18,1%) |
31/171 (18,1%) |
35/193 (18,1%) |
0,999 |
|
• 1–2 раза в неделю, n (%) |
33/364 (9,1%) |
13/171 (7,6%) |
20/193 (10,4%) |
0,472 |
|
• ежедневно, n (%) |
3/364 (0,8%) |
1/171 (0,6%) |
2/193 (1%) |
0,999 |
|
Частота выхода из дома |
||||
|
• ни разу, n (%) |
43/364 (11,8%) |
20/171 (11,7%) |
23/193 (11,9%) |
0,999 |
|
• 1–2 раза за год, n (%) |
21/364 (5,8%) |
11/171 (6,4%) |
10/193 (5,2%) |
0,767 |
|
• 1–2 раза в месяц, n (%) |
29/364 (8%) |
16/171 (9,4%) |
13/193 (6,7%) |
0,459 |
|
• 1–2 раза в неделю, n (%) |
117/364 (32,1%) |
56/171 (32,7%) |
61/193 (31,6%) |
0,881 |
|
• ежедневно, n (%) |
154/364 (42,3%) |
68/171 (39,8%) |
86/193 (44,6%) |
0,436 |
|
Пользование интернетом |
||||
|
• ни разу, n (%) |
299/364 (82,1%) |
139/171 (81,3%) |
160/193 (82,9%) |
0,865 |
|
• 1–2 раза за год, n (%) |
9/364 (2,5%) |
5/171 (2,9%) |
4/193 (2,1%) |
0,739 |
|
• 1–2 раза в месяц, n (%) |
10/364 (2,7%) |
5/171 (2,9%) |
5/193 (2,6%) |
0,999 |
|
• 1–2 раза в неделю, n (%) |
17/364 (4,7%) |
8/171 (4,7%) |
9/193 (4,7%) |
0,999 |
|
• ежедневно, n (%) |
29/364 (8%) |
14/171 (8,2%) |
15/193 (7,8%) |
0,999 |
|
Общение по телефону и/или интернету |
||||
|
• ни разу, n (%) |
23/364 (6,3%) |
9/171 (5,3%) |
14/193 (7,3%) |
0,581 |
|
• 1–2 раза за год, n (%) |
9/364 (2,5%) |
2/171 (1,2%) |
7/193 (3,6%) |
0,182 |
|
• 1–2 раза в месяц, n (%) |
15/364 (4,1%) |
10/171 (5,8%) |
5/193 (2,6%) |
0,192 |
|
• 1–2 раза в неделю, n (%) |
60/364 (16,5%) |
36/171 (21,1%) |
24/193 (12,4%) |
0,037 |
|
ежедневно, n (%) |
257/364 (70,6%) |
114/171 (66,7%) |
143/193 (74,1%) |
0,175 |
Примечания: таблица составлена авторами; p — значения получены при сравнении двух групп с использованием теста Манна — Уитни (для количественных показателей), а также точного теста Фишера и теста χ² Пирсона (для категориальных показателей); в таблице указано количество пациентов, которые были включены в анализ.
Notes: the table was compiled by the authors; p — the values were obtained by comparing the two groups using the Mann—Whitney test (for quantitative indicators), as well as Fisher’s exact test and Pearson’s χ² test (for categorical indicators); the table indicates the number of patients included in the analysis.
Для оценки психоэмоциональной сферы использованы 10 шкал для анализа когнитивных функций и эмоционального состояния. В результате выявлено, что пациенты с КЗНК в сравнении с пациентами без КЗНК были более эмоционально стабильны. Так, пациенты с КЗНК в сравнении с пациентами без КЗНК характеризовались статистически значимо меньшими значениями оценки по гериатрическим шкалам депрессии GDS-15 и GDS-30 (p = 0,007 и 0,027 соответственно), увеличение оценки по шкале GDS-15 на каждый балл было ассоциировано со снижением шансов наличия КЗНК в среднем в 1,08 (95 % ДИ: 1,02; 1,14) раза (p = 0,01), увеличение оценки по шкале GDS-30 на каждый балл было ассоциировано со снижением шансов наличия КЗНК в среднем в 1,04 (95 % ДИ: 1,00; 1,07) раза (p = 0,032) (табл. 2).
Таблица 2. Гериатрические факторы риска: психоэмоциональный статус
Table 2. Geriatric risk factors: mental and emotional status
|
Характеристика |
Все пациенты (n = 367) |
Клинически значимые небольшие кровотечения |
Уровень статистической значимости, p |
|
|
Нет (n = 172) |
Есть (n = 195) |
|||
|
Тест «Мини-ког»: воспроизведение слов, баллов, Me (Q1; Q3) |
2 (1; 3) |
2 (1; 3) |
2 (1; 3) |
0,910 |
|
Тест «Мини-ког»: рисование часов, баллов, Me (Q1; Q3) |
1 (1; 2) |
1 (1; 2) |
1 (1; 2) |
0,269 |
|
Тест «Мини-ког»: общий, баллов, Me (Q1; Q3) |
3 (2; 4) |
3 (2; 4) |
3 (2; 4) |
0,597 |
|
Тест «Мини-ког» |
||||
|
есть когнитивные нарушения (0–3 балла), n (%) |
217/367 (59,1%) |
103/172 (59,9%) |
114/195 (58,5%) |
0,782 |
|
• нет когнитивных нарушений (4–5 баллов), n (%) |
150/367 (40,9%) |
69/172 (40,1%) |
81/195 (41,5%) |
0,782 |
|
Краткая шкала оценки психического статуса (MMSE), баллов, Me (Q1; Q3) |
26 (23; 27,5) |
26 (23; 28) |
26 (23; 27) |
0,597 |
|
Краткая шкала оценки психического статуса (MMSE) |
||||
|
• нет когнитивных нарушений (28–30 баллов), n (%) |
88/351 (25,1%) |
44/161 (27,3%) |
44/190 (23,2%) |
0,674 |
|
• преддементные когнитивные нарушения (24–27 баллов), n (%) |
136/351 (38,7%) |
59/161 (36,6%) |
77/190 (40,5%) |
0,674 |
|
• деменция легкой степени (20–23 балла), n (%) |
96/351 (27,4%) |
43/161 (26,7%) |
53/190 (27,9%) |
0,674 |
|
• деменция умеренной степени выраженности (11–19 баллов), n (%) |
30/351 (8,5%) |
14/161 (8,7%) |
16/190 (8,4%) |
0,674 |
|
• тяжелая деменция (0–10 баллов), n (%) |
1/351 (0,3%) |
1/161 (0,6%) |
0/190 (0%) |
0,674 |
|
Монреальская шкала оценки когнитивных функций (Moca), баллов, Me (Q1; Q3) |
22 (19; 25) |
23 (18,8; 25,0) |
22 (20; 25) |
0,599 |
|
Монреальская шкала оценки когнитивных функций (Moca): |
||||
|
• нет когнитивных нарушений (26–30 баллов), n (%) |
75/354 (21,2%) |
36/164 (22%) |
39/190 (20,5%) |
0,744 |
|
• есть когнитивные нарушения (0–25 баллов), n (%) |
279/354 (78,8%) |
128/164 (78%) |
151/190 (79,5%) |
0,744 |
|
Тест вербальных ассоциаций: литеральные (ТВА-Л), баллов, Me (Q1; Q3) |
9 (6; 11) |
9 (6; 11) |
8,5 (6; 11) |
0,805 |
|
13 и более баллов, n (%) |
52/352 (14,8%) |
23/162 (14,2%) |
29/190 (15,3%) |
0,779 |
|
Тест вербальных ассоциаций: категориальные (ТВА-К), баллов, Me (Q1; Q3) |
12 (9; 15) |
12 (8; 15) |
12 (9; 15) |
0,775 |
|
13 и более баллов, n (%) |
151/352 (42,9%) |
71/162 (43,8%) |
80/190 (42,1%) |
0,745 |
|
Отношение ТВА-Л/ТВА-К, баллов, Me (Q1; Q3) |
0,8 (0,5; 1) |
0,8 (0,6; 1) |
0,8 (0,5; 0,9) |
0,69 |
|
Бостонский тест называния, баллов, Me (Q1; Q3) |
34 (28; 37) |
34 (29; 37) |
33 (28; 37) |
0,32 |
|
Литеральные подсказки, баллов, Me (Q1; Q3) |
4 (1; 7) |
4 (1; 7) |
4 (1; 8) |
0,313 |
|
Категориальные подсказки, баллов, Me (Q1; Q3) |
0 (0; 4) |
0 (0; 3) |
1 (0; 5) |
0,114 |
|
Тест на запоминание цифр в прямом порядке, баллов, Me (Q1; Q3) |
8 (6; 10) |
8 (6; 10) |
8 (6; 10) |
0,801 |
|
Максимальная длина ряда, баллов, Me (Q1; Q3) |
5 (4; 6) |
5 (4; 6) |
5 (4; 6) |
0,832 |
|
Тест «Символы и цифры», баллов, Me (Q1; Q3) |
17 (10; 21) |
17 (10; 21) |
17 (11; 21) |
0,702 |
|
Тест запоминания 10 слов (WLT): немедленная память, баллов, Me (Q1; Q3) |
16 (12; 19) |
16 (12; 19) |
16 (13; 19) |
0,786 |
|
Тест запоминания 10 слов (WLT): отсроченная память, баллов, Me (Q1; Q3) |
4 (2; 5) |
4 (2; 5,3) |
4 (2; 5) |
0,541 |
|
Тест запоминания 10 слов (WLT): способность к обучению, баллов, Me (Q1; Q3) |
8 (6; 10) |
9 (6; 10) |
8 (6; 10) |
0,473 |
|
Когнитивная субшкала оценки болезни Альцгеймера (ADAS-cog), баллов, Me (Q1; Q3) |
17,4 (11,6; 25,0) |
18,2 (11,8; 25,6) |
16,4 (11,3; 24,4) |
0,505 |
|
Гериатрическая шкала депрессии GDS-15, баллов, Me (Q1; Q3) |
5 (2; 8) |
5 (3; 8) |
4 (2; 7) |
0,007 |
|
Гериатрическая шкала депрессии GDS-15: |
||||
|
норма (0–4 балла), n (%) |
182/367 (49,6%) |
70/172 (40,7%) |
112/195 (57,4%) |
0,001 |
|
• вероятная депрессия (5–15 баллов), n (%) |
185/367 (50,4%) |
102/172 (59,3%) |
83/195 (42,6%) |
0,001 |
|
Гериатрическая шкала депрессии GDS-30, баллов, Me (Q1; Q3) |
11 (6; 16) |
12 (7,0; 16,3) |
10 (5,5; 15,0) |
0,027 |
|
Гериатрическая шкала депрессии GDS-30: |
||||
|
• норма (0–9 баллов), n (%) |
153/351 (43,6%) |
63/164 (38,4%) |
90/187 (48,1%) |
0,171 |
|
• легкая депрессия (10–19 баллов), n (%) |
163/351 (46,4%) |
82/164 (50%) |
81/187 (43,3%) |
0,171 |
|
• выраженная депрессия (20–30 баллов), n (%) |
35/351 (10%) |
19/164 (11,6%) |
16/187 (8,6%) |
0,171 |
Примечания: таблица составлена авторами; p — значения получены при сравнении двух групп с использованием теста Манна — Уитни (для количественных показателей), а также точного теста; в таблице указано количество пациентов, которые были включены в анализ. Сокращения: MMSE — краткая шкала оценки психического статуса; ТВА-Л — тест вербальных ассоциаций: литеральлные; ТВА-К — тест вербальных ассоциаций: категориальные; WLТ — тест запоминания 10 слов; GDS — гериатрическая шкала депрессии.
Notes: the table was compiled by the authors; p — the values were obtained by comparing the two groups using the Mann—Whitney test (for quantitative indicators), as well as the exact test; the table indicates the number of patients included in the analysis. Abbreviations: MMSE — Mini-mental State Examination; ТВА-Л — verbal fluency test (literal); ТВА-К — verbal fluency test (category); WLT — 10-word-list recall test; GDS — Geriatric Depression Scale.
Для оценки функциональной активности и физического здоровья были изучены 13 параметров, среди которых: скрининг на наличие старческой астении, самооценка качества жизни и состояния здоровья, базовая и инструментальная функциональная активность, мобильность, мышечная сила, состояние питания, наличие хронического болевого синдрома, ортостатической гипотензии, сенсорных дефицитов, недержания мочи и кала, падений, использование вспомогательных средств. В результате было выявлено, что пациенты с КЗНК в сравнении с пациентами без КЗНК реже имели старческую астению, лучше оценивали свое качество жизни и состояние здоровья, были более активны при выполнении повседневных дел, более мобильны и реже применяли вспомогательные средства. Так, пациенты с КЗНК в сравнении с пациентами без КЗНК характеризовались лучшим настроением (ОШ = 0,65 (95 % ДИ: 0,43; 0,99), p = 0,043) и статистически значимо чаще не имели старческой астении по опроснику «Возраст не помеха» (p = 0,015). У пациентов с КЗНК в сравнении с пациентами без КЗНК была отмечена тенденция к более высоким оценкам качества жизни и состояния здоровья по ВАШ (p = 0,053 и 0,05 соответственно), увеличение оценки качества жизни по ВАШ на каждый 1 балл было ассоциировано с увеличением шансов наличия кровотечения в среднем в 1,09 (95 % ДИ: 0,99; 1,21) раза (p = 0,084), увеличение оценки состояния здоровья — в 1,11 (95 % ДИ: 0,99; 1,26) раза (p = 0,07). Пациенты с КЗНК в сравнении с пациентами без КЗНК характеризовались статистически значимо более высокими значениями шкалы Лоутона (p = 0,004), увеличение оценки по данной шкале на каждый 1 балл было ассоциировано с увеличением шансов наличия КЗНК в среднем в 1,17 (95 % ДИ: 1,04; 1,32) раза (p = 0,008). Наличие КЗНК было ассоциировано с более высоким временем тандемного положения (p = 0,014), увеличение времени на каждую секунду было ассоциировано с увеличением шансов наличия КЗНК в среднем в 1,05 (95 % ДИ: 1,01; 1,10) раза (p = 0,013). Пациенты с КЗНК в сравнении с пациентами без КЗНК характеризовались статистически значимо меньшими оценками в теста с 5-кратным вставанием со стула и теста «Встань и иди» (p = 0,045 и 0,025 соответственно), увеличение оценок по данным шкалам на каждые 10 единиц было ассоциировано со снижением шансов КЗНК в среднем в 1,16 (95 % ДИ: 1,01; 1,34) раза (p = 0,045) и в 1,23 (95 % ДИ: 1,02; 1,50) раза (p = 0,03) соответственно (табл. 3).
Таблица 3. Гериатрические факторы риска: функциональный и физический статус
Table 3. Geriatric risk factors: functional and physical status
|
Характеристика |
Все пациенты (n = 367) |
Клинически значимые небольшие кровотечения |
Уровень статистической значимости, p |
|
|
Нет (n =172) |
Есть (n = 195) |
|||
|
«Возраст не помеха» (вес), n (%) |
117/364 (32,1%) |
60/171 (35,1%) |
57/193 (29,5%) |
0,257 |
|
«Возраст не помеха» (снижение зрения или слуха), n (%) |
298/364 (81,9%) |
144/171 (84,2%) |
154/193 (79,8%) |
0,275 |
|
«Возраст не помеха» (травмы, связанные с падением), n (%) |
106/363 (29,2%) |
47/170 (27,6%) |
59/193 (30,6%) |
0,541 |
|
«Возраст не помеха» (настроение), n (%) |
186/364 (51,1%) |
97/171 (56,7%) |
89/193 (46,1%) |
0,043 |
|
«Возраст не помеха» (проблемы с памятью), n (%) |
240/363 (66,1%) |
111/170 (65,3%) |
129/193 (66,8%) |
0,756 |
|
«Возраст не помеха» (недержание мочи), n (%) |
206/364 (56,6%) |
97/171 (56,7%) |
109/193 (56,5%) |
0,962 |
|
«Возраст не помеха» (трудности при ходьбе), n (%) |
218/364 (59,9%) |
106/171 (62%) |
112/193 (58%) |
0,442 |
|
Опросник «Возраст не помеха», баллов, Me (Q1; Q3) |
4 (3; 5) |
4 (3; 5) |
4 (2; 5) |
0,245 |
|
Опросник «Возраст не помеха» |
||||
|
нет астении (0–2 балла), n (%) |
86/364 (23,6%) |
29/171 (17%) |
57/193 (29,5%) |
0,008 |
|
• преастения (3–4 балла), n (%) |
151/364 (41,5%) |
80/171 (46,8%) |
71/193 (36,8%) |
0,063 |
|
• астения (5–7 баллов), n (%) |
127/364 (34,9%) |
62/171 (36,3%) |
65/193 (33,7%) |
0,663 |
|
Самооценка качества жизни по визуально-аналоговой шкале (ВАШ), баллов, Me (Q1; Q3) |
6 (5; 8) |
6 (4; 7,5) |
6 (5; 8) |
0,053 |
|
Самооценка состояния здоровья по визуально-аналоговой шкале (ВАШ), баллов, Me (Q1; Q3) |
5 (4; 6) |
5 (4; 6) |
5 (4; 7) |
0,050 |
|
Шкала оценки базовой функциональной активности (шкала Бартел), баллов, Me (Q1; Q3) |
90 (85; 95) |
90 (80; 95) |
90 (85; 95) |
0,380 |
|
Шкала оценки базовой функциональной активности (шкала Бартел) |
||||
|
• нет зависимости от посторонней помощи (96–100 баллов), n (%) |
67/364 (18,4%) |
34/171 (19,9%) |
33/193 (17,1%) |
0,570 |
|
• легкая зависимость от посторонней помощи (91–95 баллов), n (%) |
80/364 (22%) |
35/171 (20,5%) |
45/193 (23,3%) |
0,614 |
|
• умеренная зависимость от посторонней помощи (61–90), n (%) |
203/364 (55,8%) |
94/171 (55%) |
109/193 (56,5%) |
0,893 |
|
• выраженная зависимость от посторонней помощи (21–60 баллов), n (%) |
14/364 (3,8%) |
8/171 (4,7%) |
6/193 (3,1%) |
0,608 |
|
• полная зависимость от посторонней помощи (0–20 баллов), n (%) |
0/364 (0%) |
0/171 (0%) |
0/193 (0%) |
– |
|
Шкала оценки инструментальной функциональной активности в повседневной жизни (шкала Лоутона), баллов, Me (Q1; Q3) |
7 (5; 8) |
6 (5; 7,5) |
7 (5; 8) |
0,004 |
|
Функциональная активность по вопроснику FAQ, баллов, Me (Q1; Q3) |
8 (4; 14) |
9 (5; 15) |
8 (3; 13) |
0,106 |
|
Краткая шкала оценки питания (MNA), баллов, Me (Q1; Q3) |
22 (19,5; 24) |
22 (19,5; 24) |
22,5 (20; 24,5) |
0,117 |
|
Краткая шкала оценки питания (MNA) |
||||
|
• нормальный статус питания (23,5–30 баллов), n (%) |
121/350 (34,6%) |
51/164 (31,1%) |
70/186 (37,6%) |
0,246 |
|
• риск недостаточности питания / мальнутриции (17–23,5 балла), n (%) |
204/350 (58,3%) |
102/164 (62,2%) |
102/186 (54,8%) |
0,215 |
|
• недостаточность питания / мальнутриция (менее 17 баллов), n (%) |
25/350 (7,1%) |
11/164 (6,7%) |
14/186 (7,5%) |
0,928 |
|
Краткая батарея тестов физического функционирования (SPPB), баллов, Me (Q1; Q3) |
5 (3; 6) |
4 (3; 6) |
5 (3; 6) |
0,999 |
|
Краткая батарея тестов физического функционирования (SPPB) |
||||
|
• нет старческой астении (10–12 баллов), n (%) |
18/360 (5%) |
5/169 (3%) |
13/191 (6,8%) |
0,155 |
|
• преастения (8–9 баллов), n (%) |
41/360 (11,4%) |
19/169 (11,2%) |
22/191 (11,5%) |
>0,999 |
|
• старческая астения (7 и менее баллов), n (%) |
301/360 (83,6%) |
145/169 (85,8%) |
156/191 (81,7%) |
0,35 |
|
Тандемное положение, секунд, Me (Q1; Q3) |
2 (0; 6,5) |
1 (0; 4,2) |
2,3 (0; 8,5) |
0,014 |
|
Определение скорости ходьбы на 4 метра, секунд, Me (Q1; Q3) |
9 (6,7; 15,3) |
9,5 (7,0; 15,3) |
8,9 (6,3; 14,9) |
0,27 |
|
Скорость ходьбы, м/сек, Me (Q1; Q3) |
0,4 (0,3; 0,6) |
0,4 (0,3; 0,6) |
0,4 (0,3; 0,6) |
0,552 |
|
Тест с 5-кратным подъемом со стула, секунд, Me (Q1; Q3) |
15,9 (0; 24,5) |
17,7 (3,5; 26,3) |
15,5 (0; 20,5) |
0,045 |
|
Тест с 5-кратным подъемом со стула |
||||
|
• не может или более 60 секунд, n (%) |
100/359 (27,9%) |
47/169 (27,8%) |
53/190 (27,9%) |
0,999 |
|
• более 16,7 секунды, n (%) |
168/359 (46,8%) |
81/169 (47,9%) |
87/190 (45,8%) |
0,711 |
|
• 13,7–16,69 секунды, n (%) |
48/359 (13,4%) |
24/169 (14,2%) |
24/190 (12,6%) |
0,755 |
|
• 11,2–13,69 секунды, n (%) |
27/359 (7,5%) |
13/169 (7,7%) |
14/190 (7,4%) |
0,999 |
|
• 11,19 секунд и менее, n (%) |
16/359 (4,5%) |
4/169 (2,4%) |
12/190 (6,3%) |
0,125 |
|
Тест «Встань и иди», секунд, Me (Q1; Q3) |
16,1 (12,0; 21,4) |
17,1 (12,9; 22,8) |
15,3 (11,5; 20,4) |
0,025 |
|
Тест «Встань и иди» |
||||
|
• норма (10 и менее секунд), n (%) |
59/348 (17%) |
26/163 (16%) |
33/185 (17,8%) |
0,743 |
|
• промежуточный (11–13 секунд), n (%) |
289/348 (83%) |
137/163 (84%) |
152/185 (82,2%) |
0,787 |
|
• нарушение походки и равновесия (14 и более секунд), n (%) |
0/348 (0%) |
0/163 (0%) |
0/185 (0%) |
– |
|
Равновесие на одной ноге, секунд, Me (Q1; Q3) |
1,2 (0; 2,8) |
1,0 (0; 2,6) |
1,5 (0; 3) |
0,321 |
|
Динамометрия: сила сжатия кисти, килограмм, Me (Q1; Q3) |
12,5 (9,0; 17,5) |
12,5 (9,2; 17,3) |
12,3 (9,0; 17,9) |
0,869 |
|
Сила сжатия кисти (женщины), килограмм, Me (Q1; Q3) |
10,5 (7,8; 13,3) |
10,5 (8,0; 14,0) |
10,3 (7,5; 13,0) |
0,410 |
|
Сила сжатия кисти (мужчины), килограмм, Me (Q1; Q3) |
19,8 (16,4; 22,6) |
19,8 (17,6; 2,02) |
19,3 (16,3; 23,3) |
0,953 |
|
Снижение сил силы сжатия кисти, n (%) |
352/362 (97,2%) |
166/170 (97,6%) |
186/192 (96,9%) |
0,755 |
|
Снижение сил силы сжатия кисти (женщины), n (%) |
243/250 (97,2%) |
120/123 (97,6%) |
123/127 (96,9%) |
0,999 |
|
Снижение сил силы сжатия кисти (мужчины), n (%) |
109/112 (97,3%) |
46/47 (97,9%) |
63/65 (96,9%) |
0,999 |
|
Ортостатическая гипотензия, n (%) |
72/363 (19,8%) |
34/171 (19,9%) |
38/192 (19,8%) |
0,983 |
|
Предвестники ортостатической гипотензии, n (%) |
199/356 (55,9%) |
95/168 (56,5%) |
104/188 (55,3%) |
0,816 |
|
Дефицит слуха, n (%) |
294/364 (80,8%) |
136/171 (79,5%) |
158/193 (81,9%) |
0,573 |
|
Дефицит зрения, n (%) |
357/361 (98,9%) |
169/170 (99,4%) |
188/191 (98,4%) |
0,625 |
|
Хроническая боль, n (%) |
340/363 (93,7%) |
161/170 (94,7%) |
179/193 (92,7%) |
0,444 |
|
Недержание мочи, n (%) |
212/364 (58,2%) |
97/171 (56,7%) |
115/193 (59,6%) |
0,581 |
|
Трудности при мочеиспускании, n (%) |
86/349 (24,6%) |
42/163 (25,8%) |
44/186 (23,7%) |
0,648 |
|
Никтурия, n (%) |
316/351 (90%) |
150/164 (91,5%) |
166/187 (88,8%) |
0,401 |
|
Недержание кала, n (%) |
37/362 (10,2%) |
16/170 (9,4%) |
21/192 (10,9%) |
0,632 |
|
Падения за прошлый год, n (%) |
158/363 (43,5%) |
70/171 (40,9%) |
88/192 (45,8%) |
0,347 |
|
Количество падений за прошлый год |
||||
|
• нет, n (%) |
205/363 (56,5%) |
101/171 (59,1%) |
104/192 (54,2%) |
0,351 |
|
• 1 раз, n (%) |
66/363 (18,2%) |
29/171 (17%) |
37/192 (19,3%) |
0,697 |
|
• 2 и более, n (%) |
92/363 (25,3%) |
41/171 (24%) |
51/192 (26,6%) |
0,696 |
Примечания: таблица составлена авторами; p — значения получены при сравнении двух групп с использованием теста Манна — Уитни (для количественных показателей), а также точного теста Фишера и теста χ² Пирсона (для категориальных показателей); в таблице указано количество пациентов, которые были включены в анализ.
Note: the table was compiled by the authors; p — the values were obtained by comparing the two groups using the Mann—Whitney test (for quantitative indicators), as well as Fisher’s exact test and Pearson’s χ² test (for categorical indicators); the table indicates the number of patients included in the analysis.
Пациенты с КЗНК в сравнении с пациентами без КЗНК характеризовались статистически значимо меньшей частотой применения вспомогательных средств (p = 0,022) (табл. 4).
Таблица 4. Гериатрические факторы риска: физический статус (использование вспомогательных средств)
Table 4. Geriatric risk factors: physical status (use of assistive devices)
|
Характеристика |
Все пациенты (n = 367) |
Клинически значимые небольшие кровотечения |
Уровень статистической значимости, p |
|
|
Нет (n = 172) |
Есть (n = 195) |
|||
|
Использует очки/линзы, n (%) |
293/364 (80,5%) |
142/171 (83%) |
151/193 (78,2%) |
0,248 |
|
Использует слуховой аппарат, n (%) |
35/364 (9,6%) |
19/171 (11,1%) |
16/193 (8,3%) |
0,362 |
|
Использует зубные протезы, n (%) |
268/364 (73,6%) |
120/171 (70,2%) |
148/193 (76,7%) |
0,160 |
|
Использует трость, n (%) |
210/364 (57,7%) |
103/171 (60,2%) |
107/193 (55,4%) |
0,356 |
|
Использует костыли, n (%) |
10/364 (2,7%) |
7/171 (4,1%) |
3/193 (1,6%) |
0,200 |
|
Использует ходунки, n (%) |
28/364 (7,7%) |
17/171 (9,9%) |
11/193 (5,7%) |
0,130 |
|
Использует средства опоры, n (%) |
222/363 (61,2%) |
109/171 (63,7%) |
113/192 (58,9%) |
0,340 |
|
Использует ортопедическую обувь, n (%) |
42/363 (11,6%) |
19/170 (11,2%) |
23/193 (11,9%) |
0,826 |
|
Использует ортопедические стельки, n (%) |
67/364 (18,4%) |
28/171 (16,4%) |
39/193 (20,2%) |
0,346 |
|
Использует ортопедический корсет, n (%) |
32/364 (8,8%) |
16/171 (9,4%) |
16/193 (8,3%) |
0,720 |
|
Использует урологические прокладки, n (%) |
134/363 (36,9%) |
68/170 (40%) |
66/193 (34,2%) |
0,253 |
|
Использует памперсы или впитывающие пеленки, n (%) |
37/364 (10,2%) |
20/171 (11,7%) |
17/193 (8,8%) |
0,363 |
|
Количество вспомогательных средств, единицы, Me (Q1; Q3) |
3 (2; 4) |
3 (2; 4) |
3 (2; 4) |
0,316 |
|
Использование любого вспомогательного средства, n (%) |
354/364 (97,3%) |
170/171 (99,4%) |
184/193 (95,3%) |
0,022 |
Примечания: таблица составлена авторами; p — значения получены при сравнении двух групп с использованием теста Манна — Уитни (для количественных показателей), а также точного теста Фишера и теста χ² Пирсона (для категориальных показателей); втаблице указано количество пациентов, которые были включены в анализ.
Notes: the table was compiled by the authors; p — the values were obtained by comparing the two groups using the Mann—Whitney test (for quantitative indicators), as well as Fisher’s exact test and Pearson’s χ² test (for categorical indicators); the table indicates the number of patients included in the analysis.
Для расчета индекса хрупкости использовали модель накопления дефицитов, подразумевающую оценку 46 дефицитов по шкале Rockwood [18] и 34 дефицитов по шкале, которая использовалась в исследовании SPRINT [19]. В результате анализа индексов хрупкости было получено, что пациенты с КЗНК в сравнении с пациентами без КЗНК были менее хрупкими согласно индексу хрупкости, который использовался для расчета в исследовании SPRINT. Так, наличие КЗНК было статистически значимо ассоциировано с более низкими оценками по шкале SPRINT (p = 0,005), увеличение значений индекса на каждые 0,1 единицы было ассоциировано со снижением шансов КЗНК в среднем в 1,46 [ 1,14; 1,88] раза (p = 0,003) (табл. 5).
Таблица 5. Гериатрические факторы риска: индексы хрупкости
Table 5. Geriatric risk factors: frailty indices
|
Характеристика |
Все пациенты (n = 367) |
Клинически значимые небольшие кровотечения |
Уровень статистической значимости, p |
|
|
Нет (n = 172) |
Есть (n = 195) |
|||
|
Индекс хрупкости по шкале Rockwood |
0,36 (0,29; 0,44) |
0,37 (0,31; 0,44) |
0,35 (0,29; 0,43) |
0,172 |
|
Старческая астения по шкале Rockwood |
||||
|
Крепкий ≤ 0,1 |
0/367 (0 %) |
0/172 (0 %) |
0/195 (0 %) |
- |
|
Преастения 0,11–0,20 |
13/367 (3,5 %) |
6/172 (3,5 %) |
7/195 (3,6 %) |
0,999 |
|
Астения ≥ 0,21 |
354/367 (96,5 %) |
166/172 (96,5 %) |
188/195 (96,4 %) |
0,999 |
|
Индекс хрупкости по шкале SPRINT |
0,37 (0,31; 0,43) |
0,39 (0,33; 0,44) |
0,36 (0,31; 0,42) |
0,005 |
|
Старческая астения по шкале SPRINT |
||||
|
Крепкий ≤ 0,1 |
0/367 (0 %) |
0/172 (0 %) |
0/195 (0 %) |
- |
|
Преастения 0,11–0,20 |
5/367 (1,4 %) |
1/172 (0,6 %) |
4/195 (2,1 %) |
0,377 |
|
Астения ≥ 0,21 |
362/367 (98,6 %) |
171/172 (99,4 %) |
191/195 (97,9 %) |
0,377 |
Примечания: таблица составлена авторами; p — значения получены при сравнении двух групп с использованием теста Манна — Уитни (для количественных показателей), а также точного теста Фишера и теста χ² Пирсона (для категориальных показателей). Сокращение: SPRINT — шкала оценки индекса хрупкости.
Notes: the table was compiled by the authors; p — the values were obtained by comparing the two groups using the Mann—Whitney test (for quantitative indicators), as well as Fisher’s exact test and Pearson’s χ² test (for categorical indicators). Abbreviations: SPRINT — Systolic Blood Pressure Intervention Trial.
Данное исследование представляет системный подход к комплексной гериатрической оценке, основанный на анализе четырех фундаментальных доменов: социального функционирования, психоэмоционального состояния, физического здоровья и функциональных возможностей. Методология исследования позволяет осуществить всесторонний анализ состояния пациентов пожилого возраста с учетом современных принципов гериатрической науки. Полученные данные обеспечивают целостное понимание взаимосвязей между различными аспектами гериатрического статуса, что имеет большое значение для разработки персонализированных подходов в гериатрической практике.
Многофакторный анализ прогнозирования вероятности развития клинически значимых небольших кровотечений
В таблице 6 представлена многофакторная модель для прогнозирования вероятности КЗНК, разработанная с использованием пошагового отбора предикторов с исключением на основании информационного критерия Акаике (AIC). Полученная модель характеризовалась значением псевдо-R² Найджелкерке равным 0,1 (скорректированное значение — 0,05), коэффициентом DXY Соммерса равным 0,27 (скорректированное значение — 0,23) и AUC равным 0,64 [ 95 % ДИ: 0,58; 0,69] (скорректированное значение — 0,61) (рис. 2, 3). На основании коэффициентов модели была разработана прогностическая номограмма для определения вероятности развития КЗНК на фоне приема ПОАК (рис. 4).
Таблица 6. Коэффициенты в полученной модели прогнозирования вероятности клинически значимого небольшого кровотечения
Table 6. Coefficients in the resulting model for predicting the probability of clinically relevant non-major bleeding
|
Предиктор |
β (SE) |
ОШ |
95 % ДИ |
p |
VIF |
|
Свободный член |
2,15 (1,62) |
– |
– |
– |
– |
|
Количество проживающих в семье |
0,28 (0,1) |
1,32 |
1,10; 1,62 |
0,005 |
1,06 |
|
Индекс Бартел |
-0,02 (0,01) |
0,98 |
0,96; 1,01 |
0,239 |
1,65 |
|
Индекс Лоутон |
0,21 (0,08) |
1,24 |
1,06; 1,45 |
0,008 |
1,53 |
|
Тест «Встань и иди» (сек.) |
-0,01 (0,01) |
0,99 |
0,96; 1,01 |
0,237 |
1,35 |
|
Использование любого вспомогательного средства |
-2,3 (1,08) |
0,10 |
0,01; 0,57 |
0,033 |
1,02 |
Примечания: таблица составлена авторами; p — значения получены с использованием теста Вальда. Сокращения: ДИ — доверительный интервал; ОШ — отношение шансов; SE — standard error, стандартная ошибка; VIF — variance inflation factor, фактор инфляции дисперсии.
Notes: the table was compiled by the authors; p — the values were obtained using the Wald test. Abbreviations: CI — confidence interval; OR — odds ratio; SE — standard error; VIF — variance inflation factor.
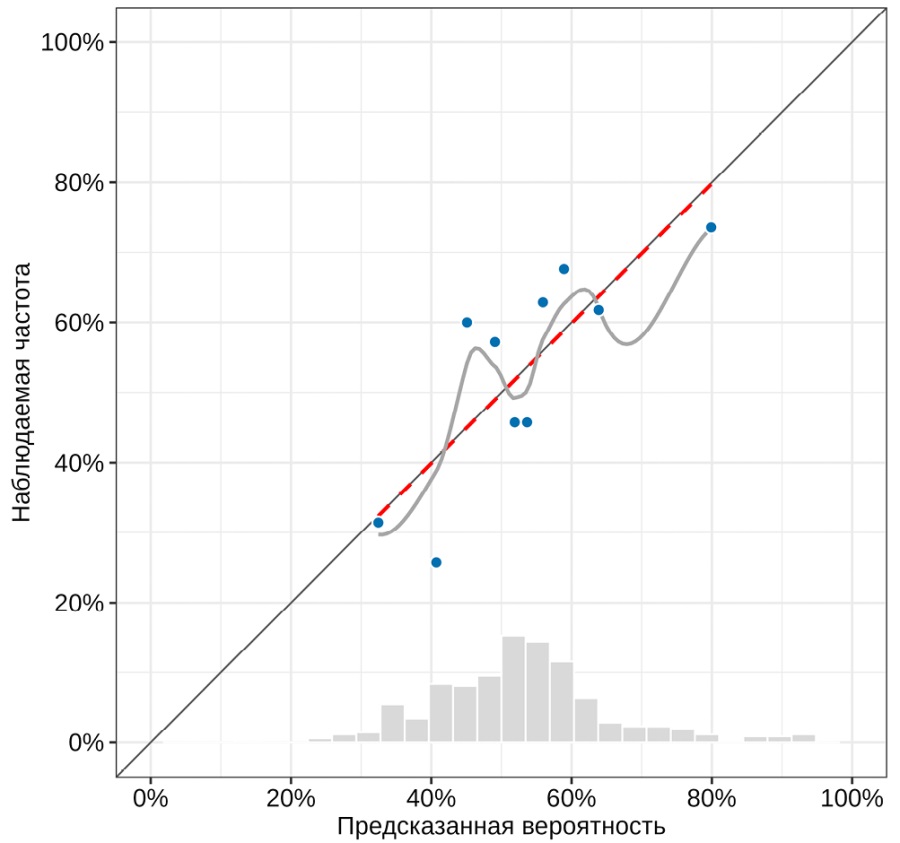
Рис 2. Калибровочная кривая для предсказаний, полученных с использованием модели
Примечание: рисунок выполнен авторами.
Fig. 2. Calibration curve for the predictions obtained using the model
Note: performed by the authors.
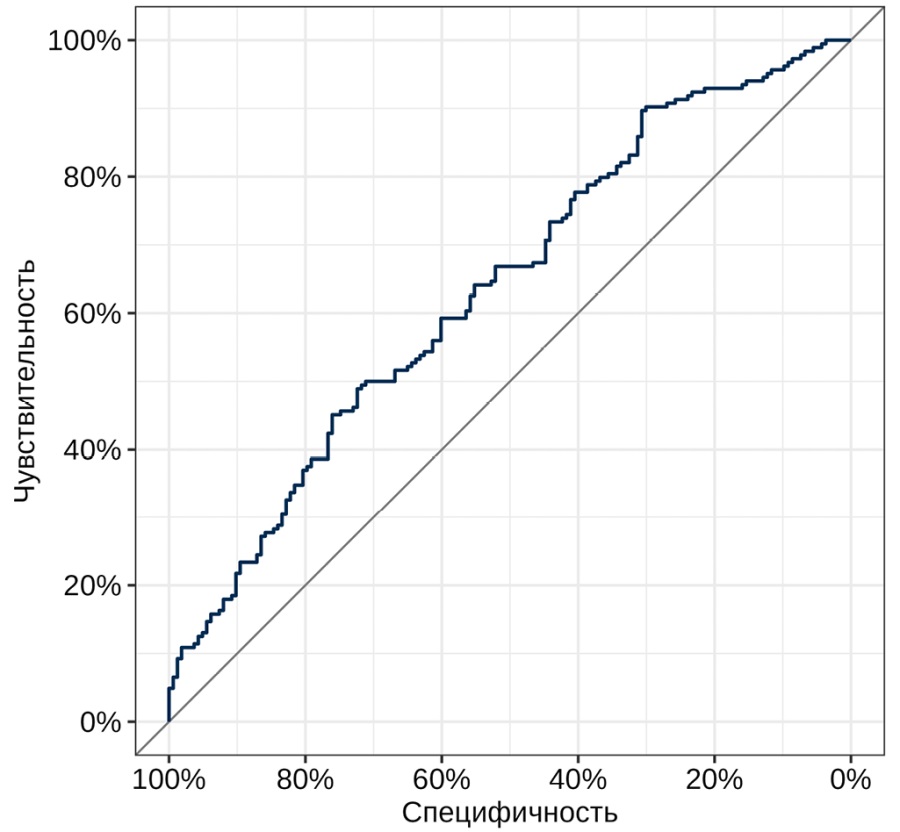
Рис 3. ROC-кривая для предсказаний, полученных с использованием модели
Примечание: рисунок выполнен авторами.
Fig. 3. ROC curve for the predictions obtained using the model
Note: performed by the authors.

Рис. 4. Номограмма для прогнозирования вероятности развития клинически значимого небольшого кровотечения
Примечания: рисунок выполнен авторами; для оценки вероятности события необходимо определить балл, соответствующий значению предиктора, опустив нормаль на соответствующую шкалу, затем необходимо найти сумму баллов и, опустив нормаль на соответствующую шкалу, найти оценку значения линейного предиктора (логарифма шансов события) и вероятности события.
Fig. 4. Nomogram to predict the probability of clinically relevant non-major bleeding
Notes: performed by the authors; to estimate the probability of an event, it is necessary to determine the score corresponding to the value of the predictor by dropping the normal to the appropriate scale; then, it is necessary to find the total score and, by dropping the normal to the appropriate scale, estimate the linear predictor (log odds) and the probability of the event.
При использовании в качестве порогового значения предсказанной вероятности КЗНК 55 % полученная модель характеризовалась 59,9 % [ 95 % ДИ: 54,6; 65,1] прогностической точностью, 48,9 % [ 95 % ДИ: 41,5; 56,4] чувствительностью и 72,4 % [ 95 % ДИ: 64,9; 79,1] специфичностью, прогностическое значение положительного результата составило 66,7 % [ 95 % ДИ: 58; 74,5], прогностическое значение отрицательного результата — 55,7 % [ 95 % ДИ: 48,7; 62,5].
Дополнительные результаты исследования
Дополнительных результатов в ходе исследования не получено.
ОБСУЖДЕНИЕ
Резюме основного результата исследования
Анализ гериатрических предикторов риска КЗНК при антикоагулянтной терапии у пациентов с ФП ≥ 80 лет выявил значимые факторы во всех четырех областях комплексной гериатрической оценки: социальной, психоэмоциональной, физической и функциональной.
Многофакторный регрессионный анализ позволил разработать прогностическую модель риска КЗНК. На основе полученных коэффициентов была создана номограмма для оценки вероятности развития кровотечений при терапии ПОАК. Значимыми прогностическими факторами выступили: количество проживающих в семье, индекс Бартел, индекс Лоутон, тест «Встань и иди» и использование вспомогательных средств. Разработанная модель показала следующие характеристики: точность прогноза — 59,9 %, чувствительность — 48,9 %, специфичность — 72,4 %. Прогностическое значение положительного результата составило 66,7 %, прогностическое значение отрицательного результата — 55,7 %.
Ограничения исследования
Основными ограничениями исследования являются малая выборка и связанная с этим недостаточная статистическая мощность. А также, с одной стороны, данное наблюдательное исследование реальной клинической практики не дает возможности оценить комплаенс пациентов в отношении приема ПОАК, а также наличия КЗНК в группе хрупких пациентов (или пациентов со старческой астенией), однако, с другой стороны, отражает картину в условиях реального практического здравоохранения.
Интерпретация результатов исследования
Среди социальных факторов риска было выявлено, что пациенты с КЗНК чаще проживали в семье, где в том числе было большее количество проживающих, а также ходили в церковь. Высокая социальная активность может способствовать выявлению КЗНК, поскольку друзья, коллеги и родственники могут заметить признаки КЗНК и придать им большее значение, чем сам пациент. Благодаря влиянию окружения пациент обращается к специалистам, которые диагностируют КЗНК.
Оценка психоэмоционального статуса показала, что пациенты с КЗНК были не склонны к депрессии и имели меньшие баллы по гериатрическим шкалам депрессии GDS-15 и GDS-30. Эти можно объяснить тем, что пациенты с депрессией могут реже предъявлять жалобы, в том числе на развившееся КЗНК, и, как следствие, не придавать им значение на приеме у врача [3].
При оценке функционального и физического статуса выявлено, что пациенты с КЗНК были более активны при выполнении повседневных дел (высокие значения индекса Лоутон), более мобильны (согласно тестам на равновесие (тандемное положение, тест с 5-кратным вставанием со стула и тест «Встань и иди»)) и реже применяли вспомогательные средства, что могло приводить к столкновениям и падениям, следствием чего могло явиться КЗНК. В дополнение к этому пациенты с КЗНК реже имели старческую астению по опроснику «Возраст не помеха» и были менее хрупкими согласно индексу хрупкости, который использовался для расчета в исследовании SPRINT [19][20].
Таким образом, в настоящем исследовании было показано, что в группе пациентов с КЗНК оказалось меньше хрупких пациентов и нуждающихся в посторонней помощи, так как в реальной клинической практике пациенты со старческой астенией реже обращаются к специалистам, несмотря на наличие КЗНК. С другой стороны, независимые от посторонней помощи пациенты находятся под меньшим присмотром, что может привести к травматизации и развитию КЗНК.
Полученные данные отличаются от результатов других исследований [7–11]. Так, R. Brook et. al [7] представил результаты исследования, в котором была проведена ретроспективная оценка 658 пациентов с ФП с высоким риском падений, рассчитанной по шкале Тhe Northern Нospital modified stratify falls rick assessment tool [21][22]. Общий медианный возраст пациентов составил 75 [31–96] лет, сопоставимый для всех трех ПОАК (апиксабан — 78 лет, ривароксабан — 72 года, дабигатрана этексилат — 76 лет) с равномерным распределением по полу. Одной из конечных точек исследования являлось клинически значимое кровотечение, которое набрало 3 и более балла по шкале кровотечений Международного общества по тромбозу и гемостазу (International Society of Thrombosis and Haemostasis, ISTH) от 2010 г. [23]. В результате анализа было показано, что высокий риск падений является фактором риска клинически значимого кровотечения (p = 0,032).
В настоящей работе изучали несколько параметров, определяющих риск падений: тест «Встань и иди», факт падения за прошлый год и травмы, связанные с падением, по шкале «Возраст не помеха». В результате исследования ни один из данных параметров значимо не влиял на риск развития КЗНК. Разница в результатах могла быть обусловлена дизайном исследования, разницей в возрасте исследуемых пациентов, пациенты были старше (Ме 84 [ 82; 88] года vs Ме 75 [ 31; 96] лет). А также разницей в диагностических критериях определения кровотечений: в данном исследовании использовали определение КЗНК по шкале ISTH от 2015 г., тогда как в вышеописанной статье изучались клинически значимые кровотечения по шкале ISTH от 2010 г., которые требовали медицинского вмешательства и применения транексамовой кислоты, хирургического гемостаза, трансфузии, инфузии концентратов факторов свертывания крови и десмопрессина, что соответствует определению большого кровотечения по шкале ISTH от 2015 г., которая была использована в настоящем исследовании.
В ряде работ было изучено влияние хрупкости на риск развития кровотечений. В ретроспективном исследовании T. Yamamoto et al. [8] участвовали 240 пациентов с ФП (средний возраст составил 76,1 ± 10,0 года) на фоне приема ПОАК, из них 42,9 % составляли женщины. Пациенты делились на хрупких или нехрупких по шкале Rockwood от 2005 г. (хрупкие 5–9 баллов или нехрупкие 1–4 балла) [24]. Хрупкие пациенты составляли 50 % (средний возраст составил 81,2 ± 7,8 года) от общей численности пациентов, доля женщин — 55,8 %. Конечной точкой исследования являлась кумулятивная частота большого или симптоматического кровотечения в критической области или органе в соответствии с определениями, установленными ISTH от 2005 г. [25]. Результаты исследования показали, что кумулятивная частота кровотечений была значительно выше в группе хрупких пациентов по сравнению с группой нехрупких пациентов (p < 0,001).
В исследовании M. Søgaard et al. [9] представлены результаты наблюдательного когортного исследования по безопасности применения ПОАК по сравнению с варфарином у хрупких пациентов с ФП. В данном исследовании участвовали 32 048 пациентов, ранее не принимавших антикоагулянты. Медиана возраста пациентов, принимающих стандартную дозу ПОАК, была 75 (69; 81) лет. Хрупкость пациентов определялась по шкале госпитального риска хрупкости (hospital frailty risk score — HFRS) [26], согласно которой все пациенты были разделены на «промежуточный» (5–15 баллов) или «высокий» (>15 баллов) риск хрупкости. С «промежуточным» риском хрупкости в группе стандартной дозы ПОАК было 87,7 % (14138/16 122) пациентов. С «высоким» риском хрупкости в группе стандартной дозы ПОАК было 12,3 % (1984/16 122) пациентов. У пациентов с «промежуточным» риском хрупкости большое кровотечение для стандартной дозы ПОАК развилось у 2,77 % (392/14138), относительный риск (ОР) развития большого кровотечения на стандартной дозе ПОАК составил 0,71 (95 % ДИ 0,60–0,84). В группе с «высоким» риском хрупкости большое кровотечение у пациентов на фоне стандартной дозы ПОАК развилось у 3,53 % (70/1984), а ОР развития большого кровотечения составил 0,62 (95 % ДИ 0,41–0,92). Вспомогательный анализ, включающий любые кровотечения (включая КЗНК и малые кровотечения), приведшие к обращению в больницу, показал сопоставимые результаты. Несмотря на то что в группе пациентов с «высоким» риском хрупкости частота развития большого кровотечения несколько выше, чем в группе с «промежуточным» риском хрупкости, ОР развития большого кровотечения в группе с «высоким» риском хрупкости был ниже.
В исследовании M. Candeloro et al. [10] представлены результаты, отражающие связь фенотипа хрупкости у пациентов с ФП с более высоким риском таких неблагоприятных клинических исходов, как клинически значимое кровотечение, включающее в себя большое кровотечение и КЗНК. Пациенты были классифицированы как хрупкие, предхрупкие и нехрупкие. В исследование были включены 236 пациентов (медианный возраст 78 лет, 44 % женщин), из которых у 156 (66 %) была ФП и у 80 (34 %) — венозная тромбоэмболия. Девяносто восемь (41 %) пациентов были хрупкими, 115 (49 %) — предхрупкими, а 23 (10 %) — нехрупкими. За медианное время наблюдения в 304 дня частота клинически значимых кровотечений у хрупких пациентов составила 20 %, у предхрупких — 10 %, среди нехрупких пациентов клинически значимых кровотечений не встречалось.
В исследовании D. H. Kim et al. [11] представлены результаты ретроспективного исследования о влиянии хрупкости на связь ПОАК (дабигатран, ривароксабан, апиксабан) с серьезным кровотечением у пациентов с ФП по сравнению с варфарином. Хрупкость определялась с помощью модели накопления дефицитов (индекс хрупкости на основе опроса, claims-based frailty index, CFI) [27]. Пациенты были разделены на следующие группы: нехрупкие, если CFI < 0,15, предхрупкие, если CFI 0,15–0,24, и хрупкие, если CFI ≥ 0,25. Средний возраст пациентов, принимающих как дабигатран, так и варфарин, в когорте дабигатрана был 76,4 ± 7,1 года, в когорте ривароксабана 76,8 ± 7,3 года, в когорте апиксабана 77,3 ± 7,4 года. Результаты данного исследования представлены в виде случаев на 1000 человеко-лет. Результаты исследования показали, что частота возникновения кровотечений при большом, желудочно-кишечном, внутричерепном кровотечениях возрастает с увеличением уровня хрупкости.
В отличие от вышеописанных исследований в настоящей работе хрупкость пациентов оценивалась по нескольким шкалам: шкала «Возраст не помеха», Краткая батарея тестов физического функционирования, Индекс хрупкости по шкале Rockwood от 2010 г. и по шкале SPRINT. В результате было показано, что наличие старческой астении или хрупкости, рассчитанной по данным параметрам, значимо не влияло на риск развития КЗНК, кроме того, пациенты с КЗНК были более крепкими по индексу хрупкости, рассчитанному по шкале SPRINT. Разница в результатах могла быть обусловлена также дизайном исследования, возрастом пациентов, диагностическими критериями определения кровотечений и методом измерения целевых показателей.
ЗАКЛЮЧЕНИЕ
В настоящем исследовании было показано, что социально активные, эмоционально устойчивые, мобильные и крепкие пациенты имеют более высокий риск развития КЗНК. И, наоборот, хрупкие пациенты могут реже сталкиваться с возникновением КЗНК. Также сниженная социальная активность, депрессия, нуждаемость в посторонней помощи и использование вспомогательных средств были связаны с меньшей частотой развития КЗНК. Были выявлены гериатрические факторы, которые могут являться предикторами КЗНК на фоне приема ПОАК у пациентов с ФП старше 80 лет, на основании которых была разработана прогностическая номограмма, позволяющая оценить вероятность развития КЗНК. Наибольшее влияние на прогноз оказали: количество проживающих в семье, индекс Бартел, индекс Лоутон, тест «Встань и иди» и использование вспомогательных средств. С учетом активного внедрения технологий искусственного интеллекта в клиническую практику полученные данные могут быть интегрированы в системы поддержки врачебных решений. Это позволит оценить риск развития КЗНК до его начала и отобрать пациентов, подверженных высокому риску, для дальнейшей работы в отношении профилактики этого нежелательного явления.
1. Сычев Д. А., Ткачева О. Н., Котовская Ю. В., Малая И. П. Фармакотерапия у лиц пожилого и старческого возраста. М.: Конгрессхим; 2024. 124 с.
2. Министерство здравоохранения Российской Федерации. Общероссийская общественная организация «Российская ассоциация геронтологов и гериатров». Клинические рекомендации «Старческая астения». 2024. Available: https://rgnkc.ru/images/metod_materials/%D0%9A%D0%A0613.pdf
3. Министерство здравоохранения Российской Федерации. Приказ от 29 января 2016 г. № 38н «Об утверждении порядка оказания медицинской помощи по профилю “Гериатрия”» (в ред. приказов Минздрава РФ от 20.12.2019 № 1067н, от 21.02.2020 № 114н, от 29.03.2024 № 148н)
4. Министерство здравоохранения Российской Федерации. Общероссийская общественная организация «Российская ассоциация геронтологов и гериатров». Клинические рекомендации «Старческая астения». 2024. Available: https://rgnkc.ru/images/metod_materials/%D0%9A%D0%A0613.pdf
5. Общероссийская общественная организация «Российская ассоциация геронтологов и гериатров». Карта пациента: комплексная гериатрическая оценка. Available: https://rgnkc.ru/images/metod_materials/Pacient_card.pdf
6. Министерство здравоохранения Российской Федерации. Общероссийская общественная организация «Российская ассоциация геронтологов и гериатров». Клинические рекомендации «Старческая астения». 2024. Available: https://rgnkc.ru/images/metod_materials/%D0%9A%D0%A0613.pdf
7. Министерство здравоохранения Российской Федерации. Общероссийская общественная организация «Российская ассоциация геронтологов и гериатров». Общественная организация «Российское общество психиатров». Когнитивные расстройства у лиц пожилого и старческого возраста. 2020. Available: https://rgnkc.ru/images/metod_materials/KR_KR.pdf
Список литературы
1. Аракелян М.Г., Бокерия Л.А., Васильева Е.Ю., Голицын С.П., Голухова Е.З., Горев М.В., Давтян К.В., Драпкина О.М., Кропачева Е.С., Кучинская Е.А., Лайович Л.Ю., Миронов Н.Ю., Мишина И.Е., Панченко Е.П., Ревишвили А.Ш., Рзаев Ф.Г., Татарский Б.А., Уцумуева М.Д., Шахматова О.О., Шлевков Н.Б., Шпектор А.В., Андреев Д.А., Артюхина Е.А., Барбараш О.Л., Галявич А.С., Дупляков Д.В., Зенин С.А., Лебедев Д.С., Михайлов Е.Н., Новикова Н.А., Попов С.В., Филатов А.Г., Шляхто Е.В., Шубик Ю.В. Фибрилляция и трепетание предсердий. Клинические рекомендации 2020. Российский кардиологический журнал. 2021;26(7):4594. https://doi.org/10.15829/150-4071-2021-4594
2. Van Gelder IC, Rienstra M, Bunting KV, Casado-Arroyo R, Caso V, Crijns HJGM, De Potter TJR, Dwight J, Guasti L, Hanke T, Jaarsma T, Lettino M, Løchen ML, Lumbers RT, Maesen B, Mølgaard I, Rosano GMC, Sanders P, Schnabel RB, Suwalski P, Svennberg E, Tamargo J, Tica O, Traykov V, Tzeis S, Kotecha D; ESC Scientific Document Group. 2024 ESC Guidelines for the management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J. 2024;45(36):3314–3414. https://doi.org/10.1093/eurheartj/ehae176
3. Ткачева О.Н., Воробьёва Н.М., Котовская Ю.В., Рунихина Н.К., Стражеско И.Д., Виллевальде С.В., Драпкина О.М., Комаров А.Л., Орлова Я.А., Панченко Е.П., Погосова Н.В., Фролова Е.В., Явелов И.С. Антитромботическая терапия в пожилом и старческом возрасте: согласованное мнение экспертов Российской ассоциации геронтологов и гериатров и Национального общества профилактической кардиологии. Кардиоваскулярная терапия и профилактика. 2021;20(3):2847. https://doi.org/10.15829/1728-8800-2021-2847
4. Загидуллин Н.Ш., Давтян П.А. Особенности антикоагуляции при сочетании фибрилляции предсердий и хронической болезни почек. Российский кардиологический журнал. 2021;26(3S):4676. https://doi.org/10.15829/1560-4071-2021-4676
5. Филонова У.Д., Карнакова П.К., Карнакова К.К., Попова М.О., Попова А.А., Арчакова О.А., Комаров Т.Н., Шохин И.Е. Разработка и валидация методики количественного определения апиксабана в плазме крови с помощью метода ВЭЖХ-МС/МС. Разработка и регистрация лекарственных средств. 2024;13(1):224–240. https://doi.org/10.33380/2305-2066-2024-13-1-1684
6. Hindricks G, Potpara T, Dagres N, Arbelo Е, Bax JJ, Blomstrӧm-Lundqvist С, Boriani G, Castella M, Dan G, Dilaveris PE, Fauchier L, Filippatos G, Kalman JM, La Meir M, Lane DA, Lebeau J, Lettino M, Lip GY, Pinto FJ, Neil Thomas G, Valgimigli M, Van Gelder IC, Van Putte BP, Watkins CL. Рекомендации ESC 2020 по диагностике и лечению пациентов с фибрилляцией предсердий, разработанные совместно с европейской ассоциацией кардиоторакальной хирургии (EACTS). Российский кардиологический журнал. 2021;26(9):4701. https://doi.org/10.15829/1560-4071-2021-4701
7. Hindricks G, Potpara T, Dagres N, Arbelo E, Bax JJ, Blomstrӧm-Lundqvist C, Boriani G, Castella M, Dan G, Dilaveris PE, Fauchier L, Filippatos G, Kalman JM, La Meir M, Lane DA, Lebeau J, Lettino M, Lip GY, Pinto FJ, Neil Thomas G, Valgimigli M, Van Gelder IC, Van Putte BP, Watkins CL. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS). Russian Journal of Cardiology. 2021;26(9):4701 (In Russ.). https://doi.org/10.15829/1560-4071-2021-4701
8. Brook R, Aswapanyawongse O, Tacey M, Kitipornchai T, Ho P, Lim HY. Real-world direct oral anticoagulant experience in atrial fibrillation: falls risk and low dose anticoagulation are predictive of both bleeding and stroke risk. Intern Med J. 2020;50(11):1359–1366. h ttps://doi.org/10.1111/imj.14640
9. Yamamoto T, Yamashita K, Miyamae K, Koyama Y, Izumimoto M, Kamimura Y, Hayakawa S, Mori K, Yamada T, Tomita Y, Murohara T. The influence of frailty under direct oral anticoagulant use in patients with atrial fibrillation. Heart Asia. 2019;11(2):e011212. https://doi.org/10.1136/heartasia-2019-011212
10. Søgaard M, Ording AG, Skjøth F, Larsen TB, Nielsen PB. Effectiveness and safety of direct oral anticoagulation vs. warfarin in frail patients with atrial fibrillation. Eur Heart J Cardiovasc Pharmacother. 2024;10(2):137–146. https://doi.org/10.1093/ehjcvp/pvad091
11. Candeloro M, Di Nisio M, Potere N, Di Pizio L, Secinaro E, De Flaviis C, Federici C, Guglielmi MD, Pardi S, Schulman S, Porreca E. Frailty phenotype as a predictor of bleeding and mortality in ambulatory patients receiving direct oral anticoagulants. J Am Geriatr Soc. 2022;70(12):3503–3512. https://doi.org/10.1111/jgs.18001
12. Kim DH, Pawar A, Gagne JJ, Bessette LG, Lee H, Glynn RJ, Schneeweiss S. Frailty and Clinical Outcomes of Direct Oral Anticoagulants Versus Warfarin in Older Adults With Atrial Fibrillation: A Cohort Study. Ann Intern Med. 2021;174(9):1214–1223. https://doi.org/10.7326/M20-7141
13. Сычев Д.А., Черняева М.С., Рожкова М.А., Моисеева Е.А., Погодина А.А., Байзель Ю.С., Егорова Л.А., Масленникова О.М., Ломакин Н.В. Безопасность прямых оральных антикоагулянтов в лечении фибрилляции предсердий у гериатрических пациентов: фокус на клинически значимые небольшие кровотечения. Фарматека. 2024;31(4):8–23. https://doi.org/10.18565/pharmateca.2024.4.8-23
14. Sychev DA, Cherniaeva MS, Rozhkova MA, Moiseeva A., Pogodina AA, Bayzel YuS, Egorova LA, Maslennikova OM, Lomakin NV. Safety of direct oral anticoagulants in the treatment of atrial fibrillation in geriatric patients: focus on clinically relevant non-major bleeding. Farmateka. 2024;31(4):8–23 (In Russ.). https://doi.org/10.18565/pharmateca.2024.4.8-23
15. Черняева М.С., Рожкова М.А., Кондрахин А.П., Погодина А.А., Махмудов И.Н., Алисултанов Д.А., Егорова Л.А., Масленникова О.М., Ломакин Н.В., Сычев Д.А. Частота встречаемости и структура клинически значимых небольших кровотечений на фоне приема прямых оральных антикоагулянтов у пациентов 80 лет и старше с неклапанной фибрилляцией предсердий. Эффективная фармакотерапия. 2024;20(26):28–38. https://doi.org/10.33978/2307-3586-2024-20-26-28-38
16. Bonanad C, Formiga F, Anguita M, Petidier R, Gullón A. Oral Anticoagulant Use and Appropriateness in Elderly Patients with Atrial Fibrillation in Complex Clinical Conditions: ACONVENIENCE Study. J Clin Med. 2022;11(24):7423. https://doi.org/10.3390/jcm11247423
17. Mailhot T, McManus DD, Waring ME, Lessard D, Goldberg R, Bamgbade BA, Saczynski JS. Frailty, Cognitive Impairment, and Anticoagulation Among Older Adults with Nonvalvular Atrial Fibrillation. J Am Geriatr Soc. 2020;68(12):2778–2786. https://doi.org/10.1111/jgs.16756
18. Mahoney FI, Barthel DW. Functional evaluation: the Barthel Index. Md State Med J. 1965;14:61–65.
19. Lawton MP, Brody EM. Assessment of older people: self-maintaining and instrumental activities of daily living. Gerontologist. 1969;9(3):179– 186.
20. Kaiser MJ, Bauer JM, Ramsch C, Uter W, Guigoz Y, Cederholm T, Thomas DR, Anthony P, Charlton KE, Maggio M, Tsai AC, Grathwohl D, Vellas B, Sieber CC; MNA-International Group. Validation of the Mini Nutritional Assessment short-form (MNA-SF): a practical tool for identification of nutritional status. J Nutr Health Aging. 2009;13(9):782–788. https://doi.org/10.1007/s12603-009-0214-7
21. Rockwood K, Rockwood MR, Mitnitski A. Physiological redundancy in older adults in relation to the change with age in the slope of a frailty index. J Am Geriatr Soc. 2010;58(2):318–323. https://doi.org/10.1111/j.1532-5415.2009.02667.x
22. Pajewski NM, Williamson JD, Applegate WB, et al. Characterizing Frailty Status in the Systolic Blood Pressure Intervention Trial. J Gerontol A Biol Sci Med Sci. 2016;71(5):649–655. https://doi.org/10.1093/gerona/glv228
23. Черняева М.С., Алферова П.А., Павлова А.О., Трифонов М.И., Егорова Л.А., Масленникова О.М., Ломакин Н.В., Сычев Д.А. Безопасность прямых оральных антикоагулянтов у пациентов с фибрилляцией предсердий в возрасте 80 лет и старше: клинические факторы риска. Российский медицинский журнал. 2024;30(5):464– 474. https://doi.org/10.17816/medjrf635877
24. Barker A, Kamar J, Graco M, Lawlor V, Hill K. Adding value to the STRATIFY falls risk assessment in acute hospitals. J Adv Nurs. 2011;67(2):450–457. https://doi.org/10.1111/j.1365-2648.2010.05503.x
25. Rodeghiero F, Tosetto A, Abshire T, Arnold DM, Coller B, James P, Neunert C, Lillicrap D; ISTH/SSC joint VWF and Perinatal/Pediatric Hemostasis Subcommittees Working Group. ISTH/SSC bleeding assessment tool: a standardized questionnaire and a proposal for a new bleeding score for inherited bleeding disorders.. J Thromb Haemost. 2010;8(9):2063–2065. https://doi.org/10.1111/j.1538-7836.2010.03975.x
26. Rockwood K, Song X, MacKnight C, Bergman H, Hogan DB, McDowell I, Mitnitski A. A global clinical measure of fitness and frailty in elderly people. CMAJ. 2005;173(5):489–495. https://doi.org/10.1503/cmaj.050051
27. Schulman S, Kearon C; Subcommittee on Control of Anticoagulation of the Scientific and Standardization Committee of the International Society on Thrombosis and Haemostasis. Definition of major bleeding in clinical investigations of antihemostatic medicinal products in nonsurgical patients. J Thromb Haemost. 2005;3(4):692–694. https://doi.org/10.1111/j.1538-7836.2005.01204.x
28. Gilbert T, Neuburger J, Kraindler J, Keeble E, Smith P, Ariti C, Arora S, Street A, Parker S, Roberts HC, Bardsley M, Conroy S. Development and validation of a Hospital Frailty Risk Score focusing on older people in acute care settings using electronic hospital records: an observational study. Lancet. 2018;391(10132):1775–1782. https://doi.org/10.1016/S0140-6736(18)30668-8
29. Kim DH, Schneeweiss S, Glynn RJ, Lipsitz LA, Rockwood K, Avorn J. Measuring Frailty in Medicare Data: Development and Validation of a Claims-Based Frailty Index. J Gerontol A Biol Sci Med Sci. 2018;73(7):980–987. https://doi.org/10.1093/gerona/glx229
Об авторах
М. С. ЧерняеваРоссия
Черняева Марина Сергеевна — кандидат медицинских наук, доцент, доцент кафедры клинической фармакологии и терапии имени академика Б.Е. Вотчала; доцент кафедры внутренних болезней и профилактической медицины; заведующий гериатрическим отделением № 5
ул. Баррикадная, д. 2/1, стр. 1, г. Москва, 125993
ул. Маршала Тимошенко, д. 19, стр. 1а, г. Москва, 121359
пр-т Волгоградский, д. 168, г. Москва, 109472
А. О. Павлова
Россия
Павлова Анна Олеговна — лаборант кафедры внутренних болезней и профилактической медицины
ул. Маршала Тимошенко, д. 19, стр. 1а, г. Москва, 121359
П. А. Алферова
Россия
Алферова Полина Алексеевна — лаборант кафедры клинической фармакологии и терапии имени академика Б.Е. Вотчала
ул. Баррикадная, д. 2/1, стр. 1, г. Москва, 125993
М. А. Рожкова
Россия
Рожкова Мария Александровна — врач-терапевт
б-р Ореховый, д. 28, г. Москва, 115682
М. И. Трифонов
Россия
Трифонов Михаил Игоревич — врач-гериатр, заведующий отделением терапии
пер. 3-й Монетчиковский, д. 16, стр. 1,
Т. В. Никеева
Россия
Никеева Татьяна Васильевна — врач-терапевт консультативного отделения
пр-т Волгоградский, д. 168, г. Москва, 109472
Л. А. Егорова
Россия
Егорова Лариса Александровна — доктор медицинских наук, профессор, профессор кафедры внутренних болезней и профилактической медицины
ул. Маршала Тимошенко, д. 19, стр. 1а, г. Москва, 121359
О. М. Масленникова
Россия
Масленикова Ольга Михайловна — доктор медицинских наук, доцент, заведующий кафедрой внутренних болезней и профилактической медицины
ул. Маршала Тимошенко, д. 19, стр. 1а, г. Москва, 121359
Н. В. Ломакин
Россия
Ломакин Никита Валерьевич — доктор медицинских наук, доцент, заведующий кафедрой кардиологии; заведующий кардиологическим отделением № 2
ул. Баррикадная, д. 2/1, стр. 1, г. Москва, 125993
ул. Маршала Тимошенко, 15, г. Москва, 121359
Д. А. Сычев
Россия
Сычев Дмитрий Алексеевич — доктор медицинских наук, профессор, профессор Российской академии наук, академик
Российской академии наук, заведующий кафедрой клинической фармакологии и терапии имени академика Б.Е. Вотчала
ул. Баррикадная, д. 2/1, стр. 1, г. Москва, 125993
Дополнительные файлы
Рецензия
Для цитирования:
Черняева М.С., Павлова А.О., Алферова П.А., Рожкова М.А., Трифонов М.И., Никеева Т.В., Егорова Л.А., Масленникова О.М., Ломакин Н.В., Сычев Д.А. Гериатрические факторы риска безопасности прямых оральных антикоагулянтов у пациентов с фибрилляцией предсердий 80 лет и старше: обсервационное когортное проспективное исследование. Кубанский научный медицинский вестник. 2025;32(3):15-35. https://doi.org/10.25207/1608-6228-2025-32-3-15-35
For citation:
Cherniaeva M.S., Pavlova A.O., Alferova P.A., Rozhkova M.A., Trifonov M.I., Nikeeva T.V., Egorova L.A., Maslennikova O.M., Lomakin N.V., Sychev D.A. Geriatric factors affecting the safety of direct oral anticoagulants in atrial fibrillation patients aged 80 years and older: An observational prospective cohort study. Kuban Scientific Medical Bulletin. 2025;32(3):15-35. https://doi.org/10.25207/1608-6228-2025-32-3-15-35
JATS XML








































