Перейти к:
Значение трансректального ультразвукового исследования с контрастным усилением в дифференциальной диагностике очаговой патологии предстательной железы: одноцентровое ретроспективное сравнительное исследование
https://doi.org/10.25207/1608-6228-2023-30-1-58-68
Аннотация
Введение. Рак предстательной железы — часто диагностируемое злокачественное заболевание у мужчин. На сегодня наиболее распространенным методом визуализации железы является трансректальное ультразвуковое исследование. Традиционно используется комбинация серошкального и допплерографических режимов. В связи с недостаточной информативностью стандартных режимов трансректального ультразвукового исследования предстательной железы многие авторы рекомендуют применение методики с контрастным усилением. Ультразвуковое исследование с контрастным усилением позволяет проводить количественную оценку, что, в свою очередь, повышает объективность получаемых результатов.
Цель исследования: изучить возможности трансректального ультразвукового исследования с контрастным усилением в дифференциальной диагностике очаговой патологии предстательной железы.
Методы. Проведено одноцентровое ретроспективное сравнительное исследование результатов трансректального ультразвукового исследования предстательной железы с контрастным усилением 66 пациентов, выполненного в государственном автономном учреждении здравоохранения «Республиканский клинический онкологический диспансер Министерства здравоохранения Республики Татарстан имени профессора М. З. Сигала». Условием включения в исследование являлось наличие очаговой патологии периферической зоны предстательной железы. Медиана возраста пациентов составила 67 лет. Анализировались следующие количественные параметры перфузии: time to peak, peak intensity, descending time, area under the curve и дополнительно рассчитываемый индекс для каждого из указанных параметров. Полученные кривые накопления также анализировали путем измерения углов накопления (β) и вымывания (α). Данные, полученные по результатам исследований, анализировали с использованием программы SPSS (версия 13.0) (IBM SPSS Statistics, США).
Результаты. Лучшую информативность в диагностике рака предстательной железы показал комплекс «угол ß ≥ 69,5° + угол α ≤ 69,5°» с чувствительностью 92,7%, специфичностью 80,0%. Чувствительность и специфичность полученных пороговых значений «угол накопления ß ≥ 69,5°» составили 73,2 и 60,0% соответственно, «угол вымывания α ≤ 69,5°» — 63,4 и 56,0% соответственно. По результатам анализа количественных параметров перфузии лучшая информативность в диагностике рака предстательной железы у теста «peak intensity ≥ 34,1 дБ» с чувствительностью 75,6%, специфичностью 84,0%.
Заключение. Количественный анализ трансректального ультразвукового исследования предстательной железы с контрастным усилением позволяет объективизировать исследование, а использование пороговых значений — повысить информативность в дифференциальной диагностике очаговых образований предстательной железы.
Ключевые слова
Для цитирования:
Хасанов М.З., Тухбатуллин М.Г., Насруллаев М.Н. Значение трансректального ультразвукового исследования с контрастным усилением в дифференциальной диагностике очаговой патологии предстательной железы: одноцентровое ретроспективное сравнительное исследование. Кубанский научный медицинский вестник. 2023;30(1):58-68. https://doi.org/10.25207/1608-6228-2023-30-1-58-68
For citation:
Khasanov M.Z., Tukhbatullin M.G., Nasrullaev M.N. Contrast-Enhanced Transrectal Ultrasound for Differential Diagnosis of Focal Pathology of Prostate: Single-Center Retrospective Comparative Study. Kuban Scientific Medical Bulletin. 2023;30(1):58-68. (In Russ.) https://doi.org/10.25207/1608-6228-2023-30-1-58-68
ВВЕДЕНИЕ
В большинстве стран мира рак предстательной железы (РПЖ) — распространенное злокачественное заболевание [1][2]. По данным мировых статистических данных и нашей страны, отмечается устойчивое повышение заболеваемости РПЖ1 [3]. Трансректальное ультразвуковое исследование (ТРУЗИ) предстательной железы (ПЖ) — на сегодняшний день наиболее распространенный способ визуализации в силу информативности, доступности и экономической эффективности [4][5]. Стандартно используется комбинация серошкального и допплерографических режимов [6]. Однако их данных недостаточно при постановке диагноза [7–11]. Так, информативность энергетического допплерографического картирования (ЭДК) как более чувствительной методики в сравнении с цветовым допплеровским картированием (ЦДК) ограничена в оценке микроциркуляторного русла. Применение ультразвукового исследования с контрастным усилением (КУУЗИ) направлено на преодоление данного ограничения [12–14]. Субъективная оценка качественных признаков УЗИ с контрастным усилением предстательной железы считается ограничением методики [15]. Использование количественных параметров контрастного исследования направлено на повышение объективности получаемых данных [16]. Количественная оценка накопления контрастного вещества осуществляется путем построения и анализа кривых накопления [17][18].
Цель исследования — оценка информативности трансректального ультразвукового исследования с контрастным усилением в диагностике очаговой патологии предстательной железы.
МЕТОДЫ
Дизайн исследования
Одноцентровое ретроспективное сравнительное исследование 66 пациентов c сформированием двух групп: 41 пациент с раком предстательной железы и 25 пациентов с доброкачественными очаговыми изменениями предстательной железы.
Условия проведения исследования
Исследование проводилось в государственном автономном учреждении здравоохранения «Республиканский клинический онкологический диспансер Министерства здравоохранения Республики Татарстан имени профессора М. З. Сигала» (ГАУЗ «РКОД МЗ РТ им. проф. М. З. Сигала») в период с января 2019 по октябрь 2020 г.
Критерии соответствия
Критерии включения
Наличие очаговых изменений периферической зоны предстательной железы.
Критерии невключения
Отсутствие очаговых изменений периферической зоны предстательной железы, генерализованные опухолевые процессы, верифицированный рак предстательной железы, повышенная чувствительность к компонентам контрастного препарата «Серы гексафторид», клинически нестабильная ишемическая болезнь сердца, острая сердечная недостаточность, острый коронарный синдром, аритмия, тяжелая форма легочной гипертензии, респираторный дистресс-синдром, отказ пациента.
Описание критериев соответствия (диагностические критерии)
Основными диагностическими критериями проводимого исследования у пациентов явились количественные параметры трансректального ультразвукового исследования с контрастным усилением в дифференциальной диагностике очаговой патологии предстательной железы.
Подбор участников в группы
66 пациентов с подозрением на рак предстательной железы были включены в исследование. Наличие очагового образования периферической зоны предстательной железы, выявленное по данным серошкального режима УЗИ, явилось критерием включения в исследование. Референтным методом в исследовании была трансректальная систематическая биопсия железы из 12 точек под ультразвуковым контролем, дополненная при необходимости прицельными заборами. В заключении гистологического исследования отмечалось наличие или отсутствие злокачественного заболевания с оценкой дифференцировки опухолевого процесса по шкале Глисона. По результатам были сформированы две группы.
Целевые показатели исследования
Основной показатель исследования
Основной конечной стадией исследования являлось сопоставление количественных параметров ТРУЗИ с контрастным усилением и результатами гистологического исследования с последующей оценкой информативности анализируемых параметров в дифференциальной диагностике очаговой патологии предстательной железы.
Дополнительные показатели исследования
Дизайном исследования не предусмотрены дополнительные показатели исследования.
Методы измерения целевых показателей
Медиана возраста пациентов, включенных в исследование, составила 67 лет. Всем пациентам выполнено пальцевое ректальное исследование (ПРИ), анализ уровня простат-специфического антигена (ПСА) в сыворотке крови. Исследования в контрастном режиме выполняли на ультразвуковом сканере Resona 7 (Mindrаy, Китай) с использованием внутриполостного микроконвексного датчика с частотой от 4 до 6 МГц.
Применяли ультразвуковой контрастный препарат (УКП) «Серы гексафторид» (Соновью, Bracco Swiss, SA, Швейцария) в объеме 2,4 мл на одно исследование. Препарат вводили внутривенно болюсно по стандартной схеме.
При контрастном усилении предстательная железа исследовалась в поперечной плоскости при наилучшей визуализации очагового образования. После внутривенного введения контрастного препарата сканирование предстательной железы проводили в течение 3 минут непрерывно.
Исследования контрастных исследований сохраняли в цифровом формате. В дальнейшем проводили количественный анализ путем построения кривых накопления. Областями интереса для построения кривых являлись очаговое образование периферической зоны, интактный симметричный участок периферической зоны, переходная зона. Указанные зоны интереса были выделены окнами запроса диаметром 5 мм.
В расчет были включены следующие количественные показатели: time to peak (ТТР, сек.) — время до момента максимальной интенсивности накопления контрастного препарата в зоне интереса; peak intensity (PI, дБ) — максимальная интенсивность контрастирования; descending time (DT/2, cек.) — время, за которое интенсивность контрастирования уменьшается на 50% от максимального значения; area under the curve (AUC, дБ/сек.) — площадь под кривой.
Для данных количественных показателей дополнительно рассчитывали индекс из следующей формулы:
Индекс = параметр очагового образования периферической зоны (ТТР, PI, DT/2, AUC)/аналогичный параметр интактного участка периферической зоны.
Формы кривых накопления анализировали с помощью измерения углов накопления и вымывания. При измерении угла накопления (ß) центр транспортира устанавливали на точку начала подъема кривой, одна сторона угла представляла собой линию параллельную оси абсцисс, другая сторона угла — линию, соединяющую точку начала подъема кривой с точкой PI. При измерении угла вымывания (α) центр транспортира устанавливали на точку PI, одна сторона угла представляла собой линию, образующую прямой угол с осью абсцисс, другая сторона угла — линию, соединяющую точку PI и точку DT/2 на кривой (рис. 1). Данные способы были запатентованы2 3.
Переменные (предикторы, конфаундеры, модификаторы эффекта)
Для коррекции результатов исследования путем стратификации до начала исследования был использован показатель наличия очагового образования периферической зоны предстательной железы.
Статистические процедуры
Принципы расчета размера выборки
Предварительный расчет размера выборки не проводился.
Статистические методы
Данные, полученные по результатам исследований, анализировали с использованием программы SPSS (версия 13.0) (IBM SPSS Statistics, США). Оценка информативности анализировалась путем расчета чувствительности, специфичности, точности, предсказательности положительного и отрицательного значений по общеустановленным формулам. Непараметрический критерий Манна — Уитни, критерий χ2, критерий Фишера использовали для оценки достоверности различий переменных. Статистически значимыми различия считали при р ≤ 0,05. Качество бинарной классификации оценивали с помощью ROC-анализа.
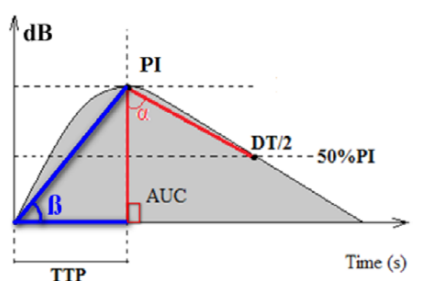
Рис. 1. Схема кривой накопления.
Примечание: рисунок составлен авторами.
Fig. 1. Diagram of enhancement curve.
Note: compiled by the authors.
РЕЗУЛЬТАТЫ
Формирование выборки исследования
На рисунке 2 представлены процесс формирования выборки исследования и его дизайн.
Характеристики выборки (групп) исследования
По результатам гистологического исследования у 41 пациента были диагностированы злокачественные очаги, которые составили группу РПЖ. Группу сравнения составили 25 пациентов с доброкачественными очаговыми изменениями. Характеристика пациентов по клинико-лабораторным данным представлена в таблице 1.
Основной результат исследования
Для выполнения цели исследования всем пациентам были выполнены ТРУЗИ ПЖ с контрастным усилением с последующим количественным анализом (рис. 3).
Полученные количественные параметры представлены в таблице 2.
По данным статистического анализа было выявлено статистически значимое различие для всех количественных показателей кривой накопления (PI, TTP, DT/2, AUC, углы вымывания и накопления) с очага периферической зоны предстательной железы между анализируемыми группами. В группе РПЖ было отмечено статистически значимое различие показателей PI, TTP, углам вымывания и накопления между интактной периферической зоной и очагом. В группе сравнения между интактной периферической зоной и очагом было отмечено статистически значимое только по показателю угла накопления.
Проведенный статистический анализ показал значимое различие между анализируемыми группами для индексов PI, TTP, DT/2.
Для показателей очага периферической зоны выполнено сравнение между группами с помощью ROC-анализа. Полученные результаты информативности пороговых значений в диагностике РПЖ представлены на рисунках 4–9 и в таблице 3.
Дополнительные результаты исследования
Дополнительных результатов исследования не получено.
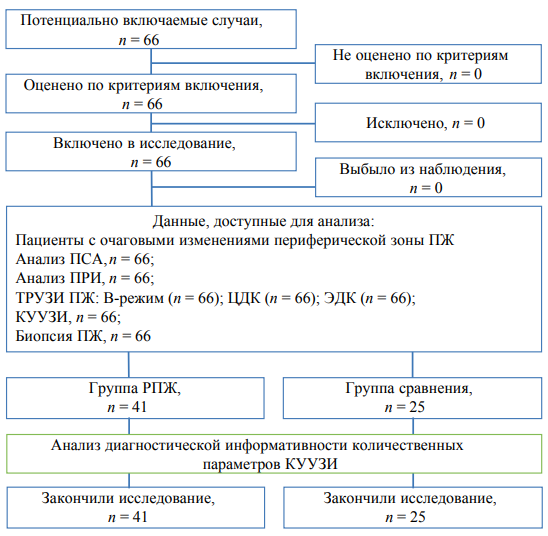
Рис. 2. Блок-схема дизайна исследования.
Примечание: блок-схема согласно рекомендациям STROBE заполнена авторами; ПЖ — предстательная железа, ПСА — простат-специфический антиген, ПРИ — пальцевое ректальное исследование, ТРУЗИ — трансректальное ультразвуковое исследование, ЦДК — цветовое допплеровское картирование, ЭДК — энергетическое допплерографическое картирование, КУУЗИ — ультразвуковое исследование с контрастным усилением, РПЖ — рак предстательной железы.
Fig. 2. Schematic diagram of the research design.
Note: A flow-chart diagram completed by the authors according to the STROBE recommendations; ПЖ — prostate gland, ПСА — prostate-specific antigen, ПРИ — digital rectal examination, ТРУЗИ — transrectal ultrasound, ЦДК — color Doppler mapping, ЭДК — power Doppler mapping, КУУЗИ — contrast-enhanced ultrasound, РПЖ — prostate cancer.
Таблица 1. Клинико-лабораторные данные пациентов
Тable 1. Clinical laboratory findings of patients
Показатель | РПЖ (n = 41) | Группа сравнения (n = 25) | р-уровень |
Возраст | 68,0 60,5–72,5 50,0–81,0 | 66,5 58,0–70,0 46,0–82,0 |
>0,05 |
ПСА, нг/мл | 9,8 7,0–17,9 0,78–89,00 | 6,5 4,9–8,8 1,26–14,53 |
˂0,01 |
Объем ПЖ, мл | 38,0 33,0–47,0 21,0–80,0 | 45,5 35,0–65,0 21,0–140,0 | >0,05 |
Размер очага, мм | 14,0 10,0–22,0 5,0–50,0 | 9,0 7,0–11,0 4,0–17,0 | ˂0,01 |
Примечание: таблица составлена авторами; в ячейках таблицы первая строка — значение медианы, вторая — 25-й и 75-й процентиль, третья — минимальные и максимальные значения; ПСА — простат-специфический антиген; ПЖ — предстательная железа.
Note: compiled by the authors; the first row indicates the value of the median, the second — 25th and 75th percentile, the third — minimum and maximum values; ПСА — prostate-specific antigen, ПЖ — prostate gland.
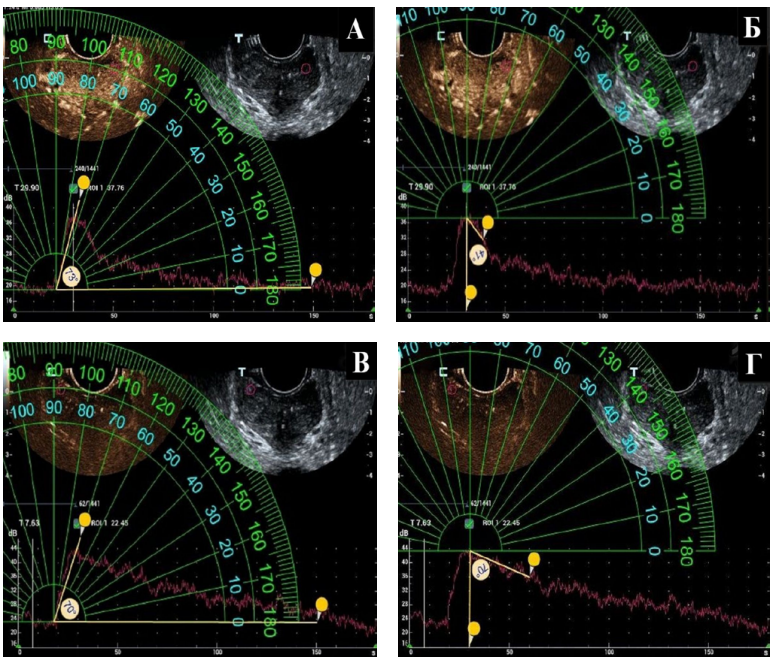
Рис. 3. Трансректальное ультразвуковое исследование с контрастным усилением. Рак предстательной железы. А — угол накопления очага, Б — угол вымывания очага, В — угол накопления интактной периферической зоны, Г — угол вымывания интактной периферической зоны.
Примечание: фотографии сделаны авторами.
Fig. 3. Contrast-enhanced transrectal ultrasound. Prostate cancer. A — enhancement angle of focal formation, Б — washout angle of focal formation, В — enhancement angle of the intact peripheral zone, Г — washout angle of the intact peripheral zone.
Note: photos taken by the authors.
Таблица 2. Количественные показатели ТРУЗИ ПЖ с контрастным усилением
Тable 2. Quantitative indicators of contrast-enhanced transrectal ultrasound of prostate gland
Показатель | Интактная периферическая зона | Очаг периферической зоны | ||
Группа сравнения (n = 25) | РПЖ (n = 41) | Группа сравнения (n = 25) | РПЖ (n = 41) | |
PI (дБ) | 31,0 29,0–33,0 26,9–35,0 | 32,0 30,0–34,0 25,0–39,0 | 32,0 31,0–33,5 25,0–39,6 | 35,7 34,2–37,0 28,3–43,0 |
TTP (сек.) | 15,3 12,5–19,0 10,0–32,0 | 15,6 14,5–21,9 8,0–52,0 | 16,0 14,0–18,0 11,3–24,0 | 13,0 12,1–16,5 10,0–23,0 |
DT/2 (сек.) | 63,0 59,0–72,9 47,0–131,6 | 70,0 57,8–78,0 43,0–102,0 | 72,8 65,3–75,0 59,0–95,0 | 70,0 54,6–72,4 37,8–79,0 |
AUC (дБ/сек.) | 4190,0 3764,0–4351,0 3490,0–4542,0 | 4235,0 4092,6–4482,0 3629,0–5288,0 | 3895,8 3772,5–4140,0 3044,0–4566,5 | 4173,3 3970,0–4460,0 3296,4–6572,0 |
Угол вымывания (α) | 75,0 66,0–78,0 37,0–87,0 | 74,0 65,0–79,0 56,0–88,0 | 70,0 64,5–75,5 54,0–83,0 | 68,0 47,0–71,0 40,0–78,0 |
Угол накопления (ß) | 63,0 47,0–67,0 20,0–76,0 | 61,0 53,0–69,0 31,0–76,0 | 68,0 62,5–73,0 54,0–79,0 | 74,0 68,0–77,0 48,0–81,0 |
Примечание: таблица составлена авторами; данные представлены как в таблице 1; РПЖ — рак предстательной железы; PI — peak intensity, максимальная интенсивность контрастирования; ТТР — time to peak, время до момента максимальной интенсивности накопления контрастного препарата в зоне интереса; DT/2 — descending time, время, за которое интенсивность контрастирования уменьшается на 50% от максимального значения; AUC — area under the curve, площадь под кривой.
Note: compiled by the authors; data are presented as in Table 1; РПЖ — prostate cancer; PI — peak intensity, maximum contrast intensity; TTP — time to peak, time to maximum contrast enhancement in the area of interest; DT/2 — descending time, time for which contrast intensity decreases by 50% of maximum; AUC — area under the curve.
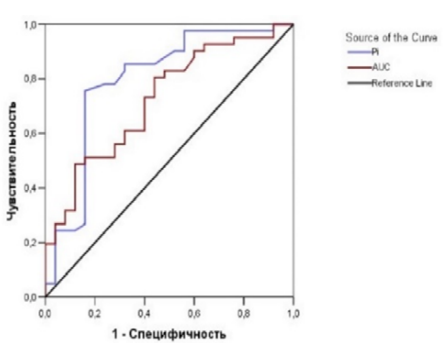
Рис. 4. ROC-кривая прогностических возможностей PI и AUC.
Примечание: рисунок составлен авторами.
Fig. 4. ROC is a curve of prognostic capabilities of PI and AUC.
Note: compiled by the authors.
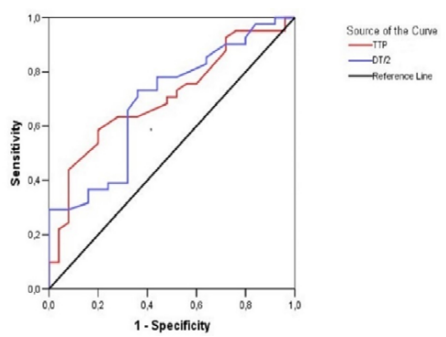
Рис. 5. ROC-кривая прогностических возможностей TTP и DT/2.
Примечание: рисунок составлен авторами.
Fig. 5. ROC is the curve of prognostic capabilities of TTP and DT/2.
Note: compiled by the authors.
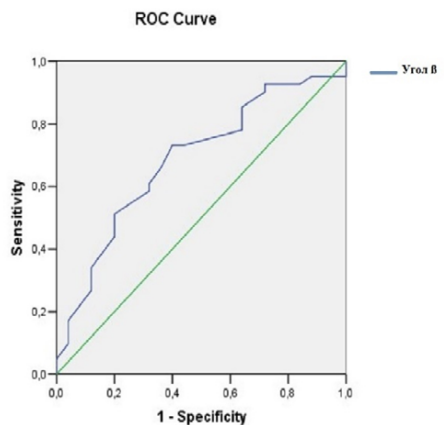
Рис. 6. ROC-кривая прогностических возможностей угла накопления (ß).
Примечание: рисунок составлен авторами.
Fig. 6. ROC is the curve of prognostic capabilities of the enhancement angle (ß).
Note: compiled by the authors.
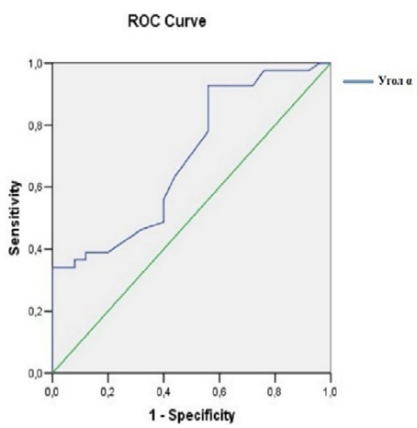
Рис. 7. ROC-кривая прогностических возможностей угла вымывания (α).
Примечание: рисунок составлен авторами.
Fig. 7. ROC is the curve of prognostic capabilities of the washout angle (α).
Note: compiled by the authors.
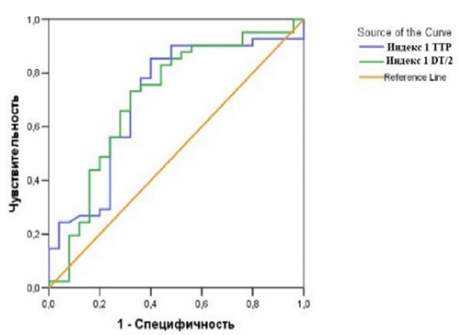
Рис. 8. ROC-кривая прогностических возможностей индексов TTP и DT/2.
Примечание: рисунок составлен авторами.
Fig. 8. ROC is the curve of prognostic capabilities of TTP and DT/2 indices.
Note: compiled by the authors.
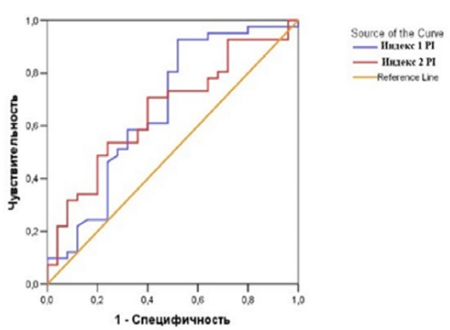
Рис. 9. ROC-кривая прогностической возможности индекса PI.
Примечание: рисунок составлен авторами.
Fig. 9. ROC is the curve of prognostic capabilities of PI index.
Note: compiled by the authors.
Таблица 3. Информативность количественных параметров ТРУЗИ ПЖ с контрастным усилением в диагностике рака предстательной железы
Table 3. Informative value of quantitative parameters of contrast-enhanced transrectal ultrasound of the prostate in diagnosis of prostate cancer
Пороговые значения | Ч., % | С., % | Т., % | ПЦПР, % | ПЦОР, % |
PI ≥ 34,1 дБ | 75,6 | 84,0 | 80,3 | 88,9 | 70,0 |
TTP ≤ 13,8 сек. | 58,5 | 80,0 | 66,7 | 82,8 | 54,1 |
DT/2 ≤ 71,7 сек. | 73,2 | 64,0 | 69,7 | 76,9 | 59,3 |
AUC ≥ 3946,0 дБ/сек. | 80,5 | 56,0 | 71,2 | 75,0 | 63,6 |
Индекс PI ≥ 1,004 | 92,7 | 48,0 | 75,8 | 74,5 | 80,0 |
Индекс TTP ≤ 0,955 | 85,4 | 60,0 | 75,8 | 77,8 | 71,4 |
Индекс DT/2 ≤ 0,993 | 73,2 | 68,0 | 71,2 | 79,0 | 60,7 |
Угол ß ≥ 69,5° | 73,2 | 60,0 | 68,2 | 75,0 | 57,7 |
Угол α ≤ 69,5° | 63,4 | 56,0 | 60,6 | 70,3 | 48,3 |
Угол ß ≥ 69,5° + угол α ≤ 69,5° | 92,7 | 80,0 | 87,9 | 88,4 | 87,0 |
Примечание: таблица составлена авторами; Ч — чувствительность, С — специфичность, Т — точность, ПЦПЗ — предсказательная ценность положительного результата, ПЦОР — предсказательная ценность отрицательного результата; PI — peak intensity, максимальная интенсивность контрастирования; ТТР — time to peak, время до момента максимальной интенсивности накопления контрастного препарата в зоне интереса; DT/2 — descending time, время, за которое интенсивность контрастирования уменьшается на 50% от максимального значения; AUC — area under the curve, площадь под кривой.
Note: compiled by the authors; Ч — sensitivity, С — specificity, T — accuracy, ПЦПЗ — positive predictive value, ПЦОР — negative predictive value, PI — peak intensity, maximum contrast intensity, TTP — time to peak, time to maximum contrast enhancement in the area of interest, DT/2 — descending time, time for which contrast intensity decreases by 50% of maximum, AUC — area under the curve.
ОБСУЖДЕНИЕ
Резюме основного результата исследования
Количественный анализ трансректального ультразвукового исследования предстательной железы с контрастным усилением позволяет объективизировать исследование, а использование пороговых значений — повысить информативность в дифференциальной диагностике очаговых образований предстательной железы.
Ограничения исследования
В связи с небольшим объемом выборки результаты исследования нельзя уверенно экстраполировать на генеральную совокупность.
Интерпретация результатов исследования
Патологическая васкуляризация является ключевым процессом в развитии сосудистой системы опухоли [19–21]. Микрососудистая сеть злокачественного очагового образования ПЖ состоит из 2 типов сосудов: сосуды нормальной ткани и сосуды, возникающие в результате неоваскуляризации. Новые опухолевые сосуды имеют нерегулярный извилистый ход, неравномерный диаметр, артериовенозные шунты, глухие концы, много бифуркаций и трифуркаций, в их стенке нет гладкомышечного слоя и слабо выражено покрытие перицитов [22]. Этими особенностями строения опухолевых сосудов объясняется повышенный приток микропузырьков УКП в злокачественной ткани и быстрый отток из него в сравнении с интактной тканью. Соответственно кривая накопления для РПЖ характеризуется быстрым подъемом с последующим быстрым падением [23].
По результатам данной работы злокачественные очаги характеризовались гиперинтенсивным контрастированием (59,0%), быстрым накоплением (56,0%) и быстрым вымыванием УКП (59,0%). Доброкачественные очаги характеризовались изоэхогенным контрастированием (56,0%) с накоплением и вымыванием, сопоставимым с неизмененной паренхимой — 76,0 и 80,0% соответственно. Проведенный ROC-анализ показал, что лучшие прогностические возможности в диагностике РПЖ среди показателей, полученных с помощью программного обеспечения ультразвукового аппарата, были у порогового значения «PI ≥ 34,1 дБ».
В ряде исследований показано увеличение прогностической ценности количественных показателей ультразвукового исследования с контрастным усилением в диагностике рака предстательной железы путем расчета индексов с учетом количественных показателей неизмененной паренхимы [24–26]. В данном исследовании был произведен расчет индексов с учетом показателей интактной периферической зоны. Так, чувствительность порогового значения «Индекс PI ≥ 1,004» в диагностике рака предстательной железы составила 92,7% при низкой специфичности — 48,0%. Пороговое значение «Индекс DT/2 ≤ 0,993» имело наилучшую специфичность (68,0%) и предсказательную ценность положительного результата (79,0%) среди индексов. Пороговые значения «Индекс PI ≥ 1,004» и «Индекс TTP ≤ 0,955» показали наилучшую точность — 75,8%. Таким образом, использование индексов с учетом количественных показателей неизмененной паренхимы не позволило оптимально повысить диагностическую эффективность стандартных параметров. Для повышения информативности нами был предложен способ количественной оценки формы кривой накопления с помощью измерения углов накопления и вымывания.
По результатам ROC-кривых пороговое значение «угол накопления ß ≥ 69,5°» показало чувствительность 73,2%, специфичность 60,0%. Пороговое значение «угол вымывания α ≤ 69,5°» имело чувствительность 63,4%, специфичность 56,0%. Учитывая, что для РПЖ характерно быстрое накопление и вымывание контрастного препарата, произвели комплексную оценку диагностической значимости углов. Чувствительность порогового значения «угол ß ≥ 69,5° + угол α ≤ 69,5°» составила 92,7%, специфичность 80,0%, точность 87,9%, ПЦПР 88,4%, ПЦОР 87,0%.
ЗАКЛЮЧЕНИЕ
ТРУЗИ с контрастным усилением и количественным анализом позволяет проводить дифференциальную диагностику очаговых поражений предстательной железы. Применение количественных параметров и индексов в комплексе позволяет получить более полную информацию для дифференциации очаговой патологии предстательной железы. Комплексное применение разработанных нами количественных оценок кривой накопления (углов накопления и вымывания) обосновано высокими показателями информативности в диагностике рака предстательной железы (чувствительность 92,7%, специфичность 80%).
1 Каприн А.Д., Старинский В.В., Шахзадова А.О. Злокачественные новообразования в России в 2019 году (заболеваемость и смертность). М.: МНИОИ им. П.А. Герцена — филиал ФГБУ «НМИЦ радиологии» Минздрава России. 2020. 252 с.
2 Хасанов М.З., Тухбатуллин М.Г., Савельева Н.А., Хидиятов И.Р., Хисамутдинов А.Н. Патент на изобретение № 2741212, Российская Федерация, A61B 8/00. Способ диагностики злокачественных очаговых образований периферической зоны предстательной железы. 2020110467/14, заявл. 12.03.2020. опубл. 22.01.2021. Бюллетень № 3.
3 Хасанов М.З., Тухбатуллин М.Г., Савельева Н.А., Хидиятов И.Р., Хисамутдинов А.Н. Патент на изобретение № 2749126, Российская Федерация, A61B 8/08 Способ дифференциальной диагностики очаговых образований предстательной железы. 2020115406, заявл. 06.05.2020. опубл. 04.06.2021. Бюллетень № 16.
Список литературы
1. Bray F., Ferlay J., Soerjomataram I., Siegel R.L., Torre L.A., Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J. Clin. 2018; 68(6): 394–424. DOI: 10.3322/caac.21492
2. Pernar C.H., Ebot E.M., Wilson K.M., Mucci L.A. The Epidemiology of Prostate Cancer. Cold Spring Harb. Perspect. Med. 2018; 8(12): a030361. DOI: 10.1101/cshperspect.a030361
3. Torre L.A., Bray F., Siegel R.L., Ferlay J., Lortet-Tieulent J., Jemal A. Global cancer statistics, 2012. CA Cancer J. Clin. 2015; 65(2): 87–108. DOI: 10.3322/caac.21262
4. Попов С.В., Орлов И.Н., Демидов Д.А., Сулейманов М.М., Гулько А.М. Возможности ультразвукового исследования в доплеровском режиме в профилактике геморрагических осложнений биопсии предстательной железы. Урологические ведомости. 2019; 9(3): 29– 32. DOI: 10.17816/uroved9329-32
5. Кравчук В.Н. Применение эластографии сдвиговой волны при трансректальной биопсии для скрининговой диагностики рака предстательной железы. Урология. 2019; 23(2(89)): 159– 164. DOI: 10.26641/23075279.23.2.2019.169157
6. Pummer K., Rieken M., Augustin H., Gutschi T., Shariat S.F. Innovations in diagnostic imaging of localized prostate cancer. World J. Urol. 2014; 32(4): 881–890. DOI: 10.1007/s00345-013-1172-6
7. Smeenge M., de la Rosette J.J., Wijkstra H. Current status of transrectal ultrasound techniques in prostate cancer. Curr. Opin. Urol. 2012; 22(4): 297–302. DOI: 10.1097/MOU.0b013e3283548154
8. Кадрев А.В., Митькова М.Д., Камалов А.А., Митьков В.В. Мультипараметрическая ультразвуковая диагностика рака предстательной железы. Ультразвуковая и функциональная диагностика. 2021; 3: 37–70. DOI: 10.24835/1607-0771-2021-3-37-70
9. Postema A., Mischi M., de la Rosette J., Wijkstra H. Multiparametric ultrasound in the detection of prostate cancer: a systematic review. World J. Urol. 2015; 33(11): 1651–1659. DOI: 10.1007/s00345015-1523-6
10. Tang J., Li X., Wang N., Zhang S., Lin Q., Li J., Shi H. Correlation between hypoechoic nodules on ultrasonography and benign hyperplasia in the prostatic outer gland. J. Ultrasound. Med. 2005; 24(4): 483–488. DOI: 10.7863/jum.2005.24.4.483
11. Державец Л.А., Красный С.А., Летковская Т.А., Карман А.В., Максимов Д.М., Бакунович В.А., Ванзиндо Е.И., Шиманец С.В. Ранняя диагностика рака предстательной железы с использованием ультразвуковой эластографии сдвиговой волны. Вестник Витебского государственного медицинского университета. 2021; 20(6): 43–55. DOI: 10.22263/2312-4156.2021.6.43
12. Postema A.W., Frinking P.J., Smeenge M., De Reijke T.M., De la Rosette J.J., Tranquart F., Wijkstra H. Dynamic contrast-enhanced ultrasound parametric imaging for the detection of prostate cancer. BJU Int. 2016; 117(4): 598–603. DOI: 10.1111/bju.13116
13. Dietrich C.F., Averkiou M., Nielsen M.B., Barr R.G., Burns P.N., Calliada F., Cantisani V., Choi B., Chammas M.C., Clevert D.A., Claudon M., Correas J.M., Cui X.W., Cosgrove D., D’Onofrio M., Dong Y., Eisenbrey J., Fontanilla T., Gilja O.H., Ignee A., Jenssen C., Kono Y., Kudo M., Lassau N., Lyshchik A., Franca Meloni M., Moriyasu F., Nolsøe C., Piscaglia F., Radzina M., Saftoiu A., Sidhu P.S., Sporea I., Schreiber-Dietrich D., Sirlin C.B., Stanczak M., Weskott H.P., Wilson S.R., Willmann J.K., Kim T.K., Jang H.J., Vezeridis A., Westerway S. How to perform Contrast-Enhanced Ultrasound (CEUS). Ultrasound Int. Open. 2018; 4(1): E2–E15. DOI: 10.1055/s-0043-123931
14. Morel D.R., Schwieger I., Hohn L., Terrettaz J., Llull J.B., Cornioley Y.A., Schneider M. Human pharmacokinetics and safety evaluation of SonoVue, a new contrast agent for ultrasound imaging. Invest. Radiol. 2000; 35(1): 80–85. DOI: 10.1097/00004424-200001000-00009
15. Sano F., Uemura H. The utility and limitations of contrast-enhanced ultrasound for the diagnosis and treatment of prostate cancer. Sensors (Basel). 2015; 15(3): 4947–49457. DOI: 10.3390/s150304947
16. Wildeboer R.R., Postema A.W., Demi L., Kuenen M.P.J., Wijkstra H., Mischi M. Multiparametric dynamic contrast-enhanced ultrasound imaging of prostate cancer. Eur. Radiol. 2017; 27(8): 3226–3234. DOI: 10.1007/s00330-016-4693-8
17. Koh J., Jung D.C., Oh Y.T., Yoo M.G., Noh S., Han K.H., Rha K.H., Choi Y.D., Hong S.J. Additional Targeted Biopsy in Clinically Suspected Prostate Cancer: Prospective Randomized Comparison between Contrast-Enhanced Ultrasound and Sonoelastography Guidance. Ultrasound Med. Biol. 2015; 41(11): 2836–28341. DOI: 10.1016/j.ultrasmedbio.2015.06.024
18. Maxeiner A., Fischer T., Schwabe J., Baur A.D.J., Stephan C., Peters R., Slowinski T., von Laffert M., Marticorena Garcia S.R., Hamm B., Jung E.M. Contrast-Enhanced Ultrasound (CEUS) and Quantitative Perfusion Analysis in Patients with Suspicion for Prostate Cancer. Ultraschall. Med. 2019; 40(3): 340–348. DOI: 10.1055/a-0594-2093
19. Melegh Z., Oltean S. Targeting Angiogenesis in Prostate Cancer. Int. J. Mol. Sci. 2019; 20(11): 2676. DOI: 10.3390/ijms20112676
20. Russo G., Mischi M., Scheepens W., De la Rosette J.J., Wijkstra H. Angiogenesis in prostate cancer: onset, progression and imaging. BJU Int. 2012; 110(11 Pt C): E794–808. DOI: 10.1111/j.1464-410X.2012.11444.x
21. Rawla P. Epidemiology of Prostate Cancer. World J. Oncol. 2019; 10(2): 63–89. DOI: 10.14740/wjon1191
22. Seitz M., Gratzke C., Schlenker B., Buchner A., Karl A., Roosen A., Singer B.B., Bastian P.J., Ergün S., Stief C.G., Reich O., Tilki D. Contrast-enhanced transrectal ultrasound (CE-TRUS) with cadence-contrast pulse sequence (CPS) technology for the identifi cation of prostate cancer. Urol. Oncol. 2011; 29(3): 295–301. DOI: 10.1016/j.urolonc.2009.03.032
23. Хасанов М.З., Тухбатуллин М.Г., Савельева Н.А., Хачатурян В.А. Возможности ультразвукового исследования с внутривенным контрастированием в диагностике рака предстательной железы. Сибирский научный медицинский журнал. 2021; 41(2): 66–73. DOI: 10.18699/SSMJ20210209
24. Huang H., Zhu Z.Q., Zhou Z.G., Chen L.S., Zhao M., Zhang Y., Li H.B., Yin L.P. Contrast-enhanced transrectal ultrasound for prediction of prostate cancer aggressiveness: The role of normal peripheral zone time-intensity curves. Sci. Rep. 2016; 6: 38643. DOI: 10.1038/srep38643
25. Кадрев А.В., Митькова М.Д., Рязанцев А.А., Камалов А.А., Митьков В.В. Количественный анализ трансректального ультразвукового исследования с контрастным усилением в диагностике рака предстательной железы (индексы): предварительные результаты. Ультразвуковая и функциональная диагностика. 2020; 3: 12–25. DOI: 10.24835/1607-0771-2020-3-12-25
26. Тимофеева Л.А., Александров Ю.К., Юсова М.А., Алешина Т.Н. Комплексное применение методов лучевой диагностики в выявлении фолликулярных неоплазий щитовидной железы: ретроспективное когортное исследование. Кубанский научный медицинский вестник. 2021; 28(6): 42–58. DOI: 10.25207/1608-6228-2021-28-6-42-58
Об авторах
М. З. ХасановРоссия
Хасанов Марат Зуфарович — кандидат медицинских наук; ассистент кафедры ультразвуковой диагностики Казанской ГМА — филиала Российская медицинская академия непрерывного профессионального образования; врач отделения ультразвуковой диагностики Республиканский КОД имени профессора М.З. Сигала.
Тел.: +7 (903) 388-64-28; ул. Ломжинская, д. 16, г. Казань, 420140; Сибирский тракт, д. 29, г. Казань, 420029
М. Г. Тухбатуллин
Россия
Тухбатуллин Мунир Габдулфатович — доктор медицинских наук, профессор; заведующий кафедрой ультразвуковой диагностики.
Ул. Бутлерова, д. 36, г. Казань, 420012
М. Н. Насруллаев
Россия
Насруллаев Магомед Нухкадиевич — доктор медицинских наук, профессор; профессор кафедры хирургии.
Ул. Бутлерова, д. 36, г. Казань, 420012
Дополнительные файлы
Рецензия
Для цитирования:
Хасанов М.З., Тухбатуллин М.Г., Насруллаев М.Н. Значение трансректального ультразвукового исследования с контрастным усилением в дифференциальной диагностике очаговой патологии предстательной железы: одноцентровое ретроспективное сравнительное исследование. Кубанский научный медицинский вестник. 2023;30(1):58-68. https://doi.org/10.25207/1608-6228-2023-30-1-58-68
For citation:
Khasanov M.Z., Tukhbatullin M.G., Nasrullaev M.N. Contrast-Enhanced Transrectal Ultrasound for Differential Diagnosis of Focal Pathology of Prostate: Single-Center Retrospective Comparative Study. Kuban Scientific Medical Bulletin. 2023;30(1):58-68. (In Russ.) https://doi.org/10.25207/1608-6228-2023-30-1-58-68
JATS XML








































