Перейти к:
Эффективность комплексного стоматологического лечения лихеноидных реакций мукопародонтального комплекса: одноцентровое пилотное когортное исследование
https://doi.org/10.25207/1608-6228-2023-30-6-102-111
Аннотация
Введение. Лихеноидные реакции слизистой оболочки рта на сегодня являются проблемным полем для врачей-стоматологов различного профиля, так как уровень их знаний и профессиональных компетенций по диагностике и патогенетическому лечению лихеноидных поражений полости рта недостаточен. Указанная проблема остро требует решения с учетом данных о наличии высокого онкогенного потенциала у отдельных форм лихеноидных реакций слизистых оболочек полости рта, актуализируя проявление особой онконастороженности от врача-стоматолога при приеме этих пациентов.
Цель исследования — оценить эффективность комплексного лечения стоматологических пациентов с лихеноидными поражениями мукопародонтального комплекса.
Методы. Проведено одноцентровое пилотное когортное исследование по оценке эффективности применения комплекса (фармакои физиотерапия) лечения пациентов с лихеноидными реакциями слизистой оболочки полости рта. Группу наблюдения составили 49 пациентов (15 мужчин, 34 женщины) в возрасте 58,92 ± 0,82 года с верифицированными диагнозами лихеноидных реакций слизистой оболочки полости рта. Предлагаемый комплекс лечения включал в себя фармакотерапию (высокоактивные топические стероиды, ингибиторы кальциневрина) и физиотерапию с использованием низкоинтенсивного лазерного излучения (режим 635 нм, 10 Вт), которую проводили с использованием аппарата лазерного терапевтического «Матрикс» («Матрикс», Россия). Оценку эффективности лечения проводили по результатам динамики суммарной шкалы эффективности лечения, регистрирующей показатели площади очагов поражения и выраженность болевого симптома, а также изменению стоматологических показателей качества жизни по индексу специализированного опросника «Профиль влияния стоматологического здоровья» OHIP-49-RU (Oral Health Impact Profile) в русскоязычной версии. Статистическая обработка данных проводилась с использованием t-критерия Стьюдента для связанных совокупностей или критерия Вилкоксона для связанных совокупностей. Отличия считали значимыми при р ≤ 0,05. Статистический анализ данных выполняли в программе SPSS 13.0 (SPSS Inc., США).
Результаты. Показатели суммарной шкалы эффективности лечения за период наблюдения статистически значимо ( p < 0,001) снизились у 100 % пациентов и составили в виде медиан и квартилей: 6,0 (4,0–7,0) балла (до лечения) и 1,0 (1,0–2,0) балла (после лечения), что было объективизировано значительным сокращением площади участков поражения (на 63,2 %, p < 0,001) и снижением выраженности болевого симптома (спонтанная боль — с 2,0 (1,5–3,0) балла до лечения до 0,0 (0,0–1,0) балла после лечения; индуцированная боль — с 3,0 (2,0–3,0) до 1,0 (0,0–1,0) балла). Клиническое улучшение сопровождалось улучшением стоматологических показателей качества жизни по индексу OHIP-49 RU (Oral Health Impact Profile) с 83,11 ± 2,58 до 39,94 ± 0,86 балла соответственно.
Заключение. Раннее выявление и дифференциация лихеноидных реакций слизистых оболочек полости рта позволяют своевременно приступить к лечению с использованием разработанного протокола комплексного лечения (фармакои физиотерапия), эффективность которого подтверждена клинически и обоснована с позиций качества жизни.
Ключевые слова
Для цитирования:
Гилева О.С., Либик Т.В., Рогожников Г.И., Гибадуллина Н.В., Рогожников А.Г., Гавриленко М.С. Эффективность комплексного стоматологического лечения лихеноидных реакций мукопародонтального комплекса: одноцентровое пилотное когортное исследование. Кубанский научный медицинский вестник. 2023;30(6):102-111. https://doi.org/10.25207/1608-6228-2023-30-6-102-111
For citation:
Gileva O.S., Libik T.V., Rogozhnikov G.I., Gibadullina N.V., Rogozhnikov A.G., Gavrilenko M.S. Efficacy of comprehensive dental treatment for lichenoid reactions of the mucoparodontal complex: A single-center pilot cohort study. Kuban Scientific Medical Bulletin. 2023;30(6):102-111. (In Russ.) https://doi.org/10.25207/1608-6228-2023-30-6-102-111
ВВЕДЕНИЕ
Лихеноидные реакции (ЛР) слизистой оболочки рта (СОР) и пародонта составляют проблемное поле для врача-стоматолога различного профиля, требуют понимания механизмов возникновения, комплексных подходов к диагностике и выбору метода лечения с учетом генеза заболевания [1–15]. По данным ВОЗ (2020), у населения земного шара частота выявления ЛР в тканях мукопародонтального комплекса увеличивается на фоне нарастания случаев полипрагмазии, частоты приема (часто бесконтрольного) лекарственных препаратов с лихенизирующим побочным действием, числа пациентов с иммунодефицитными состояниями, тяги к потреблению табака и табак-содержащих смесей. Свой вклад в прирост частоты выявления ЛР СОР вносит и повышение качества их диагностики на стоматологическом приеме.
Данные о частоте лихеноидных поражений СОР и пародонта в российской популяции практически отсутствуют, уровень знаний и профессиональных компетенций по диагностике и патогенетическому лечению ЛР СОР у отечественных стоматологов недостаточен [16]. Указанные проблемы требуют ургентного решения, учитывая актуальные данные о наличии высокого онкогенного потенциала у отдельных форм лихеноидных поражений слизистой оболочки рта, что требует от врача-стоматолога проявления особой онконастороженности при приеме этих пациентов1. C позиций современной стоматологии и дерматовенерологии ЛР рассматриваются как иммуноопосредованное воспаление, развивающееся в тканях мукопародонтального комплекса и (или) кожи в ответ на действие идентифицированного антигена (лекарственные средства, стоматологические (конструкционные, реставрационные и др.) материалы, средства гигиены полости рта, пищевые продукты, табак-содержащие смеси и др.) [4][6][11][14]. Выделяют [3] 4 основные группы ЛР, проявляющихся на слизистой оболочке рта: 1) Поражения по типу контактной аллергической реакции замедленного типа на стоматологические материалы (L23.0 — аллергический контактный стоматит/дерматит, вызванный металлами; К12.12 — стоматит, связанный с ношением зубного протеза, К12.14 — контактный стоматит, стоматит «ватного валика»; Т81.50 — амальгамовая «татуировка»); 2) Лекарственно-обусловленные ЛР, чаще сочетанно поражающие ткани полости рта и кожу (L42.2Х — проявления в полости рта в ответ на действие лекарственного средства; Т36-Т-50 — стоматит медикаментозный); 3) ЛР, обусловленные «болезнью трансплантат против хозяина» (Graft Versus Host Disease, GVHD); 4) Неклассифицированные ЛР на средства гигиены полости рта (зубные пасты, ополаскиватели, жевательные резинки с активными ингредиентами), табак и табак-содержащие смеси, отдельные вкусовые и ароматические добавки в составе пищевых продуктов, а также на факторы производственной среды (парафенилендиамин, эфир метакриловой кислоты и др.) по L24.3, L24.6, L 24.8 и др.).
Патогенетические особенности каждой формы лихеноидных поражений мукопародонтального комплекса предполагают проявление в различных клинико-топографических и гистологических паттернах (устойчивых признаках), обуславливают различные подходы к диагностике и дифференциальной диагностике, определяют особенности стоматологического лечения (консервативного, ортопедического и др.) в комплексной терапии пациента. Эрозивные, эрозивно-язвенные и смешанные клинические паттерны лихеноидных поражений СОР 1-й и 3-й групп, потенциал озлокачествления которых, по некоторым данным [17–23], варьирует от 0,4 до 6,5 %, представляют наиболее серьезную дифференциально-диагностическую, лечебную и прогностическую дилемму для практикующих стоматологов терапевтического, ортопедического, хирургического и, реже, ортодонтического профиля.
Низкий уровень разработанности многогранной проблемы лихеноидных реакций СОР, недостаточная информационная и методологическая база для формирования профессиональных компетенций врача-стоматолога различного профиля по диагностике, дифференциальной диагностике, профилактике и лечению пациентов с ЛР СОР различного генеза предопределили цель настоящего исследования.
Цель исследования — оценить эффективность комплексного лечения стоматологических пациентов с лихеноидными поражениями мукопародонтального комплекса.
МЕТОДЫ
Дизайн исследования
Дизайн работы построен в виде одноцентрового пилотного когортного исследования, которое проведено среди 49 пациентов с лихеноидными реакциями слизистой оболочки рта в возрасте от 40 до 75 лет.
Условия проведения
Исследование проведено на базах ряда профильных клинических кафедр стоматологического факультета, регионального центра по лечению заболеваний слизистой оболочки рта и поликлинического отделения многопрофильной клинической больницы федерального государственного бюджетного образовательного учреждения высшего образования «Пермский государственный медицинский университет имени академика Е. А. Вагнера» Министерства здравоохранения Российской Федерации. Исследование проводилось с августа 2022 по январь 2023 г. Продолжительность периода наблюдения пациентов — 21 день.
Критерии соответствия
Критерии включения
Сознательное решение пациента участвовать в исследовании, подтвержденное письменным информированным согласием; наличие субъективных (выраженный дискомфорт/болевой симптом/ощущение стянутости и сухости в полости рта, чувство жжения СОР, чувство тревоги, симптом канцерофобии, связанные с необычным видом гиперемированной, отечной, эрозированной слизистой полости рта) и объективных (наличие участков гиперемии, эрозивных и язвенных элементов на слизистой полости рта) симптомов эритематозных и эрозивно-язвенных лихеноидных поражений мукопародонтального комплекса; возраст пациента от 40 до 75 лет; лекарственный анамнез, не отягощенный приемом препаратов с лихеноидным действием; отсутствие вредных привычек (табакокурение, использование табак-содержащих и др. смесей); отсутствие хронических системных заболеваний в стадии декомпенсации/обострения, ограничивающих активность или угрожающих жизни пациента (ASA (American Society of Anesthesiology) I–II: ASA I — сохранное системное здоровье, отсутствие риска стоматологического лечения; ASA II — легкое (среднетяжелое) течение системной патологии, компенсируемое медикаментозно; минимальные риски стоматологического лечения, консультации соответствующих специалистов перед стоматологическим лечением); высокая настроенность пациента на проведение дополнительных исследований и комплексное лечение, достаточная комплаентность к поддержанию стоматологического здоровья.
Критерии невключения
Отсутствие письменно подтвержденного информированного согласия на участие в исследовании; возраст до 40 и старше 75 лет; длительный прием по назначению врача лекарственных препаратов с лихенизирующим действием; наличие «белых» гиперкератотических паттернов ЛР и их клинических форм с подозрением на озлокачествление; наличие системной патологии в декомпенсированной форме (ASA III–V: ASA III — среднетяжелое течение одной или нескольких форм системной патологии; сохранная трудоспособность, ограничение активности; определенные риски стоматологического лечения, требующие консультаций соответствующих специалистов и подготовки к стоматологическому лечению пациента; ASA IV — пациенты с тяжелой системной патологией, ограничивающей их активность, составляющей угрозу для жизни пациента; высокие риски стоматологического лечения; ASA V — пациенты в состоянии агонии, без надежды выжить в ближайшие 24 часа без/после оперативного вмешательства); низкая настроенность к проведению необходимых лечебно-диагностических мероприятий и недостаточная комплаентность к поддержанию стоматологического здоровья.
Критерии исключения
Отказ от дальнейшего участия в исследовании, отказ от выполнения врачебных рекомендаций, беременность/лактация.
Описание критериев соответствия (диагностические критерии)
Диагностические критерии для пациентов с ЛР СОР: тип клинического паттерна — эритематозный, эрозивно-язвенный (наличие участков гиперемии, эрозивных и язвенных элементов на слизистой полости рта); преимущественно фиксированная локализация элементов поражения, топографически связанная с установленной реставрацией/конструкцией/применением средств гигиены полости рта; положительный патч-тест на аллергизирующий агент (стоматологический материал/средство гигиены полости рта).
Подбор участников в группы
Не предусмотрен. Группа наблюдения 49 пациентов была сформирована из общего числа пациентов (n = 537) с хроническими заболеваниями СОР, обратившихся в центр за лечебно-консультативной помощью в период с сентября 2022 по январь 2023 г.
В соответствии с рекомендациями [1][6][8][13][14] комплексное лечение эрозивно-язвенных лихеноидных поражений начинали с проведения терапевтической санации полости рта с использованием максимально атравматичных методов профессиональной гигиены, лечения кариеса зубов и заболеваний пародонта, устраняли в полости рта местные потенциально лихенизирующие факторы (зубные протезы, пломбы и др.). Индивидуальные планы комплексного патогенетического лечения составляли исходя из рекомендаций EAOM (European Association of Oral Medicine) с учетом выраженности болевого, отечно-воспалительного, ксеростомического, сенсорно-парестетического, геморрагического и других симптомов, данных дополнительных лабораторных исследований.
При эрозивно-язвенном и смешанных паттернах ЛРС первые 7–10 дней проводили аппликации высокоактивных топических стероидов (клобетазол 0,05 % (мазь/крем)) на участки поражения. Клобетазол обладает выраженным противовоспалительным, противоаллергическим и иммуносупрессорным действием. Механизм противовоспалительного действия: подавление всех фаз воспаления, стабилизация мембран клеточных и субклеточных структур, предупреждение выхода из клетки протеолитических ферментов, торможение образования свободных радикалов кислорода и перекисей липидов в мембранах. Иммуносупрессорный эффект обусловлен уменьшением количества и активности Т-лимфоцитов, циркулирующих в крови, снижением продукции иммуноглобулинов и влиянием Т-хелперов на В-лимфоциты, понижением содержания комплемента в крови, образования фиксированных иммунных комплексов, интерлейкинов -1, -2, фактора некроза опухоли (ФНО)-α. Клобетазол демонстрирует более выраженные терапевтические эффекты по сравнению с другими топическими стероидами, позволяя достичь высокой терапевтической эффективности при меньшем числе аппликаций в день, а также удлинения периода ремиссии.
На 2-й неделе переходили на негормональные топические средства (особенно при наличии противопоказаний, присоединении грибковой инфекции) — топические ингибиторы кальциневрина в качестве иммуномодулирующей и противовоспалительной терапии (пимекролимус 1 % крем). Пимекролимус является производным макролактама аскомицина и обладает противовоспалительным действием, избирательно ингибирует продукцию и высвобождение цитокинов и медиаторов воспаления из Т-лимфоцитов и тучных клеток, специфично связывается с цитозольным рецептором макрофилином-12 и ингибирует кальций-зависимую фосфатазу — кальциневрин, что приводит к подавлению пролиферации Т-лимфоцитов и предотвращает транскрипцию и выработку Т-хелперами цитокинов: интерлейкина-2, интерферона-γ, интерлейкина-4, интерлейкина-5, интерлейкина-10, ФНО-α и гранулоцитарно-макрофагального колониестимулирующего фактора. Пимекролимус проявляет неспецифическое иммуномодулирующее действие при воспалении, т. к. не влияет на рост кератиноцитов, фибробластов и эндотелиальных клеток и, в отличие от кортикостероидов, оказывает селективное действие на клетки иммунной системы, не вызывая нарушений функции клеток Лангерганса и дендритных клеток моноцитарного происхождения.
На 3-й неделе использовали увлажняющие средства и средства гигиены полости рта (заменители слюны; мягкая стимуляция слюноотделения — лазеротерапия (НИЛИ); увлажняющие зубные пасты; смазывание губ лубрикантами).
По показаниям проводили местную противогрибковую терапию (клотримазола 1 % крем 3–4 раза в день).
Фармакотерапию дополняли физиотерапией с использованием низкоинтенсивного лазерного излучения, которую проводили с использованием аппарата лазерного терапевтического «Матрикс» («Матрикс», Россия). На 1–2-й неделе аппарат использовали с целью снижения воспаления и стимуляции регенерации, а также улучшения микроциркуляции в тканях пародонта и СОР, используя дистантную внутриротовую методику (лазерная головка непрерывного излучения КЛО3 со стоматологической насадкой С-1–2: длина волны — 635 нм, мощность — 10 мВт, время воздействия 1,5–2 мин. на участок поражения). На 3-й неделе аппарат использовали для стимуляции слюноотделения, используя контактную внеротовую методику (лазерная головка непрерывного излучения КЛО3: длина волны — 635 нм, мощность — 10 мВт, время воздействия 1,5–2 мин. на проекцию околоушных и поднижнечелюстных слюнных желез). Общее лечение включало: коррекцию диетического рациона (исключение острой, пряной, горячей пищи/напитков); антигистаминные препараты 3-го поколения (Эриус, Зодак, Супрастинекс и др.) или 2-го поколения (цетеризин и др.) по схеме в течение 7–10 дней; назначение препаратов Zn (цинктерал, сульфат Zn в таб. по 1 табл. 3 раза в день курсом) для стимуляции слюноотделения, особенно у лиц со сниженным уровнем Zn в сыворотке крови; нормализацию микробиоты полости рта (спрей от кровоточивости десен «ДентаБаланс®», синбиотический комплекс, содержащий Streptococcus Thermophilus лизат и пребиотики) и организма (про-, пре-, синбиотики); проведение мероприятий по формированию онконастороженности у пациента. По достижении эпителизации очагов поражения совместно с врачом-аллергологом-иммунологом проводили индивидуальный подбор постоянного реставрационного/конструкционного материала с учетом результатов индивидуального патч-теста. Все пациенты также ставились на обязательное диспансерное наблюдение — 4 раза в год (в течение 1-го года), 2 раза в год (в последующие 2 года).
Целевые показатели исследования
Основной показатель исследования
Оценка эффективности комплексного (фармако-, физиотерапия) лечения стоматологических пациентов с лихеноидными поражениями мукопародонтального комплекса.
Дополнительные показатели исследования
Не предусмотрены.
Методы измерения целевых показателей
Эффективность комплексного лечения пациентов с ЛР СОР оценивали по состоянию СОР и пародонта в динамике, до и по завершении курса терапии (до 21-го дня), определяли непосредственные результаты лечения. В исследовании использовали визуальный, люминесцентный, планиметрический методы, метод клинического фотомониторинга очагов поражения, рассчитывали параметры суммарной шкалы эффективности лечения (СШЭЛ) в баллах, по суммарным показателям визуально-аналоговой шкалы (VAS) спонтанной и индуцированной боли (по 0–4 балла: где 0 — отсутствие боли, 1 — слабая боль, 2 — средняя интенсивность боли, 3 — сильная боль, 4 — нестерпимая боль) и площади эритемы/эрозирования согласно критериям площади (S) очага (ов) поражения < 5 % общей площади СОР — 1 балл, S от 5 до 15 % — 2 балла, S от 16 до 25 % — 3 балла и S более 25 % — 4 балла. Эффективным считали лечение, при котором показатели боли и площади поражения давали убыль на менее чем на 50 и более % к концу первой недели лечения относительно исходных данных, а к концу курса достигали не менее 95 %.
В дополнение к профессиональной оценке динамики заболевания и эффективности лечения учитывали субъективное мнение пациента по критериям: улучшение (значительное, слабое), отсутствие эффекта, ухудшение. Ориентировались также на динамику стоматологических показателей качества жизни пациента по изменению параметров специализированного опросника «Профиль влияния стоматологического здоровья» OHIP-49-RU2. Опросник OHIP-49-RU состоит из 49 вопросов, объединенных в 7 шкал, по которым оцениваются наиболее существенные параметры нарушения КЖ стоматологического больного: ограничение функций (ОФ), физическая боль и физический дискомфорт (ФД), психологический дискомфорт (ПД), физические расстройства (ФР), психологические расстройства (ПР), социальная дезадаптация (СД) и ущерб (У), возникающий в результате стоматологической патологии (от утраты трудоспособности до инвалидизации — физический ущерб, материальный ущерб и т. д.). Пациентам предлагалось ответить на каждый из 49 вопросов опросника по 5 категориям, ранжированным по балльным (от 0 до 4) показателям. Более высокий показатель индекса соответствовал более низкому уровню КЖ. Диапазон баллов по суммарному показателю OHIP-49-RU варьировал от 0 (идеально высокий уровень качества жизни) до 196 баллов («обнуление» качества жизни). Учитывая, что в отечественной литературе отсутствуют данные о вариантах популяционной нормы по индексу OHIP-49 для соматически сохранных жителей РФ с интактной полостью рта, ориентировались на значения контрольной нормы OHIP-49-RU (24,1 ± 3,2 балла), установленные в процессе многоступенчатой валидации этого опросника 2.
В процессе обследования для подтверждения диагноза всесторонне анализировали лекарственный анамнез, наличие и характер вредных привычек, топическую сопряженность зон лихенизации с конструкциями зубных протезов, реставрационными материалами, рациональность (с позиций безопасности) программ индивидуальной гигиены полости рта, наличие корреляционных связей по данным кожно-аппликационных тестов, по показаниям — результатов общего и биохимического анализов крови (уровень железа, ферритин, витамины группы В, ревматоидный фактор), микробиологического культурального исследования. По показаниям пациентов направляли на консультацию к аллергологу-иммунологу, терапевту, клиническому фармакологу, дерматовенерологу.
Переменные (предикторы, конфаундеры, модификаторы эффекта)
В задачи данного исследования не входило определение предикторов течения ЛР СЛР. Факторы, которые могли бы модифицировать результаты проводимой терапии (прием лекарственных препаратов с лихенизирующим действием; наличие «белых» гиперкератотических паттернов ЛР СОР, в т. ч. с подозрением на озлокачествление; наличие системной патологии в декомпенсированной форме; низкая комплаентность к поддержанию стоматологического здоровья; беременность/лактация) исходно были отнесены к критериям исключения и отсутствовали у исследуемых пациентов.
Статистические процедуры
Принципы расчета размера выборки
Размер выборки предварительно не рассчитывался. Пилотный профиль исследования позволял на небольшой выборке пациентов с ЛР СОР получить предварительную информацию о терапевтической эффективности курсового лечения деструктивных форм лихеноидных поражений для проведения дальнейших высокоуровневых многоцентровых исследований в укрупненных выборках соответственно установленным наиболее чувствительным клиническим профилям.
Статистические методы
Статистическая обработка результатов исследования проведена методами параметрической статистики c расчетом среднего арифметического (M), стандартной ошибки среднего (m) для выборок, у которых нормальность числового распределения (количественные показатели) не отклонялась по критерию Колмогорова и Смирнова. Описательная статистика приведена в виде (M ± m). Для таких выборок статистическую значимость различий средних значений рассчитывали по t-критерию Стьюдента для связанных совокупностей. При характеристике порядковых показателей или при отклонении закона распределения выборки от нормального закона распределения описательную статистику представляли в виде значения медианы и первого и третьего квартилей Me (Q1–Q3). Для таких выборок статистическую значимость различий значений медиан рассчитывали по критерию Вилкоксона для связанных совокупностей. Отличия считали статистически значимыми при p ≤ 0,05. Статистический анализ данных выполняли в программе SPSS 13.0 (SPSS Inc., США).
РЕЗУЛЬТАТЫ
Формирование выборки исследования
В выборку включались пациенты с установленными и подтвержденными диагнозами ЛР СОР, обращавшиеся за медицинской помощью в региональный центр по лечению заболеваний слизистой оболочки рта и поликлиническое отделение многопрофильной клинической больницы ФГБОУ ВО «Пермский государственный медицинский университет имени академика Е. А. Вагнера» Минздрава России. Включение пациентов осуществлялось в порядке их обращения при соответствии критериям включения и отсутствии критериев невключения, без каких-либо дополнительных условий. Из 56 пациентов, вошедших в выборку, 7 пациентов отказались от участия в исследовании.
Блок схема дизайна проведенного исследования представлена на рисунке 1.
Характеристики выборки (групп) исследования
В исследование включены 49 пациентов (15 мужчин и 34 женщины в возрасте от 47 до 68 лет, средний возраст пациентов в группе наблюдения составил 58,92 ± 0,82 года) с диагнозами: L23.0 — аллергический контактный стоматит/дерматит, вызванный металлами; К12.12 — стоматит, связанный с ношением зубного протеза, К12.14 — контактный стоматит, стоматит «ватного валика»; Т81.50 — амальгамовая «татуировка»; L24.8 — простой контактный стоматит/периоральный дерматит, вызванный раздражающим действием продуктов гигиены полости рта.
Основные результаты исследования
Установлено что, лихеноидные поражения мукопародонтального комплекса чаще (34; 69,4 %) выявлялись у женщин, чем у мужчин. Согласно классификации МКБ-10 ЛР СОР чаще (27; 55,1 %) проявлялись как аллергический контактный стоматит, вызванный металлами конструкций зубных протезов (преимущественно металлокерамические мостовидные протезы) — L23.0, простым контактным стоматитом/периоральным дерматитом, вызванным раздражающим действием продуктов гигиены полости рта — L24.8 (9; 18,4 %), а также стоматитом, связанным с ношением зубных протезов (из акрилата), наличием композитных реставраций — К12.12, K12.14 (13;26,5 %).
У пациентов доминировал (36; 73,5 %) эрозивно-язвенный клинический паттерн, проявляющийся резко болезненными эрозивными и/или язвенными, чаще односторонними сливными эрозиями или язвами в зоне топографической привязанности к конструкции зубного протеза/реставрации. У 18,4 % лиц с ЛР, обусловленными аллергизирующим и раздражающим действием активных ингредиентов продуктов гигиены полости рта (в основном зубные пасты и жевательные резинки с перечной мятой), чаще определялись разлитые эритематозные участки СОР, проявляющиеся выраженным болевым, ксеростомическим и парестетическим симптомами.
Исходно площадь зон «красных» лихеноидных поражений составила 8,09 ± 0,69 см 2 в среднем на один клинический случай, выраженность болевого симптома по VAS составляла в виде медиан 2,0 (1,5–3,0) балла и 3,0 (2,0–3,0) балла по показателям спонтанной и индуцированной боли соответственно. Интегральный показатель СШЭЛ составил до лечения в виде медианы 6,0 (4,0–7,0) балла. Клинические симптомы проявлялись снижением стоматологических составляющих качества жизни по индексу OHIP-49-RU до 83,11 ± 2,58 балла.
По завершении комплексного лечения у пациентов группы наблюдения фиксировали положительный эффект комплексного лечения пациентов с ЛР СОР, объективизированный с помощью СШЭЛ, медиана показателя которой статистически значимо (p < 0,001) снизились со значений медианы 6,0 (4,0–7,0) балла (до лечения) до значений медианы с квартилями 1,0 (1,0–2,0) балла (после лечения). Для углубленной оценки динамики показателя СШЭЛ, определения особенностей противовоспалительного, анальгезирующего и заживляющего действия апробируемых лечебных комплексов у пациентов с ЛР СОР проведен динамический анализ внутришкаловых показателей СШЭЛ: VAS-боли (выраженность спонтанного и индуцированного болевого симптома) и площади эрозивно-язвенных дефектов. Пошкаловые показатели представлены в таблице 1.
Визуально и люминесцентно выявляли значительное сокращение площади участков поражения (рис. 2).
К концу курса терапии у 59,1 % пациентов исчезли клинические проявления заболевания. У 20 (40,9 %) пациентов к концу курса комплексной терапии площадь участков поражения составила 2,98 ± 0,33 см 2 против 13,1 ± 0,75 см 2 до начала лечения (р < 0,001), причем изначально патология СОР у них протекала по эрозивно-язвенному паттерну. В целом по группе убыль площади поражения составила 63,2 % (8,09 ± 0,69 см 2 против 2,98 ± 0,33 см 2 до и после лечения соответственно при статистической значимости р < 0,001). Выраженность спонтанного и индуцированного болевого симптома также значимо (p < 0,001) снизилась.
К концу срока наблюдения только у 24,5 % (12 пациентов) наблюдались ощущения дискомфорта в состоянии покоя, у 40,8 % (20 пациентов) — быстропроходящее чувство жжения СОР при приеме раздражающей пищи. По субъективным мнениям пациентов эффективность комплексного лечения была оценена как «значительное улучшение» в 93,9 % (46 пациентов) случаев. У 3-х пациентов в процессе лечения возникли осложнения в виде присоединения грибковой инфекции, что повлияло на субъективную оценку пациентом результатов лечения и было оценено ими по критерию «слабое улучшение».
Положительная клиническая динамика по суммарной шкале эффективности лечения сопровождалась достоверным (p < 0,001) улучшением стоматологических показателей качества жизни пациентов по индексу «Профиль влияния стоматологического здоровья» OHIP-49 RU с 83,11 ± 2,58 балла до лечения до 39,94 ± 0,86 балла после лечения.
Дополнительные результаты исследования
Не получены.
Нежелательные явления
Не выявлены.
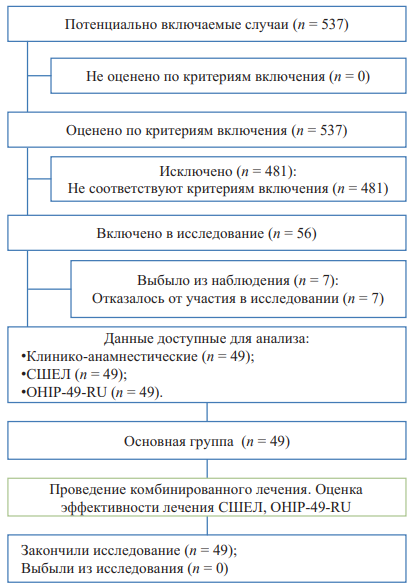
Рис. 1. Блок-схема проведенного исследования
Примечание: блок-схема выполнена авторами (согласно рекомендациям STROBE). Сокращения: СШЭЛ — суммарная шкала эффективности лечения; OHIP-49-RU — Oral Health Impact Profile-49-RU («Профиль влияния стоматологического здоровья»).
Fig. 1. Schematic diagram of the scientific layout
Note: performed by the authors (according to STROBE recommendations). Abbreviations: СШЭЛ — total scale of treatment efficacy; OHIP-49-EN — Oral Health Impact Profile-49-RU.
Таблица 1. Интегральный и пошкаловые показатели суммарной шкалы эффективности лечения (СШЭЛ) у пациентов группы наблюдения до и после проведенного лечения
Table 1. Integral and scale indicators of the total scale of treatment efficacy (СШЭЛ) in patients of the observation group before and after treatment
Показатели
Точки | Пошкаловые показатели СШЭЛ | Интегральный показатель СШЭЛ, баллы Me (Q1–Q3) | ||
Площадь участка поражения, см 2 (M ± m) | Спонтанная боль (VAS), баллы Me (Q1–Q3) | Индуцированная боль (VAS), баллы Me (Q1–Q3) | ||
До лечения (n = 49) | 8,09 ± 0,69 | 2,0 (1,5–3,0) | 3,0 (2,0–3,0) | 6,0 (4,0–7,0) |
После лечения (n = 49) | 2,98 ± 0,33 | 0,0 (0,0–1,0) | 1,0 (0,0–1,0) | 1,0 (1,0–2,0) |
Критерий значимости различий, p | p < 0,001* | p < 0,001** | p < 0,001** | p < 0,001** |
Примечание: таблица выполнена авторами; * — по критерию Стьюдента для зависимых выборок, ** — по критерию Вилкоксона для зависимых выборок. Сокращения: СШЭЛ — суммарная шкала эффективности лечения.
Note: compiled by the authors; * — according to the Student’s t-test for matched samples, ** — according to the Wilcoxon’s t-test for matched samples. Abbreviations: СШЭЛ — total scale of treatment efficacy.

Рис. 2. Пациент, 52 года. Диагноз: L24.8 — простой контактный стоматит, вызванный раздражающим действием продуктов гигиены полости рта. Состояние слизистой оболочки полости рта (СОР) до начала лечения: гиперемия и эрозии (выделено фигурой), 31, 32, топографический код по ВОЗ (ТК ВОЗ); субъективные жалобы на боль (спонтанную и индуцированную) в полости рта; СШЭ = 8 баллов; OHIP-49-RU = 84 балла (А, Б). Состояние СОР после проведенного лечения (на 10-й день): СОР по 31, 32 ТК ВОЗ физиологической окраски, сохраняются единичные папулезные элементы по 31 ТК ВОЗ. Эффективность проведенного лечения субъективно оценивается как «значительное улучшение»; СШЭЛ = 0 баллов; OHIP-49-RU = 37 баллов (В, Г)
Примечание: рисунки выполнены авторами. Сокращения: СШЭ — суммарная шкала эффективности лечения; СОР — слизистая оболочка полости рта; OHIP-49-RU — Oral Health Impact Profile-49-RU («Профиль влияния стоматологического здоровья»).
Fig. 2 (А–Г). Patient, 52 years. Diagnosis: L24.8 — simple contact stomatitis induced by amyctic effect of oral hygiene products. Oral mucosa before treatment: hyperemia and erosions (indicated by a figure) 31, 32 topographic code according to World Health Organization, WHO (International Classification of Health Interventions, ICHI); complaints about pain (spontaneous and induced) in the oral cavity; СШЭЛ = 8 points; OHIP-49-RU = 84 points (А, Б). Post-treatment status of oral mucosa (on day 10): Oral mucosa is of physiological color, according to ICHI 31, 32; single papular elements according to ICHI 31. The treatment efficacy is personally evaluated as “significant improvement”; СШЭЛ = 0 points; OHIP-49-RU = 37 points (В, Г)
Note: performed by the authors. Abbreviations: СШЭЛ — total scale of treatment efficacy; OHIP-49-RU — Oral Health Impact Profile-49-RU.
ОБСУЖДЕНИЕ
Резюме основного результата исследования
Значимым результатом проведенного исследования являются полученные исследователями данные об эффективности комплексного (фармако-, физиотерапия) лечения пациентов с лихеноидными реакциями мукопародонтального комплекса, объективизированные по суммарной шкале эффективности лечения и индексу OHIP-49-RU.
Ограничения исследования
Не выявлены.
Интерпретация результатов исследования
Стоматологи различного профиля активно осваивают доказательную базу о частоте выявления, клинической симптоматологии, принципах выявления, дифференциальной диагностике, рисках малигнизации и методах комплексного лечения пациентов с эрозивно-язвенными и эритематозными формами лихеноидных поражений СОР и пародонта. Однако систематизированная информация о направлениях патогенетического лечения отдельных клинических форм ЛР СОР в отечественной литературе практически не представлена. Вместе с тем в многочисленных зарубежных публикациях последних лет констатируется, что в практике врача-стоматолога (преимущественно терапевта-стоматолога и ортопеда-стоматолога) при приеме пациентов с различными реактивными изменениями СОР все чаще возникают особые клинические ситуации, требующие знаний по проблематике лихеноидных кожно-слизистых поражений, навыков ассоциативного мышления, умений дифференциальной диагностики, взвешенного подхода к выбору диагностических тестов, объективной оценки их информативности для последующей верификации диагноза, прогнозирования течения заболевания, максимально раннего начала базовой и последующей поддерживающей терапии согласованно с врачом-дерматовенерологом, аллергологом-иммунологом и другими специалистами [8–15][20–23].
Предложенный комплекс лечения 1-й и 4-й групп лихеноидных реакций СОР может широко использоваться в стоматологической практике, так как показал убедительную эффективность в настоящем клинико-социологическом исследовании.
ЗАКЛЮЧЕНИЕ
Таким образом, раннее выявление и корректная дифференциация различных форм лихеноидных поражений слизистой оболочки рта позволили своевременно приступить к лечению пациентов с лихеноидными реакциями полости рта по разработанному нами протоколу комплексного лечения (фармако- и физиотерапия), эффективность которого была подтверждена клинически по суммарной шкале эффективности лечения. Стоматологические параметры качества жизни по данным опросника OHIP-49-RU в динамике могут рассматриваться как показатель оценки эффективности проведенного лечения у пациентов с хронической патологией слизистой оболочки рта, в частности с лихеноидными реакциями мукопародонтального комплекса.
1. Гилева О., Кошкин С., Либик Т., Городилова Е., Халявина И. Пародонтологические аспекты заболеваний слизистой оболочки полости рта: красный плоский лишай. Пародонтология. 2017;22 (3):9–14.
2. Гилева О. С., Халилаева Е. В., Либик Т. В., Подгорный Р. В., Халявина И. Н., Гилева Е. С. Многоступенчатая валидация международного опросника качества жизни «Профиль влияния стоматологического здоровья» OHIP-49-RU. Уральский медицинский журнал. 2009;82 (6):106–111.
Список литературы
1. McParland H. Oral Lichenoid and Lichen Planus-like Lesions. Prim Dent J. 2016;5(1):34–39. https://doi.org/10.1177/205016841600500103
2. Fortuna G, Aria M, Schiavo JH. Drug-induced oral lichenoid reactions: a real clinical entity? A systematic review. Eur J Clin Pharmacol. 2017;73(12):1523–1537. https://doi.org/10.1007/s00228-017-2325-0
3. Netto JNS, Pires FR, Costa KHA, Fischer RG. Clinical features of oral lichen planus and oral lichenoid lesions: an oral pathologist’s perspective. Braz Dent J. 2022;33(3):67–73. https://doi.org/10.1590/01036440202204426
4. Nagaraj T, Saxena S, Nigam H, Sahu P, Biswas A. Oral lichenoid reaction on right buccal mucosa: A case report. Nagaraj T, editor. Journal of Advanced Clinical & Research Insights. 2018;5(2):56–57. http://dx.doi.org/10.15713/ins.jcri.210
5. Khudhur AS, Di Zenzo G, Carrozzo M. Oral lichenoid tissue reactions: diagnosis and classification. Expert Rev Mol Diagn. 2014;14(2):169–184. https://doi.org/10.1586/14737159.2014.888953
6. Aminzadeh A, Jahanshahi G, Ahmadi M. A retrospective comparative study on clinico-pathologic features of oral lichen planus and oral lichenoid lesions. Dent Res J (Isfahan). 2013;10(2):168–172. https://doi.org/10.4103/1735-3327.113328
7. Müller S. Oral lichenoid lesions: distinguishing the benign from the deadly. Mod Pathol. 2017;30(s1):S54–S67. https://doi.org/.1038/modpathol.2016.121
8. Rotaru D, Chisnoiu R, Picos AM, Picos A, Chisnoiu A. Treatment trends in oral lichen planus and oral lichenoid lesions (Review). Exp Ther Med. 2020;20(6):198. https://doi.org/10.3892/etm.2020.9328
9. González-Moles MÁ, Ramos-García P, Warnakulasuriya S. The importance of understanding the terminology on oral lichenoid lesions for future research: in reply. Oral Oncol. 2021;117:105282. https://doi.org/10.1016/j.oraloncology.2021.105282
10. Rahat S, Kashetsky N, Bagit A, Sachdeva M, Lytvyn Y, Mufti A, Maibach HI, Yeung J. Can We Separate Oral Lichen Planus from Allergic Contact Dermatitis and Should We Patch Test? A Systematic Review of Chronic Oral Lichenoid Lesions. Dermatitis. 2021;32(3):144–150. https://doi.org/10.1097/DER.0000000000000703
11. Tsushima F, Sakurai J, Shimizu R, Harada H. A case report of oral lichenoid lesions related to cross-reactivity between nickel and palladium. Contact Dermatitis. 2021;85(6):700–701. https://doi.org/10.1111/cod.13932
12. Lu R, Zhou G. Oral lichenoid lesions: Is it a single disease or a group of diseases? Oral Oncol. 2021;117:105188. https://doi.org/10.1016/j.oraloncology.2021.105188
13. Hosseinpour Sarmadi M, Taghavi Zonouz A, Bahramian A, Ghorbanihaghjo A, Javadzadeh F. Comparison of CEA and IgG serum levels in oral lichenoid lesions before and after treatment with topical corticosteroids. J Dent Res Dent Clin Dent Prospects. 2022;16(2):130–134. https://doi.org/10.34172/joddd.2022.022
14. Tsushima F, Sakurai J, Shimizu R, Kayamori K, Harada H. Oral lichenoid contact lesions related to dental metal allergy may resolve after allergen removal. J Dent Sci. 2022;17(3):1300–1306. https://doi.org/10.1016/j.jds.2021.11.008
15. González-Moles MÁ, Ramos-García P. Oral lichen planus and related lesions. What should we accept based on the available evidence? Oral Dis. 2023;29(7):2624–2637. https://doi.org/10.1111/odi.14438
16. Гилева О.С., Либик Т.В. Сложные клинические варианты мукопародонтальных поражений: десквамативный гингивит. Пермский медицинский журнал. 2023;40(1):41–52. https://doi.org/10.17816/pmj40141-52
17. Fitzpatrick SG, Hirsch SA, Gordon SC. The malignant transformation of oral lichen planus and oral lichenoid lesions: a systematic review. J Am Dent Assoc. 2014;145(1):45–56. https://doi.org/10.14219/jada.2013.10
18. Aghbari SMH, Abushouk AI, Attia A, Elmaraezy A, Menshawy A, Ahmed MS, Elsaadany BA, Ahmed EM. Malignant transformation of oral lichen planus and oral lichenoid lesions: A meta-analysis of 20095 patient data. Oral Oncol. 2017;68:92–102. https://doi.org/10.1016/j.oraloncology.2017.03.012
19. Iocca O, Sollecito TP, Alawi F, Weinstein GS, Newman JG, De Virgilio A, Di Maio P, Spriano G, Pardiñas López S, Shanti RM. Potentially malignant disorders of the oral cavity and oral dysplasia: A systematic review and meta-analysis of malignant transformation rate by subtype. Head Neck. 2020 Mar;42(3):539–555. https://doi.org/10.1002/hed.26006
20. Suzuki T, Suemitsu M, Nakayama M, Taguchi C, Ukigaya M, Nakamura C, et al. Histopathological and Immunohistochemical Study of the Distinction between Oral Lichen Planus and Oral Lichenoid Lesions. Open Journal of Stomatology. 2021;11(02):91–106. http://dx.doi.org/10.4236/ojst.2021.112008
21. Warnakulasuriya S, Kujan O, Aguirre-Urizar JM, Bagan JV, GonzálezMoles MÁ, Kerr AR, Lodi G, Mello FW, Monteiro L, Ogden GR, Sloan P, Johnson NW. Oral potentially malignant disorders: A consensus report from an international seminar on nomenclature and classification, convened by the WHO Collaborating Centre for Oral Cancer. Oral Dis. 2021;27(8):1862–1880. https://doi.org/10.1111/odi.13704
22. Kumari P, Debta P, Dixit A. Oral Potentially Malignant Disorders: Etiology, Pathogenesis, and Transformation Into Oral Cancer. Front Pharmacol. 2022;13:825266. https://doi.org/10.3389/fphar.2022.825266
23. Li JW, Li KY, Chan BWA, McGrath CP, Zheng LW. Rate of Malignant Transformation Differs Based on Diagnostic Criteria for Oral Lichenoid Conditions: A Systematic Review and Meta-Analysis of 24,277 Patients. Cancers (Basel). 2023;15(9):2537. https://doi.org/10.3390/cancers15092537
Об авторах
О. С. ГилеваРоссия
Гилева Ольга Сергеевна — доктор медицинских наук, профессор, заведующая кафедрой терапевтической стоматологии и пропедевтики стоматологических заболеваний.
Ул. Петропавловская, д. 26, Пермь, 614990
Т. В. Либик
Россия
Либик Татьяна Владимировна — кандидат медицинских наук, доцент, доцент кафедры терапевтической стоматологии и пропедевтики стоматологических заболеваний.
Ул. Петропавловская, д. 26, Пермь, 614990
Г. И. Рогожников
Россия
Рогожников Геннадий Иванович — доктор медицинских наук, профессор, профессор кафедры ортопедической стоматологии.
Ул. Петропавловская, д. 26, Пермь, 614990
Н. В. Гибадуллина
Россия
Гибадуллина Наталья Владимировна — кандидат медицинских наук, доцент кафедры терапевтической стоматологии и пропедевтики стоматологических заболеваний.
Ул. Петропавловская, д. 26, Пермь, 614990
А. Г. Рогожников
Россия
Рогожников Алексей Геннадьевич — кандидат медицинских наук, доцент, доцент кафедры ортопедической стоматологии.
Ул. Петропавловская, д. 26, Пермь, 614990
М. С. Гавриленко
Россия
Гавриленко Мария Сергеевна — кандидат медицинских наук, доцент кафедры терапевтической стоматологии и пропедевтики стоматологических заболеваний.
Ул. Петропавловская, д. 26, Пермь, 614990
Рецензия
Для цитирования:
Гилева О.С., Либик Т.В., Рогожников Г.И., Гибадуллина Н.В., Рогожников А.Г., Гавриленко М.С. Эффективность комплексного стоматологического лечения лихеноидных реакций мукопародонтального комплекса: одноцентровое пилотное когортное исследование. Кубанский научный медицинский вестник. 2023;30(6):102-111. https://doi.org/10.25207/1608-6228-2023-30-6-102-111
For citation:
Gileva O.S., Libik T.V., Rogozhnikov G.I., Gibadullina N.V., Rogozhnikov A.G., Gavrilenko M.S. Efficacy of comprehensive dental treatment for lichenoid reactions of the mucoparodontal complex: A single-center pilot cohort study. Kuban Scientific Medical Bulletin. 2023;30(6):102-111. (In Russ.) https://doi.org/10.25207/1608-6228-2023-30-6-102-111
JATS XML








































