Перейти к:
Оптимизация хирургической тактики при кистозном эхинококкозе печени: ретроспективное обсервационное нерандомизированное исследование
https://doi.org/10.25207/1608-6228-2024-31-3-17-29
Аннотация
Введение. Эхинококкоз печени представляет большую угрозу для здоровья и жизни человека. Необходим взвешенный выбор хирургической тактики лечения, чтобы максимально снизить риски инвалидизации и ускорить процесс послеоперационного восстановления. Вопрос, в каких случаях стоит применять традиционные хирургические методы, а в каких можно ограничиться менее травматичными минимально инвазивными вмешательствами под ультразвуковым контролем, остается открытым. Эти доводы и дали повод к проведению данного исследования. В статье представлены результаты различных хирургических методов лечения больных с эхинококковыми кистами печени.
Цель исследования — улучшение результатов лечения больных с кистозным эхинококкозом печени путем оптимизации хирургической тактики с применением чрескожных минимально инвазивных вмешательств и традиционных хирургических вмешательств.
Методы. Проведено нерандомизированное сравнительное исследование на базе государственного бюджетного учреждения здравоохранения города Москвы «Научно-исследовательский институт скорой помощи им. Н. В. Склифосовского Департамента здравоохранения города Москвы». Лечение испытуемых проводилось в период с 2010 по 2020 год, продолжительность периода наблюдения после хирургического лечения составляла 4 года. Были пролечены 78 пациентов с эхинококковыми кистами печени в возрасте от 18 до 78 лет. На дооперационном этапе у всех больных был собран анамнез заболевания, включая моменты миграции в течение жизни. У всех больных диагноз был подтвержден лабораторно, инструментально (компьютерная томография, ультразвуковое исследование) и морфологическим исследованием операционного материала. Все пациенты были распределены на 4 группы: три группы с различными методами применения чрескожно минимально инвазивных вмешательств и группу сравнения с традиционными хирургическими методами. Систематизация материала и первичная математическая обработка были выполнены с помощью программного пакета Excel 2016 (Microsoft, США). Полученные цифровые данные были обработаны методами математической статистики с использованием компьютерной программы IBM SPSS Statistics 26 Version (IBM, США).
Результаты. В распределении выборок исследуемых групп по полу, возрасту, количеству кист и сопутствующих заболеваний статистически значимых различий не выявлено, однако на основании проведенного исследования был получен ряд результатов, свидетельствующих о преимуществах минимально инвазивного лечения эхинококковых кист печени. Несмотря на большую вероятность возникновения желчных свищей и нагноения остаточной полости при применении минимально инвазивных методов, отмечалось статистически значимое сокращение длительности операций, длительности обезболивания в послеоперационном периоде, уменьшение кровопотери, что, в свою очередь, привело к сокращению пребывания в хирургическом стационаре.
Заключение. Применение минимально инвазивных методов возможно при всех типах эхинококковых кист печени наравне с применением традиционных хирургических методов. Минимально инвазивные вмешательства целесообразны при наличии должного оснащения в клинике и опыта хирурга для минимизации послеоперационных осложнений и рецидивов.
Для цитирования:
Бояринов В.С., Рогаль М.Л., Новиков С.В., Джаграев К.Р., Ярцев П.А. Оптимизация хирургической тактики при кистозном эхинококкозе печени: ретроспективное обсервационное нерандомизированное исследование. Кубанский научный медицинский вестник. 2024;31(3):17-29. https://doi.org/10.25207/1608-6228-2024-31-3-17-29
For citation:
Boyarinov V.S., Rogal M.L., Novikov S.V., Dzhagraev K.R., Yartsev P.A. Optimization of the surgical approach to treating hepatic cystic echinococcosis: A retrospective observational non-randomized study. Kuban Scientific Medical Bulletin. 2024;31(3):17-29. https://doi.org/10.25207/1608-6228-2024-31-3-17-29
ВВЕДЕНИЕ
По данным Всемирной организации здравоохранения (ВОЗ), эхинококкозом печени страдают более 2 млрд человек во всем мире. Ежегодно поражаются около 200 человек на 100 тыс. населения [1]. Кистозный эхинококкоз и альвеолярный эхинококкоз являются двумя наиболее распространенными формами эхинококкоза человека и вызываются личиночными стадиями Echinococcus granulosus и Echinococcus multilocularis соответственно [2][3].
В Европейской зоне за 2020 г. было зарегистрировано более 5000 подтвержденных случаев эхинококкоза. Из них больше половины случаев были зарегистрированы как Echinococcus granulosus1.
Эпидемиологическая ситуация по заболеваемости эхинококкозом в Российской Федерации остается также сложной, в общем по стране ежегодно регистрируется свыше 500 новых случаев эхинококкоза2 [4].
Печень является наиболее частой локализацией эхинококковых кист, составляя примерно 70 % наблюдений эхинококкоза всех органов [5][6].
Применение химиотерапии целесообразно при эхинококковых кистах менее 5 см, при отрицательной динамике роста кисты возможно применение минимально инвазивного лечения [7][8].
Основная стратегия хирургического лечения эхинококкоза печени включает традиционную эхинококкэктомию, а также чрескожные минимально инвазивные вмешательства (методы PAI (puncture, aspiration, injection), PAIR (puncture, aspiration, injection, re-aspiration) и PEVAC (perifoveal exudative vascular anomalous complex)) [9][10].
Осложнения и риски после PAI, PAIR не превышают таковые после операций из традиционного доступа [11].
Послеоперационная летальность, по некоторым сообщениям, достигает 0,5–8 %, а частота послеоперационных осложнений колеблется в пределах 12–80 % в зависимости от вида хирургического вмешательства, типа и локализации эхинококковых кист. Рецидив после открытого и минимально инвазивного хирургического лечения возникает в широком диапазоне — от 2 до 22 %3 [12][13].
Это может быть связано с тем, что в хирургическом лечении эхинококкоза печени до сих пор нет единого общепринятого протокола, учитывающего форму и морфологическую стадию заболевания, что связано с недостаточной доказательной базой в плане выработки показаний к различным оперативным доступам (мини-инвазивные, традиционные операции), методы ликвидации и лечения остаточной полости после эхинококкэктомии. Несмотря на то что чрескожные методы удаления эхинококковых кист (ЭК) печени под интроскопическим контролем нацелены на минимальную травму и на быструю реабилитацию с возвращением пациента к обычной жизни и труду в кратчайшие сроки, клиник, где внедрены чрескожные хирургические вмешательства при ЭК, в России не так много [14][15].
В связи с вышесказанным считаем актуальным дальнейшее исследование в направлении определения преимущества одного из хирургических методов (традиционного или минимально инвазивного) лечения эхинококкоза печени.
Цель исследования — улучшение результатов лечения больных с кистозным эхинококкозом печени путем оптимизации хирургической тактики применения чрескожных минимально инвазивных вмешательств и традиционных хирургических вмешательств.
МЕТОДЫ
Дизайн исследования
Проведено ретроспективное обсервационное нерандомизированное клиническое исследование больных с эхинококковыми кистами печени, в исследовании приняли участие 78 пациентов.
Критерии соответствия
Критерии включения
Пациенты с эхинококковыми кистами печени и пациенты с сочетанным поражением печени и других паренхиматозных органов на различных стадиях жизнедеятельности; пациенты, находившиеся на стационарном лечении в государственном бюджетном учреждении здравоохранения города Москвы «Научно-исследовательский институт скорой помощи им. Н. В. Склифосовского Департамента здравоохранения города Москвы» (ГБУЗ «НИИ СП им. Н. В. Склифосовского ДЗМ»), в отделении неотложной хирургии, эндоскопии и интенсивной терапии (хирургическое отделение № 2) с 2010 по 2020 год; возраст пациентов от 18 до 78 лет; размер эхинококковых кист от 5 см и больше; получение добровольного согласия на хирургическое вмешательство.
Критерии невключения
Размер эхинококковых кист менее 5 см.
Критерии исключения
Отказ пациента от дальнейшего участия в исследовании, острые воспалительные заболевания, нарушение свертываемости крови.
Условия проведения исследования
Лечение пациентов проводилось на базе хирургического отделения № 2 ГБУЗ «НИИ СП им. Н. В. Склифосовского ДЗМ» с 2010 по 2020 год.
Продолжительность исследования
Набор групп испытуемых и регистрация результатов проводились в период с 2010 по 2020 год. Продолжительность периода наблюдения составила 10 лет. Продолжительность периода наблюдения после хирургического лечения — 4 года.
Описание медицинского вмешательства
Клинический диагноз выставлялся на основании сбора жалоб, анамнеза заболевания, серологических исследований, УЗИ и КТ органов брюшной полости, цитологического или гистологического исследования операционного материала.
Ведущими современными методами лечения эхинококковой болезни являются минимально инвазивные чрескожные вмешательства, такие как PAI (puncture, aspiration, injection, пункция, аспирация, введение гермицида); PAIR (puncture, aspiration, injection, re-aspiration, пункция, аспирация, введение гермицида, реаспирация); PDE (percutaneous drainage, evacuation, чрескожное дренирование, эвакуация). Для достижения сколецидного эффекта применяли гермициды: глицерин 99 %, гипохлорит натрия 1 %, хлорид натрия 30 %, этиловый спирт от 90 % [16]. Перед выбором любого хирургического способа лечения, будь то традиционные хирургические вмешательства или минимально инвазивные, тактика операций и возможные последствия обсуждаются с больными.
В исследовании среди минимально инвазивных вмешательств преобладала PDE под контролем УЗИ и рентгенографии. PDE была выполнена 27 пациентам, размер кисты превышал 5 см, вмешательства выполнялись больным со всеми типами кист по УЗ классификации Gharbi [17]. Все операции были выполнены в специализированной операционной с наличием ультразвуковых аппаратов «Logiq e» (Китай), «Esaote My lab 70, 500» (Италия) с линейным и конвексным датчиками частотой 3,5–5 мГц и рентгенотелескопическими установками C-дуга «OEC Elite» «GE OEC Medical Systems» (США) и «Siemens Arcadis Avantic» (Германия). Для защиты от облучения вся операционная и анестезиологическая бригады использовали свинцовые рентгенозащитные фартуки и воротники RA623, RA614. Все операции проводили под внутривенным или эндотрахеальным наркозом в положении больного лежа на спине или на боку. После трехкратной обработки операционного поля раствором антисептиков под УЗ-контролем выбирали безопасную траекторию со слоем паренхимы печени над кистой не менее 5 см, а также чтобы на пути движения иглы отсутствовали крупные кровеносные сосуды, желчные протоки, плевральный синус.
Первичные дренирования выполнялись одноэтапной системой стелет-катетерами фирмы Balton 6Fr, 9Fr и 12Fr типа «pig-tail», во всех случаях применяли методику «свободной руки». После разреза кожи от 3–5 мм под УЗ-контролем резким одномоментным движением катетер вводили в кисту. Затем из комплекса извлекали мандрен со стилетом, а трубку низводили в полость кисты и полностью аспирировали содержимое под контролем УЗ. Содержимое полости кисты отправлялось в лабораторию на цитологическое исследование и бактериальный посев. Объем аспирированной жидкости варьировал от 30 до 3000 мл. При этом в 76 % наблюдений отметили чистое прозрачное содержимое с гидатидным песком, а в 24 % получено мутное отделяемое с признаками инфицирования. С целью своевременного выявления связи с желчными протоками проводился анализ содержимого кист на наличие желчных кислот при помощи тест полосок Total Bile Acid (TBA) [18]. Выполнялась цистография, в качестве контрастного вещества использовали Ультравист 100 (Bayer Schering Pharma, Германия). После исключения билиарных свищей в полость кисты вводили 99 % глицерин в количестве от 1/3 до 1/2 части от первичного аспирированного объема с последующей экспозицией в течение 10 минут. По истечении времени экспозиции весь глицерин аспирировали из полости кисты. По трубке в полость вводили J-образный проводник или несколько проводников Amplatz фирмы COOK (Польша). После введения проводников удаляли первичные трубки. По одному из проводников, в зависимости от клинической ситуации, производилось расширение дренажного канала бужами от 18 до 30 Fr фирмы Balton, COOK (Польша). Далее по одному проводнику восстанавливалась одна трубка Balton 9 Fr типа «pig-tail» и по второму проводнику силиконовая трубка фирмы Balton от 18 до 30 Fr в зависимости от размеров кисты. После замены трубок на больший диаметр хитиновые оболочки становились доступными для эвакуации из полости кисты. Все хитиновые оболочки отправлялись на гистологическое исследование. Трубки фиксировались к коже двумя нитками, к дренажам подключали мочеприемники, на рану накладывали асептическую повязку.
Сразу после операции больные переводились в хирургическое отделение общего профиля. С первых часов послеоперационного периода проводилось однократное обезболивание раствором кетопрофена 2,0 мл внутримышечно, никаких физических ограничений не было, больной активировался в первые часы после операции. На 1-е сутки после операции проводился УЗ-контроль плевральных полостей, органов брюшной полости и фистулография. При адекватном дренировании и аспирации при отсутствии жидкостных скоплений в брюшной полости и плевральных полостях пациент выписывался с функционирующими дренажными трубками. Перед выпиской проводили инструктаж о правилах промывания полостей через трубки, перевязках и действиях в непредвиденных ситуациях.
На амбулаторном этапе рекомендуется промывать трубками водным раствором хлоргексидина 0,05 % в разбавлении 1/2 с 0,9 % раствором натрия хлорида, 2 раза в день, объем промывания обговаривается индивидуально с учетом количества первично полученного отделяемого из кисты. После операции больные приходят на контроль каждые 7–14–30 суток в зависимости от размера первичной кисты, анатомических особенностей и динамики облитерации остаточной полости. По мере уменьшения количества отделяемого по трубкам и уменьшения объема остаточной полости производим замену трубок на меньший диаметр. Замены выполняются амбулаторно под рентгеноскопическим контролем без анестезии с учетом уже сформированных дренажных каналов. Срок уменьшения размеров остаточной полости варьируется от 15 до 60 дней. Данный способ не рекомендуется применять у больных с кальцинозом стенок кисты ввиду длительной или невозможной облитерации остаточной полости и ликвидации инфекционного процесса.
Методом PAIR было пролечено 24 пациента, все операции проводились по ранее описанной методике, как и при PDE.
Дренирование выполнялось одноэтапной системой стелет-катетерами фирмы Balton 6 Fr или 9 Fr типа «pig-tail» в зависимости от планируемого к применению сколецидного препарата. Для введения гипохлорита натрия, хлорида натрия или этилового спирта применяли катетеры диаметром 6 Fr, а для глицерина — 9 Fr. Во всех случаях применяли методику «свободной руки». После проведение рентгенофистулографии и исключения билиарных свищей в полость кисты вводили глицерин 99 %, гипохлорит натрия 1 %, хлорид натрия 30 % или этиловый спирт от 90 % в количестве от 1/3 до 1/2 части от первичного аспирированного объема с последующей экспозицией в течение 10 минут. По истечении времени экспозиции весь гермицид аспирируется из полости кисты, трубка удаляется.
Сразу после операции больные переводились в хирургическое отделение общего профиля, в анальгетической терапии они не нуждаются. На 1-е сутки больной выписывается на амбулаторный этап долечивания.
После выписки больные приходят на УЗ-контроль через месяц, далее каждые три месяца. Данный способ применялся у больных со всеми типами кист.
Методом PAI было пролечено 14 пациентов, все операции проводились по ранее описанной методике, как и при PDE и PAIR.
Пункция выполнялась под УЗ-наведением одномоментным способом при помощи пункционной иглы Chiba 18G. После аспирации в полость кисты вводили гипохлорит натрия 1 %, хлорид натрия 30 % или этиловый спирт от 90 % в количестве от 1/3 до 1/2 части от первичного аспирированного объема. Далее пункционная игла удалялась. При отсутствии нежелательных реакций после операции больные выписывались на 1-е сутки.
В исследовании традиционный хирургический метод представлен перицистэктомией с холодноплазменной аргонусиленной электрокоагуляцией фиброзной капсулы, операция выполнена 13 пациентам. Все операции выполнялись под эндотрахеальным наркозом, доступ к кисте производился путем выполнения J-образной лапаротомии. Далее выполнялось интраоперационное УЗИ, которое позволяло уточнить локализацию кист, выявить не видимые ранее кисты, определить соотношение кист с желчными протоками и сосудами печени. До выделения кисты необходимо тщательное отграничение свободной брюшной полости вначале сухими салфетками, затем салфетками, смоченными гермицидом, после производится мобилизация печени традиционным способом в зависимости от локализации кисты. Неосторожные манипуляции до вскрытия кисты могут привести к ее разгерметизации и массивному обсеменению брюшной полости. Чтобы предотвратить диссеминацию сколексов при открытых операциях, мы используем специальный вакуумный аспиратор с мощностью 1000 мм водного столба и выше с широким наконечником от 3 см и более, такое устройство позволяет быстро аспирировать содержимое кисты вместе с хитиновой оболочкой, полностью исключая попадание содержимого в брюшную полость. Следующим этапом выполняется разрез кисты в наиболее выступающей части от паренхимы печени. Содержимое кисты удаляли аспиратором, через этот же разрез весь объем кисты заполняли раствором глицерина 80–100 % с экспозицией не менее 10–15 минут. Время экспозиции имеет принципиальное значение для гибели всех элементов паразита.
После завершения противопаразитарной обработки отверстие в кисте расширяется, производится удаление гермицида и оставшихся элементов жизнедеятельности ЭК. Производится смена перчаток и инструментария, выполняется иссечение стенок кисты, тщательный осмотр внутренней поверхности фиброзной капсулы на предмет желчных свищей. После производится холодноплазменная аргонусиленная электрокоагуляция фиброзной капсулы аппаратом Covidien Argon Gas Delivery Unit II (США). Если после коагуляции желчеистечения нет и гемостаз адекватный, операция заканчивается дренированием остаточной полости дренажной трубкой 12 Fr типа «pig-tail» или силиконовой от 18 до 24 Fr, послойным ушиванием раны. В послеоперационном периоде больные наблюдаются согласно общепринятой хирургической тактике. Всем оперированным больным химиотерапия не применялась.
Исходы исследования
Основной исход исследования
Планировалось уменьшить количество койко-дней пребывания в стационаре, минимизировать хирургическую травматичность у больных с эхинококковыми кистами печени за счет применения минимально инвазивных вмешательств.
Дополнительные исходы исследования
Не предусмотрены.
Анализ в подгруппах
Был обследован 91 пациент. В исследование вошли 78 пациентов. Им были выполнены хирургические вмешательства. Из 13 больных, не вошедших в исследование, в 4 случаях размер кист не превышал 5 см, у 4 выявлены ЭК легкого, 5 пациентов отказались от операции.
Все пациенты, вошедшие в исследование, были распределены на 4 группы: три основные (метод вмешательства PDE, n = 27; метод вмешательства PAI, n = 14; метод вмешательства PAIR, n = 24) и группа сравнения (n = 13). В основных группах — оперированные минимально инвазивными чрескожными методами, в группе сравнения — оперированные традиционными хирургическими методами.
Проведен сравнительный анализ полученных результатов обследования в четырех группах.
Методы регистрации исходов
Эффективность отдаленных результатов лечения и качество жизни больных с эхинококковыми кистами печени оценивали с помощью опросника SF-36. Оценка производилась до операции и через 12 месяцев после.
Опросник MOSSF-36 состоит из 36 вопросов, объединенных в 8 шкал, ответы оцениваются в баллах (от 0 до 100), которые отражают степень удовлетворенности и общее благополучие человека.
Показатели, которые включены в оценку: физическое функционирование (ФФ), ролевое физическое функционирование (РФФ), физическая боль (ФБ) и общее состояние здоровья (ОЗ) — сгруппированы в физический компонент здоровья (ФКЗ). Шкалы: жизненная активность (ЖА), социальное функционирование (СФ), ролевое эмоциональное функционирование (РЭФ) и психологическое здоровье (ПЗ) — сгруппированы в психический компонент здоровья (ПКЗ). Чем выше оценка, тем лучше уровень качества жизни. При полной удовлетворенности здоровьем максимальное значение равно 100 баллам.
Статистический анализ
Принципы расчета размера выборки
Размер выборки предварительно не рассчитывался.
Методы статистического анализа данных
На основании анализа распределений количественных показателей выполняли оценку нормальности распределения (критерии Колмогорова—Смирнова) для последующего применения параметрических или непараметрических методов. В случае соответствия распределения выборки нормальному закону распределения первичных данных применяли описательную статистику в виде среднего арифметического и стандартного отклонения — М ± SD, а сравнительный анализ проводили с помощью параметрических методов (t-критерий Стьюдента, F-критерий Фишера). Если распределения выборок не соответствовали нормальному закону распределения первичных данных, то применяли описательную статистику в виде медианы и первого (Q1–25 %) и третьего квартилей (Q3–75 %) — Ме (Q1; Q3), а сравнительный анализ проводили с помощью непараметрических методов (U-критерий Манна—Уитни, критерий Краскела—Уоллиса). В случае анализа качественных показателей в виде долей (процентов) применяли четырехпольные или многопольные таблицы сопряженности (Хи-квадрат Пирсона, точный критерий Фишера). Уровень статистической значимости p ≤ 0,05 считали статистически значимым. Статистическая обработка полученных данных проводилась с помощью программного пакета Excel 2016 (Microsoft, США). Полученные цифровые данные были обработаны методами математической статистики с использованием компьютерной программы IBM SPSS Statistics 26 Version (IBM, США).
РЕЗУЛЬТАТЫ
Участники исследования
Выборка состояла из 91 пациента, 13 исключены из исследования, а 78 включены в четыре группы для анализа.
Первые три группы представлены минимально инвазивными хирургическими вмешательствами. Группа PDE состояла из 27 пациентов, группа PAI — из 14, группа PAIR — из 24 и группа сравнения, 13 больных, представлена традиционным хирургическим вмешательством: перицистэктомия с холодноплазменной аргонусиленной электрокоагуляцией фиброзной капсулы. Блок-схема дизайна исследования приведена на рисунке 1.
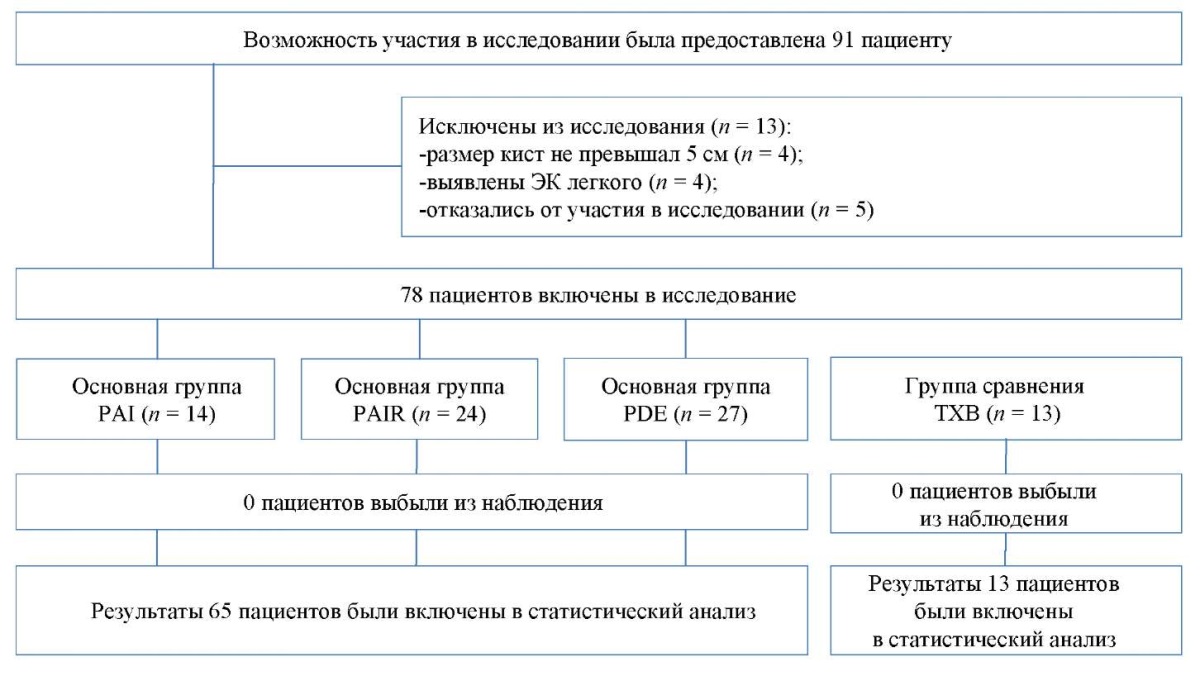
Рис. 1. Блок-схема дизайна исследования
Примечание: блок-схема выполнена авторами (согласно рекомендациям, TREND). Сокращения: ЭК — эхинококковые кисты; PAI — puncture, aspiration, injection (пункция, аспирация, введение гермицида); PAIR — puncture, aspiration, injection, re-aspiration (пункция, аспирация, введение гермицида, реаспирация); PDE — percutaneous drainage, evacuation (чрескожное дренирование, эвакуация); ТХВ — традиционное хирургическое вмешательство.
Fig. 1. Block diagram of the study design
Note: the block diagram was created by the authors (as per TREND recommendations). Abbreviations: ЭК — echinococcal cysts; PAI — puncture, aspiration, injection; PAIR — puncture, aspiration, injection, re-aspiration; PDE — percutaneous drainage, evacuation; ТХВ — traditional surgery.
Характеристика четырех групп исследования по жалобам приведена в таблице 1.
Таблица 1. Жалобы при эхинококковых кистах печени
Table 1. Complaints in patients with hepatic echinococcal cysts
|
Жалобы |
Количество больных, абс. (%) |
|
Астенический синдром |
6 (7,7 %) |
|
Боль в верхних отделах живота |
9 (11,4 %) |
|
Снижение аппетита |
2 (2,6 %) |
|
Гипертермия |
2 (2,6 %) |
|
Аллергическая реакция |
2 (2,6 %) |
|
Бессимптомное течение |
57 (73,1 %) |
|
Всего |
78 (100 %) |
Примечание: таблица составлена авторами.
Note: the table was compiled by the authors.
Бессимптомная (латентная) стадия эхинококкоза выявлена у 57 (73,1 %) пациентов — паразитарные кисты были выявлены случайно в ходе ультразвукового исследования органов брюшной полости; у 21 (26,9 %) пациента наблюдали симптоматику. В общей выборке отмечалось проявление клинических симптомов в виде болевого синдрома в эпигастральной области и правом подреберье (11,4 %), кахексии (7,7 %), аллергической реакции (2,6 %), снижения аппетита (2,6 %), гипертермии (2,6 %). Статистически значимо различались (по критерию хи-квадрат) по долям три группы пациентов с жалобами. Наибольшая часть пациентов с бессимптомным течением — 73,1 %, вторая по численности с жалобами на боль в верхних отделах живота — 11,4 % и группа с остальными жалобами — 15,5 %, доли которых не отличались статистически значимо друг от друга (p > 0,05).
Для установления однородности выборок сравниваемых групп анализировали некоторые показатели: половой состав групп, возраст, ИМТ, количество пациентов с одной кистой или с двумя и больше кистами, количество больных с одним сопутствующим заболеванием или с двумя и больше сопутствующими заболеваниями. В таблице 2 приведены данные показатели.
Таблица 2. Значения некоторых показателей сравниваемых групп пациентов
Table 2. Values of some indicators in the compared patient groups
|
Показатель |
Группа PDE (n = 27) |
Группа PAI (n = 14) |
Группа PAIR (n = 24) |
Группа сравнения (n = 13) |
Уровень значимости, p |
|
Пол (муж./жен.) |
12/15 |
6/8 |
10/14 |
7/6 |
0,909* |
|
Возраст (М ± SD), (лет) |
41,7 ± 15,6 |
44,9 ± 17,3 |
37,1 ± 13,9 |
38,0 ± 14,2 |
0,843# |
|
ИМТ (М ± SD), (у. е.) |
25,5 ± 3,2 |
25,8 ± 3,4 |
24,6 ± 4,6 |
24,4 ± 3,4 |
0,674# |
|
Количество пациентов, имеющих одно/более одного сопутствующего заболевания |
21/6 |
10/4 |
16/8 |
9/4 |
0,989* |
|
Количество пациентов, имеющих одну/более одной кисты |
18/9 |
7/7 |
19/5 |
8/5 |
0,181* |
Примечания: таблица составлена авторами; * — по критерию хи-квадрат, # — по F-критерию Фишера. Сокращения: PAI — puncture, aspiration, injection (пункция, аспирация, введение гермицида); PAIR — puncture, aspiration, injection, re-aspiration (пункция, аспирация, введение гермицида, реаспирация); PDE — percutaneous drainage, evacuation (чрескожное дренирование, эвакуация); ИМТ — индекс массы тела.
Note: the table was compiled by the authors; * — as per the chi-squared test, # — as per the F-test. Abbreviations: PAI — puncture, aspiration, injection; PAIR — puncture, aspiration, injection, re-aspiration; PDE — percutaneous drainage, evacuation; ИМТ — body mass index.
Половой состав групп с помощью многопольной таблицы сопряженности статистически значимо не отличался в группах (p = 0,909), наименьшая доля мужчин (41,7 %) была в группе PAIR, а наибольшая доля (53,8 %) в группе сравнения.
Доли пациентов с одним сопутствующим заболеванием также статистически значимо не отличались друг от друга в группах исследования (p = 0,989) по критерию хи-квадрат, наименьшая доля (66,7 %) была в группе PAIR, а наибольшая доля (77,8 %) в группе PDE.
Аналогично доли пациентов с одной кистой также статистически значимо не отличались друг от друга в группах исследования (p = 0,181) по критерию хи-квадрат, наименьшая доля (50,0 %) была в группе PAI, а наибольшая доля (79,2 %) в группе PAIR.
Предварительно проведенный анализ законов распределения количественных значений возраста и показателя ИМТ по критериям Колмогорова — Смирнова показал, что распределения соответствуют нормальному закону (p > 0,05). Поэтому для сравнения средних значений возраста и ИМТ в группах применяли дисперсионный анализ по F-критерию Фишера (табл. 2).
Статистически значимого различия в возрасте по группам не установлено (p = 0,843), наименьший средний возраст (37,1 ± 13,9 года) был в группе PAIR, наибольший средний возраст (44,9 ± 17,3 года) — в группе PAI.
Статистически значимого различия средних значений ИМТ по группам не установлено (p = 0,674), наименьший средний ИМТ (24,4 ± 3,4) был в группе сравнения, наибольший средний ИМТ (25,8 ± 3,4) — в группе PAI.
По всем сравниваемым показателям группы не отличались статистически значимо (p > 0,05) друг от друга, что указывает на их однородность.
Основные результаты исследования
В таблице 3 отражены медианы показателей шкал опросника SF-36 до хирургического лечения по поводу эхинококковых кист печени. При анализе значения медиан выявлено, что все показатели: ФФ, РФФ, ФБ, ОЗ — физический компонент здоровья и ЖА, СФ, РЭФ, ПЗ — психологический компонент здоровья находятся на уровне здорового человека, не считая изменений за счет возрастных особенностей и наличия хронических заболеваний. Что еще раз подчеркивает, что эхинококкоз печени, как правило, протекает практически бессимптомно.
Таблица 3. Параметры качества жизни MOSSF-36 (в баллах) у пациентов
до хирургического вмешательства на эхинококковых кистах печени
Table 3. MOSSF 36 quality-of-life parameters (score) in patients
prior to surgery for hepatic echinococcal cysts
|
Шкалы MOSSF-36 (баллы) |
Группа PDE (n = 27) |
Группа PAI (n = 14) |
Группа PAIR (n = 24) |
Группа сравнения (n = 13) |
|
ФФ |
90 |
95 |
90 |
90 |
|
РФФ |
90 |
85 |
80 |
90 |
|
ФБ |
95 |
95 |
95 |
90 |
|
ОЗ |
80 |
90 |
85 |
85 |
|
ЖА |
85 |
80 |
90 |
90 |
|
СФ |
90 |
95 |
90 |
95 |
|
РЭФ |
90 |
90 |
95 |
95 |
|
ПЗ |
85 |
80 |
80 |
78 |
|
ФКЗ |
55,1 |
55,7 |
53,5 |
53,7 |
|
ПКЗ |
55,4 |
53,9 |
54,3 |
52,5 |
Примечание: таблица составлена авторами. Сокращения: MOSSF-36 — Medical Outcomes Study Short-Form 36; PAI — puncture, aspiration, injection (пункция, аспирация, введение гермицида); PAIR — puncture, aspiration, injection, re-aspiration (пункция, аспирация, введение гермицида, реаспирация); PDE — percutaneous drainage, evacuation (чрескожное дренирование, эвакуация); ФФ — физическое функционирование; РФФ — ролевое физическое функционирование; ФБ — физическая боль; ОЗ — общее состояние здоровья; ФКЗ — физический компонент здоровья; ЖА — жизненная активность; СФ — социальное функционирование; РЭФ — ролевое эмоциональное функционирование; ПЗ — психологическое здоровье; ПКЗ — психический компонент здоровья.
Note: the table was compiled by the authors. Abbreviations: MOSSF-36 — Medical Outcomes Study Short-Form 36; PAI — puncture, aspiration, injection; PAIR — puncture, aspiration, injection, re-aspiration; PDE — percutaneous drainage, evacuation; ФФ — physical functioning; РФФ — role-physical; ФБ — bodily pain; ОЗ — general health; ФКЗ — physical component summary; ЖА — vitality; СФ — social functioning; РЭФ — role-emotional; ПЗ — mental health; ПКЗ — mental component summary.
При анализе значений медиан шкал ФФ, РФФ, ФБ, ОЗ, отражающих суммарные показатели физического компонента здоровья (ФКЗ), через 12 месяцев после хирургического лечения установлено, что медианы в группе сравнения были снижены по сравнению с медианами в основной группе (PAI, PAIR, PDE). Так, более низкие медианы шкал ФФ и РФФ говорят о том, что у пациентов из группы сравнения в большей мере ограничена физическая активность, чем в основной группе.
При этом медианы ФБ, характеризующие интенсивность боли, снижены в группе сравнения, что отражает большую травматичностью хирургического доступа при традиционных вмешательствах.
В результате анализа полученных данных (табл. 4) установлено, что через год после минимально инвазивного лечения значения медиан психических компонентов здоровья статистически повысились у всех пациентов по сравнению с предоперационными показателями. Полученные результаты по шкалам ПКЗ достигли уровня практически здоровых лиц.
Таблица 4. Параметры качества жизни MOSSF-36 (в баллах) у пациентов
через 12 месяцев после хирургического вмешательства на эхинококковых кистах печени
Table 4. MOSSF 36 quality-of-life parameters (scores) in patients
12 months after surgery for hepatic echinococcal cysts
|
Шкалы MOSSF-36 (баллы) |
Группа PDE (n = 27) |
Группа PAI (n = 14) |
Группа PAIR (n = 24) |
Группа сравнения (n = 13) |
|
ФФ |
95 |
100 |
92 |
80 |
|
РФФ |
95 |
95 |
95 |
85 |
|
ФБ |
100 |
100 |
100 |
90 |
|
ОЗ |
90 |
95 |
95 |
90 |
|
ЖА |
95 |
90 |
95 |
85 |
|
СФ |
95 |
100 |
95 |
90 |
|
РЭФ |
95 |
100 |
95 |
90 |
|
ПЗ |
92 |
90 |
85 |
80 |
|
ФКЗ |
57,3 |
58,5 |
57,8 |
52,1 |
|
ПКЗ |
59,6 |
61,4 |
60,1 |
50,2 |
Примечание: таблица составлена авторами. Сокращения: MOSSF-36 — Medical Outcomes Study Short-Form 36; PAI — puncture, aspiration, injection (пункция, аспирация, введение гермицида); PAIR — puncture, aspiration, injection, re-aspiration (пункция, аспирация, введение гермицида, реаспирация); PDE — percutaneous drainage, evacuation (чрескожное дренирование, эвакуация); ФФ — физическое функционирование; РФФ — ролевое физическое функционирование; ФБ — физическая боль; ОЗ — общее состояние здоровья; ФКЗ — физический компонент здоровья; ЖА — жизненная активность; СФ — социальное функционирование; РЭФ — ролевое эмоциональное функционирование; ПЗ — психологическое здоровье; ПКЗ — психический компонент здоровья.
Note: the table was compiled by the authors. Abbreviations: MOSSF-36 — Medical Outcomes Study Short-Form 36; PAI — puncture, aspiration, injection; PAIR — puncture, aspiration, injection, re-aspiration; PDE — percutaneous drainage, evacuation; ФФ — physical functioning; РФФ — role-physical; ФБ — bodily pain; ОЗ — general health; ФКЗ — physical component summary; ЖА — vitality; СФ — social functioning; РЭФ — role-emotional; ПЗ — mental health; ПКЗ — mental component summary.
Выделен ряд результатов исследования, к которым относились длительность оперативного вмешательства, длительность анальгезии в послеоперационном периоде, продолжительность нахождения в отделении реанимации, послеоперационные осложнения, длительность госпитализации, интраоперационные кровопотери.
Предварительно проведенный анализ законов распределения количественных значений показателей по критериям Колмогорова—Смирнова показал, что часть распределений соответствуют нормальному закону (p > 0,05) (например, количество койко-дней в группах PDE и PAIR), а для части распределений других показателей и в других группах гипотеза о нормальности отклонена (p < 0,05). Исходя из этого, показатели представлены в виде медианы и квартилей, а сравнение проводили с помощью критерия Краскела—Уоллиса (табл. 5).
Таблица 5. Значения некоторых показателей (Ме (Q1; Q3))
по результатам хирургического лечения в сравниваемых группах
Table 5. Values of some indicators (Me (Q1; Q3))
following surgical treatment in the compared groups
|
Показатели |
Группа PDE (n = 27) |
Группа PAI (n = 14) |
Группа PAIR (n = 24) |
Группа сравнения (n = 13) |
Уровень значимости, p |
|
Длительность операции (мин.) |
15 (15; 16) |
7 (6; 9) |
13 (12; 13) |
310 (290;330) |
<0,001 |
|
Длительность послеоперационной анальгезии (дни) |
1 (1; 1) |
0 (0; 0) |
0 (0; 0) |
3 (3; 3) |
0,012 |
|
Койко-дни в реанимации |
0 (0; 0) |
0 (0; 0) |
0 (0; 0) |
1 (1; 2) |
0,006 |
|
Интраоперационная кровопотеря, мл |
10 (8; 10) |
4 (3; 5) |
4 (4; 5) |
150 (150;200) |
<0,001 |
|
Койко-дни в стационаре |
19 (15; 25) |
3 (2; 5) |
15 (10; 27) |
25 (17; 39) |
0,045 |
Примечание: таблица составлена авторами. Сокращения: PAI — puncture, aspiration, injection (пункция, аспирация, введение гермицида); PAIR — puncture, aspiration, injection, re-aspiration (пункция, аспирация, введение гермицида, реаспирация); PDE — percutaneous drainage, evacuation (чрескожное дренирование, эвакуация).
Note: the table was compiled by the authors. Abbreviations: PAI — puncture, aspiration, injection; PAIR– puncture, aspiration, injection, re-aspiration; PDE — percutaneous drainage, evacuation.
Длительность операции в исследуемых группах принимала медианные значения от 7 мин. в группе PAI, 13 мин. в группе PAIR, 15 мин. в группе PDE до 310 мин. в группе сравнения, что статистически значимо (p < 0,001) отличалось. При попарном сравнении с помощью критерия Манна—Уитни между значениями медиан группы PAI и двух групп PAIR и PDE также есть значимое различие. Не выявлено значимого различия медиан групп PAIR и PDE (p > 0,05). Но для всех групп при сравнении с группой сравнения длительность операции была значимо больше. Так, для группы PDE увеличение длительности операции соответствует 20,7 раза. Для других групп еще больше.
Для длительности послеоперационной анальгезии в группе PDE медианное значение составило 1 (1; 1) день, а в группе сравнения 3 (3; 3) дня (p = 0,012). В группах PAI и PAIR этот показатель равен нулю (табл. 5).
Длительность пребывания в отделении реанимации в виде койко-дней не наблюдалась для групп PDE, PAI и PAIR, а в группе сравнения медиана была 1 (1; 2) день (p = 0,006).
Длительность госпитализации в виде койко-дней во всех группах статистически значимо отличалась по критерию Краскела — Уоллиса (p = 0,045). При попарном сравнении по критерию Манна — Уитни в группе сравнения медианное значение было значимо больше 25 (17; 19) дней, чем во всех остальных группах (p < 0,05), для группы PDE — 19 (15; 25) дней, для группы PAI — 3 (2; 5) дня, для группы PAIR — 15 (10; 27) дней (табл. 5).
Объем кровопотери во всех группах статистически значимо отличался по критерию Краскела — Уоллиса (p < 0,001). Для малоинвазивных групп потери были значимо меньше, чем потери крови в группе сравнения (p < 0,001) при попарном сравнении по критерию Манна — Уитни. В группе сравнения интраоперационная кровопотеря составила 150 (150; 200) мл. Аналогичный показатель в группе PDE равен 10 (8; 10) мл, в группе PAI — 4 (3; 5) мл, в группе PAIR — 4 (4; 5) мл, что, в свою очередь, ведет к скорейшей социально-трудовой реабилитации пациентов.
Доля развития послеоперационных осложнений в малоинвазивных группах составила 13,8 %, или 9 осложнений из 65 операций. В группе сравнения — 15,4 %, или 2 осложнения из 13 операций. Статистически значимого различия нет по критерию хи-квадрат (p = 0,359) (табл. 6).
Таблица 6. Количество послеоперационных осложнений в группах сравнения
Table 6. Number of postoperative complications in the compared groups
|
Показатели |
Группа PDE (n = 27) |
Группа PAI (n = 14) |
Группа PAIR (n = 24) |
Группа сравнения (n = 13) |
Уровень значимости, p |
|
Желчный свищ |
2 |
0 |
4 |
2 |
|
|
Абсцессы брюшной полости |
0 |
0 |
0 |
0 |
|
|
Кровотечение |
0 |
0 |
0 |
0 |
|
|
Нагноение остаточной полости |
2 |
0 |
1 |
0 |
|
|
Нагноение послеоперационной раны |
0 |
0 |
0 |
0 |
|
|
Остаточная полость |
0 |
0 |
0 |
0 |
|
|
Всего |
4 |
0 |
5 |
2 |
0,359 |
Примечание: таблица составлена авторами. Сокращения: PAI — puncture, aspiration, injection (пункция, аспирация, введение гермицида); PAIR — puncture, aspiration, injection, re-aspiration (пункция, аспирация, введение гермицида, реаспирация); PDE — percutaneous drainage, evacuation (чрескожное дренирование, эвакуация).
Note: the table was compiled by the authors. Abbreviations: PAI — puncture, aspiration, injection; PAIR– puncture, aspiration, injection, re-aspiration; PDE — percutaneous drainage, evacuation.
Данное явление обуславливалось наличием пациентов с послеоперационными осложнениями, приобретенными в иных медицинских учреждениях. Зачастую больные даже не могли назвать объем выполненной операции, предоставить медицинскую документацию и уж тем более не слышали о послеоперационном наблюдении.
Одним из частых осложнений являлось нагноение остаточной полости. Такое осложнение ликвидировали путем промывания растворами антисептиков или дополнительным дренированием. Наружные желчные свищи были ликвидированы в процессе полной облитерации остаточной полости во всех случаях. В комплексную терапию был добавлен гимекромон, в дозировке 200 мг в среднем на 14 дней до прекращения желчеотделения по трубке. Дополнительных вмешательств для этого не потребовалось. В исследовании не выявлено такое осложнение, как склерозирующий холангит на использование гипертонического солевого раствора, глицерина и спирта.
Наиболее частым осложнением в хирургической практике являются кровотечения. Развитие подобного осложнения во время чрескожных операций несет в себе дополнительную опасность, потому что в этом случае может потребоваться конверсия. Кровотечения в ходе минимально инвазивных вмешательств могут возникнуть либо при непосредственном повреждении крупных сосудов, либо при разрыве капсулы и паренхимы печени во время проведения инструмента. Для исключения подобных осложнений необходимо правильно выбрать траекторию проведения инструмента, убедиться в отсутствии на пути его следования сосудистых структур. Важно видеть иглу на протяжении всей операции, особенно при прохождении через паренхиму печени. В исследовании ни у одного больного не наблюдалось подобных осложнений. С целью достижения окончательного гемостаза при традиционных вмешательствах были применены методы аргоноплазменной электрокоагуляции или местные гемостатические средства (губка, матрица), нанесенные на раневую поверхность паренхимы печени (табл. 4).
Теми же принципами необходимо руководствоваться для профилактики повреждения желчных путей. Ни в одном из наблюдений не отмечено повреждения желчных протоков при минимально инвазивных вмешательствах.
Аллергическая реакция организма, вызванная паразитарной инвазией, является характерным признаком, при эхинококкозе встречается довольно часто. Так как продукты жизнедеятельности эхинококков являются сильными аллергенами, излитие содержимого кисты в свободную брюшную полость может привести к аллергическим реакциям различной степени выраженности. Особенно высок риск, когда вход в кисту осуществляется через свободный край экстрапаренхиматозно расположенной кисты либо слой паренхимы печени над кистой в месте вкола слишком мал. В таких случаях возможно подтекание гидатидной жидкости по ходу пункционного канала. Среди всех оперированных больных аллергических реакций не было.
В дальнейшем все пациенты в течение 4–5 лет наблюдались в ГБУЗ «НИИ СП им. Н. В. Склифосовского ДЗМ» выполнялось: УЗИ брюшной полости, КТ органов брюшной полости, серологическое исследование крови. Частота рецидива эхинококкоза печени, как и летальности, в всех случаях составила 0 %.
Дополнительные результаты исследования
Дополнительных результатов в ходе исследования выявлено не было.
Нежелательные явления
Не выявлены.
ОБСУЖДЕНИЕ
Резюме основного результата исследования
В исследовании продемонстрировано преимущество применения минимально инвазивных методов лечения эхинококковых кист печени за счет меньшего времени оперативного вмешательства, минимальной интраоперационной кровопотери. Всем пациентам из основной группы после операции не требовалось лечение в отделение реанимации и интенсивной терапии. В связи с меньшей травматичностью операций и более ранней активизацией сроки госпитализации сокращаются от одного до двух дней максимум. Важным результатом проведенного исследования являются полученные данные эффективности по шкалам ФКЗ и ПКЗ, свидетельствующие о том, что спустя 1 год после минимально инвазивного лечения установлена преимущественная эффективность лечения пациентов основной группы над группой сравнения.
Обсуждение основного результата исследования
При отсутствии лечения ЭК растет и развивается по одному из нескольких путей: самопроизвольная инактивация; прорыв в брюшную полость с распространением множественных дочерних кист по всей брюшной полости; образование свищей в соседние органы или желчевыводящую систему [19].
Основные варианты лечения кистозного эхинококкоза печени включают в себя выжидательную тактику, медикаментозную терапию, традиционную хирургию и применение минимально инвазивных технологий (МИТ).
В ВОЗ было заявлено, что хирургическое вмешательство остается краеугольным камнем лечения эхинококковой болезни, поскольку данный метод может позволить элиминировать эхинококковую кисту и привести к полному излечению [20]. Наиболее острой проблемой лечения пациентов с эхинококкозом печени является выбор хирургического метода. Хирургия печени значительно продвинулась вперед, но есть ряд нерешенных вопросов, касающихся применения МИТ при кистах типа CE2, CE3 а, CE3b. В ходе нашего исследования мы использовали МИТ при всех типах кист, несмотря на определенные ограничения, навязанные зарубежными и отечественными авторами.
На основании проведенного нами исследования был получен ряд результатов, свидетельствующих о существенных преимуществах использования минимально инвазивных технологий. МИТ были связаны с повышенной эффективностью, более низкими показателями рецидивов заболевания и более коротким пребыванием в стационаре, что, в свою очередь, обеспечивало скорейшую социально-трудовую реабилитацию пациентов.
Несмотря на большую вероятность возникновения послеоперационных осложнений при применении минимально инвазивных методов, отмечалось статистически значимое сокращение длительности операций, длительности обезболивания в послеоперационном периоде, что, в свою очередь, вело к сокращению прибывания в хирургическом стационаре.
Учитывая отсутствие актуальных национальных и зарубежных клинических рекомендаций, остается открытым вопрос о тактике ведения пациентов с эхинококкозом печени, что делает актуальным наше исследование.
Ограничения исследования
Не выявлены.
ЗАКЛЮЧЕНИЕ
Минимально инвазивные чрескожные хирургические вмешательства под УЗ-контролем при эхинококкозе печени применяются наравне с другими хирургическими методами с 1985 года. С развитием технических возможностей хирургии и изменением направления в сторону менее травматичных хирургических методов лечения остаются актуальными вопросы дифференцированного подхода к выбору способа хирургического лечения пациентов с кистозным эхинококкозом печени.
Такие показатели, как длительность оперативного вмешательства, длительность анальгезии в послеоперационном периоде, продолжительность нахождения в отделении реанимации, длительность госпитализации, интраоперационная кровопотеря, статистически значимо были меньше значений в группах с малоинвазивным вмешательством, чем в группе сравнения.
1. European Centre for Disease Prevention and Control. Surveillance systems overview. Stockholm: ECDC; 2021. Available: https://www.ecdc.europa.eu/en/publications-data/surveillance-systems-overview-2021
2. Демиденко Л.А., Федорец А.В., Намазова Л.Э. Динамика развития эхинококкозов в России. Человек — природа — общество: теория и практика безопасности жизнедеятельности, экологии и валеологии. 2019;5 (12):136–140.
3. Икрамов Р.З., Жаворонкова О.И., Ботиралиев А.Ш., Олифир А.А., Степанова Ю.А., Вишневский В.А., Чжао А.В. Современные подходы в лечении эхинококкоза печени. Высокотехнологическая медицина. 2020;7 (2):14–27.
Список литературы
1. Lee PC, Lo C, Lai PS, Chang JJ, Huang SJ, Lin MT, Lee PH. Randomized clinical trial of single-incision laparoscopic cholecystectomy versus minilaparoscopic cholecystectomy. Br J Surg. 2010;97(7):1007–1012. https://doi.org/10.1002/bjs.7087
2. Woolsey ID, Miller AL. Echinococcus granulosus sensu lato and Echinococcus multilocularis: A review. Res Vet Sci. 2021;135:517–522. https://doi.org/10.1016/j.rvsc.2020.11.010
3. Alvi MA, Ali RMA, Khan S, Saqib M, Qamar W, Li L, Fu BQ, Yan HB, Jia WZ. Past and present of diagnosis of echinococcosis: A review (1999–2021). Acta Trop. 2023;243:106925. https://doi.org/10.1016/j.actatropica.2023.106925
4. Драгомерецкая А.Г., Троценко О.Е., Логвин Ф.В., Твердохлебова Т.И., Романова Е.Б., Ищенкова И.В., Москвина Ю.И., Димидова Л.Л., Черникова М.П. Современная эпидемическая ситуация по эхинококкозам на Дальнем Востоке и Юге России. Медицинский вестник Юга России. 2024;15(1):27–35. https://doi.org/10.21886/2219-8075-2024-15-1-27-35
5. Сквoрцoв В.В., Левитан Б.Н., Гoрбaч А.Н. Эхинококкоз и другие паразитарные заболевания печени. Эффективная фармакотерапия. 2020;16(30):88–91. https://doi.org/10.33978/2307-3586-2020-16-30-88-91
6. Baruah A, Sarma K, Barman B, Phukan P, Nath C, Boruah P, Rajkhowa P, Baruah M, Dutta A, Naku N. Clinical and Laboratory Presentation of Hydatid Disease: A Study From Northeast India. Cureus. 2020;12(9):e10260. https://doi.org/10.7759/cureus.10260
7. Алиев М.Ж., Ниязбеков К.И. Эффективность консервативного лечения эхинококкоза. Вестник Смоленской государственной медицинской академии. 2020;19(4):117–122. https://doi.org/10.37903/vsgma.2020.4.19
8. Salm LA, Lachenmayer A, Perrodin SF, Candinas D, Beldi G. Surgical treatment strategies for hepatic alveolar echinococcosis. Food Waterborne Parasitol. 2019;15:e00050. https://doi.org/10.1016/j.fawpar.2019.e00050
9. Wan L, Wang T, Cheng L, Yu Q. Laparoscopic Treatment Strategies for Liver Echinococcosis. Infect Dis Ther. 2022;11(4):1415–1426. https://doi.org/10.1007/s40121-022-00664-2
10. Öztürk G, Uzun MA, Özkan ÖF, Kayaalp C, Tatli F, Eren S, Aksungur N, Çoker A, Bostanci EB, Öter V, Kaya E, Taşar P. Turkish HPB Surgery Association consensus report on hepatic cystic Echinococcosis (HCE). Turk J Surg. 2022;38(2):101–120. https://doi.org/10.47717/turkjsurg.2022.5757
11. Efanov M, Azizzoda Z, Elizarova N, Alikhanov R, Karimkhon K, Melekhina O, Kulezneva Y, Kazakov I, Vankovich A, Chitadze A, Salimgereeva D, Tsvirkun V. Laparoscopic radical and conservative surgery for hydatid liver echinococcosis: PSM based comparative analysis of immediate and long-term outcomes. Surg Endosc. 2022;36(2):1224–1233. https://doi.org/10.1007/s00464-021-08391-4
12. Мусаев Г.Х., Фатьянова А.С., Левкин В.В. Принципы и современные тенденции лечения эхинококкоза печени. Хирургия. Журнал им. Н.И. Пирогова. 2017;(12):90–94. https://doi.org/10.17116/hirurgia20171290-94
13. Wang Z, Zhu HH, Yang JY, Wang Y, Gai ZG, Ma FC, Yang DW. Laparoscopic versus conventional open treatment of hepatic cystic hydatidosis: a systematic review and meta-analysis of cohort studies. Wideochir Inne Tech Maloinwazyjne. 2022 Sep;17(3):406–417. https://doi.org/10.5114/wiitm.2022.115225
14. Киртанасов Я.П., Ившин В.Г. Чрескожные вмешательства в лечении больных многокамерным гидатидным эхинококкозом печени. Вестник новых медицинских технологий. 2019;2:23–32. https://doi.org/10.24411/2075-4094-2019-16365
15. Заривчацкий М.Ф., Мугатаров И.Н., Каменских Е.Д., Колыванова М.В., Теплых Н.С. Хирургическое лечение эхинококкоза печени. Пермский медицинский журнал. 2021;38(3):32–40. https://doi.org/10.17816/pmj38332-40
16. Cai D, Li Y, Jiang Y, Wang H, Wang X, Song B. The role of contrast-enhanced ultrasound in the diagnosis of hepatic alveolar echinococcosis. Medicine (Baltimore). 2019;98(5):e14325. https://doi.org/10.1097/MD.0000000000014325
17. Liu W, Delabrousse É, Blagosklonov O, Wang J, Zeng H, Jiang Y, Wang J, Qin Y, Vuitton DA, Wen H. Innovation in hepatic alveolar echinococcosis imaging: best use of old tools, and necessary evaluation of new ones. Parasite. 2014;21:74. https://doi.org/10.1051/parasite/2014072
18. Khuroo MS. Percutaneous Drainage in Hepatic Hydatidosis-The PAIR Technique: Concept, Technique, and Results. J Clin Exp Hepatol. 2021 Sep-Oct;11(5):592–602. https://doi.org/10.1016/j.jceh.2021.05.005
19. Шамсиев А.М., Шамсиев Ю.А., Рахманов К.Е., Давлатов С.С. Дифференцированная лечебная тактика в хирургии эхинококкоза печени. Экспериментальная и клиническая гастроэнтерология. 2020;5(177):72–77. https://doi.org/10.31146/1682-8658-ecg-177-5-72-77
20. Mönnink GLE, Stijnis C, van Delden OM, Spijker R, Grobusch MP. Percutaneous Versus Surgical Interventions for Hepatic Cystic Echinococcosis: A Systematic Review and Meta-Analysis. Cardiovasc Intervent Radiol. 2021;44(11):1689–1696. https://doi.org/10.1007/s00270-021-02911-4
Об авторах
В. С. БояриновРоссия
Бояринов Владимир Сергеевич — врач-хирург хирургического отделения
пл. Большая Сухаревская, д. 3, г. Москва, 129090
М. Л. Рогаль
Россия
Рогаль Михаил Леонидович — доктор медицинских наук, профессор, заместитель директора по научной работе
пл. Большая Сухаревская, д. 3, г. Москва, 129090
С. В. Новиков
Россия
Новиков Сергей Валентинович — доктор медицинских наук, ведущий научный сотрудник научного отдела неотложной хирургии, эндоскопии и интенсивной терапии
пл. Большая Сухаревская, д. 3, г. Москва, 129090
К. Р. Джаграев
Россия
Джаграев Карен Рубенович — кандидат медицинских наук, зам. главного врача по хирургической работе
пл. Большая Сухаревская, д. 3, г. Москва, 129090
П. А. Ярцев
Россия
Ярцев Петр Андреевич — доктор медицинских наук, профессор, заведующий научным отделом неотложной хирургии, эндоскопии и интенсивной терапии
пл. Большая Сухаревская, д. 3, г. Москва, 129090
Дополнительные файлы
Рецензия
Для цитирования:
Бояринов В.С., Рогаль М.Л., Новиков С.В., Джаграев К.Р., Ярцев П.А. Оптимизация хирургической тактики при кистозном эхинококкозе печени: ретроспективное обсервационное нерандомизированное исследование. Кубанский научный медицинский вестник. 2024;31(3):17-29. https://doi.org/10.25207/1608-6228-2024-31-3-17-29
For citation:
Boyarinov V.S., Rogal M.L., Novikov S.V., Dzhagraev K.R., Yartsev P.A. Optimization of the surgical approach to treating hepatic cystic echinococcosis: A retrospective observational non-randomized study. Kuban Scientific Medical Bulletin. 2024;31(3):17-29. https://doi.org/10.25207/1608-6228-2024-31-3-17-29
JATS XML








































