Перейти к:
Влияние транскраниальной электростимуляции на сывороточную концентрацию интерлейкина-1-бета при COVID-19: рандомизированное проспективное исследование
https://doi.org/10.25207/1608-6228-2025-32-6-41-55
Аннотация
Введение. Интерлейкин-1β играет важную роль в патогенезе коронавирусной инфекции (COVID-19), а также может быть информативен в качестве прогностического маркера инфекции. Другие широко используемые диагностические и прогностические маркеры — С-реактивный белок и ферритин.
Цель исследования: оценка влияния транскраниальной электростимуляции на концентрацию интерлейкина-1β, С-реактивного белка, ферритина в крови у пациентов с COVID-19 среднетяжелого и тяжелого течения, не получающих таргетной противоцитокиновой терапии.
Методы. Рандомизированное проспективное исследование охватило пациентов, проходивших лечение в государственном бюджетном учреждении здравоохранения «Краевая клиническая больница № 2» Министерства здравоохранения Краснодарского края в период с 24.06.2021 по 23.02.2022. Пациенты с диагнозом новой коронавирусной инфекции (COVID-19) среднетяжелого и тяжелого течения разделены на группу сравнения (n = 20), получавшую стандартное лечение в соответствии с действующими методическими рекомендациями, и группу транскраниальной электростимуляции (n = 15), в которой к стандартной терапии дополнительно применялась транскраниальная электростимуляция (один сеанс в день до 7-го дня госпитализации в COVID-отделение). Из исследования исключались пациенты, получавшие специфическую антицитокиновую терапию (моноклональные антитела, киназные ингибиторы, рекомбинантные антагонисты рецепторов цитокинов). Уровни IL-1β, С-реактивного белка и ферритина оценивали до начала лечения и по завершении первой недели терапии. Статистический анализ и визуализация данных выполнены в среде R (The R Foundation, Австрия). Различия считались статистически значимыми при p < 0,05.
Результаты. До начала лечения уровни IL-1β, С-реактивного белка и ферритина между группами статистически значимо не различались. К концу первой недели в группе сравнения уровень IL-1β снизился на 11,8% (p = 0,7), что не являлось статистически значимым. В группе транскраниальной электростимуляции наблюдалось достоверное снижение концентрации IL-1β на 71% от исходного уровня (p = 0,007). К тому же концентрация IL-1β в группе транскраниальной электростимуляции была на 52% ниже, чем в группе сравнения (p = 0,005). Уровень С-реактивного белка значимо снизился в обеих группах, тогда как уровень ферритина статистически значимо не изменился.
Заключение. Включение транскраниальной электростимуляции в комплексное лечение пациентов с COVID-19 среднетяжелого и тяжелого течения способствует более выраженному снижению сывороточной концентрации интерлейкина-1β по сравнению со стандартной терапией, что может свидетельствовать о противовоспалительном потенциале данного метода.
Ключевые слова
Для цитирования:
Игнатенко М.Ю., Кочкарова Е.В., Измайлова Н.В., Занин С.А. Влияние транскраниальной электростимуляции на сывороточную концентрацию интерлейкина-1-бета при COVID-19: рандомизированное проспективное исследование. Кубанский научный медицинский вестник. 2025;32(6):41-55. https://doi.org/10.25207/1608-6228-2025-32-6-41-55
For citation:
Ignatenko M.Yu., Kochkarova E.V., Izmaylova N.V., Zanin S.A. Effect of transcranial electrical stimulation on serum interleukin-1β levels in COVID-19 patients: A randomized prospective study. Kuban Scientific Medical Bulletin. 2025;32(6):41-55. https://doi.org/10.25207/1608-6228-2025-32-6-41-55
ВВЕДЕНИЕ
Коронавирусная инфекция (COVID-19) представляет собой сложный вызов для медицины и здравоохранения современности [1][2]. В основе патогенеза инфекции и ее фатальных осложнений обнаруживается системная иммунная диcрегуляция, в том числе аномальный профиль секреции разнообразных цитокинов. Среди них одно из центральных мест занимает интерлейкин-1β (ИЛ-1β). Гиперпродукция провоспалительных субстанций лежит в основе патогенеза тяжелых, жизнеугрожающих проявлений инфекции: синдрома выброса цитокинов, тромбообразования, вторичного гемофагоцитарного лимфогистиоцитоза (синдрома активации макрофагов), — что в итоге может привести к мультиорганной недостаточности [1–3]. Несмотря на достигнутые успехи в области таргетного противоцитокинового лечения, требуется продолжение поиска лечебных методов, способных повлиять на иммунную диcрегуляцию и другие звенья патогенеза при COVID-19.
Внимание клиницистов разных стран мира привлекают методы неинвазивной электростимуляции мозга. Последние могут быть классифицированы на стимуляцию постоянным током (transcranial direct current stimulation, tDCS), переменным током (transcranial alternating current stimulation, tACS) и импульсным током (transcranial pulsed current stimulation, tPCS) [4]. Транскраниальная электростимуляция (ТЭС-терапия), разработанная под руководством В. П. Лебедева, сочетает импульсный и постоянный компоненты, хотя в зарубежной литературе ее нередко относят к tPCS; встречается также обозначение «Lebedev’s currents» (токи Лебедева) [4][5]. Транскраниальная электростимуляция активно изучается в разных контекстах отечественными и зарубежными учеными [5–8]. Однако исследования, посвященные ее эффектам при острой коронавирусной инфекции, в настоящее время неизвестны. Того же нельзя сказать про другие методы неинвазивного воздействия электрическим током на нервную систему. Так, T. P. Pinto et al. (2023) изучили эффекты однократного сеанса tDCS (величина тока до 2 мА) у 20 пациентов, госпитализированных в связи с острой инфекцией, вызванной вирусом SARS-CoV-2, в возрасте от 18 до 80 лет, без признаков крайне тяжелого течения. Авторы показали, во-первых, безопасность и отсутствие серьезных побочных явлений (как связанных с собственно инфекцией, так и прочих), а во-вторых, обнаружили ряд благоприятных эффектов процедуры. По сравнению с 20 пациентами группы контроля (без tDCS) наблюдались нормализация вариабельности сердечного ритма (что исследователи связывают с модуляцией автономной регуляции сердца) и увеличение сатурации [9]. Следует подчеркнуть, что эти явления наблюдались после единственного сеанса процедуры. В другой работе, S. M. Andrade et al. (2022), приняли участие 56 пациентов палаты интенсивной терапии, из которых 28 получали tDCS (до 3 мА) дважды в день в течение 10 дней. Побочные эффекты не отличались между группами стимуляции и контроля. В группе tDCS при этом было больше дней без искусственной вентиляции легких (первичная конечная точка) и наблюдалась более выраженная положительная динамика показателей органной недостаточности (шкала SOFA (Sequential Organ Failure Assessment)) [10]. Больший массив работ посвящен применению методов электростимуляции для коррекции отдаленных последствий инфекции, включая длительный COVID (long COVID) [11]. На этапе реабилитации особое значение приобретают стресс-лимитирующий, анксиолитический и антиноцицептивный эффекты этих методов. Некоторые из таких работ посвящены и ТЭС-терапии [12].
Для объяснения благоприятных эффектов неинвазивного воздействия электрическим током на нервную систему предлагается ряд объяснений. Во-первых, это модуляция работы центров мозга, участвующих среди прочего в регуляции дыхания, гемодинамики и иммунитета [13]. Так, например, известна роль парасимпатической нервной системы в ингибировании чрезмерного иммунного ответа; напротив, симпатоадреналовая гиперактивация (характерная для многих критических состояний) неблагоприятно воздействует на сердечно-сосудистую систему, реологию крови (способствуя тромбообразованию), метаболизм, терморегуляцию, потенцирует эндотелиальную дисфункцию, воспаление и т. д. [13]. Обсуждается предположение о том, что «симпатический (адренергический) шторм» играет важную роль в развитии нейрогенного отека легких и дыхательной недостаточности, аналогично тому, как это происходит при других критических состояниях [14][15]. Сочетание стресс-ассоциированной кардиомиопатии такоцубо и COVID-19 также может быть обусловлено гиперсимпатикотонией и гиперкатехоламинемией наряду с другими механизмами [16].
В контексте ТЭС-терапии, которая ранее показала свое благоприятное воздействие при различных нозологиях, в качестве важного механизма действия обсуждается стимуляция антиноцицептивных структур мозга: эндорфинергических, серотонинергических, дофаминергических, — которые выполняют разнообразные функции за пределами подавления боли, включая иммуномодуляцию и ингибирование реакции стресса [7][17][18]. Так, ранее была показана способность ТЭС-терапии снижать концентрацию ряда провоспалительных веществ в крови, например ИЛ-1β, фактора некроза опухолей (ФНО), ИЛ-6, ИЛ-2 [18][19]. Подобные эффекты были описаны как у лабораторных животных на моделях разнообразных патологий, так и в клиническом контексте у пациентов с воспалительными заболеваниями микробной и немикробной этиологии [18–20].
Опираясь на эти данные, сформулирована гипотеза, что ТЭС-терапия в комплексном лечении новой коронавирусной инфекции (COVID-19) может оказать дополнительный саногенный эффект, подавляя гиперпродукцию провоспалительных цитокинов. В дополнение к этому информативной является оценка лабораторных показателей острофазного ответа — С-реактивного белка (СРБ) и ферритина [21][22]. Ферритин к тому же отражает выраженность цитолиза и дисбаланса системного ответа железа [22]. Таким образом, авторы считают обоснованным изучение эффекта ТЭС-терапии в отношении данных показателей для интегративной оценки возможности применения метода в комплексном патогенетическом лечении обсуждаемого заболевания.
Цель исследования — оценка влияния транскраниальной электростимуляции на концентрацию интерлейкина-1β, С-реактивного белка и ферритина в крови у пациентов с новой коронавирусной инфекцией (COVID-19) среднетяжелого и тяжелого течения, не получающих таргетной противоцитокиновой терапии.
МЕТОДЫ
Дизайн исследования
Рандомизированное проспективное исследование проведено у 35 пациентов с новой коронавирусной инфекцией (COVID-19) среднетяжелого и тяжелого течения, проходивших лечение в отделении № 3 для взрослого населения с новой коронавирусной инфекцией COVID-19, не нуждающихся в проведении искусственной вентиляции легких, государственного бюджетного учреждения здравоохранения «Краевая клиническая больница № 2» Министерства здравоохранения Краснодарского края (ГБУЗ «ККБ № 2»).
Критерии соответствия
Критерии включения
Течение заболевания — среднетяжелое и тяжелое согласно критериям «Временных методических рекомендаций: профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)» Министерства здравоохранения Российской Федерации, актуальных в период пребывания пациента в стационаре (версий 11–151). Положительная динамика клинических и лабораторных показателей на фоне стандартной терапии в первые два дня лечения (по этой причине пациентам не назначалась дополнительная антицитокиновая терапия). Возраст пациентов от 18 до 70 лет. Информированное добровольное согласие от участников.
Критерии невключения
Наличие бактериальной коинфекции или подозрение на нее. Наличие декомпенсированных хронических заболеваний. Наличие противопоказаний к ТЭС-терапии.
Критерии исключения
Прерывание ТЭС-терапии по желанию пациента. Необходимость добавить к лечению любую специфическую противоцитокиновую терапию. Присоединение бактериальной коинфекции или подозрение на нее.
Условия проведения
Работа производилась в государственном бюджетном учреждении здравоохранения «Краевая клиническая больница № 2» Министерства здравоохранения Краснодарского края; в федеральном государственном бюджетном образовательном учреждении высшего образования «Кубанский государственный медицинский университет» Министерства здравоохранения Российской Федерации (ФГБОУ ВО КубГМУ Минздрава России), кафедра общей и клинической патологической физиологии.
Продолжительность исследования
Общая продолжительность исследования составила 9 месяцев (июнь 2021 г. — февраль 2022 г.). Общая продолжительность наблюдения за пациентами составила первые 7 дней госпитализации.
Описание медицинского вмешательства
Верификация диагноза COVID-19 осуществлялась методами амплификации нуклеиновых кислот, идентифицирующими РНК вируса SARS-CoV-2. Тяжесть заболевания определялась в соответствии с Временными методическими рекомендациями Министерства здравоохранения Российской Федерации (версий 11–152).
Современное стандартное лечение в соответствии с упомянутыми выше рекомендациями, во-первых, включало глюкокортикоидные препараты в стартовой максимальной дозе, эквивалентной 20 мг/сутки дексаметазона, с последующим снижением дозы на 20–25 % на введение/сутки в первые 2 суток, далее — на 50 % каждые 1–2 суток до отмены3. Во-вторых, пациенты получали антикоагулянтные препараты (низкомолекулярные гепарины): эноксапарин натрия в дозе 40 анти-Ха МЕ подкожно 1 раз в сутки, либо далтепарин натрия, либо надропарин кальция в эквивалентных дозах (в зависимости от возможностей аптеки); пациенты с индексом массы тела более 30 кг/м² получали 80 анти-Ха МЕ эноксапарина.
Процедура транскраниальной электростимуляции проводилась в положении лежа с использованием импульсного тока прямоугольной формы. Параметры стимуляции: длительность импульса — 3,75 ± 0,25 мс, сила тока — 3 мА, частота — 77 Гц. Электроды размещались на коже лба и в области сосцевидных отростков. Первый сеанс длился 15 минут и носил адаптационный характер. Последующие процедуры проводились по 45 минут ежедневно в течение 6 дней (1 сеанс в день).
Исходы исследования
Основной исход исследования
Динамика концентрации ИЛ-1β, СРБ и ферритина в крови в двух временных точках: в день поступления в COVID-отделение и к концу первой недели лечения.
Дополнительные исходы исследования
Не оценивались.
Методы регистрации исходов
Забор биологического материала (венозной крови) осуществлялся при поступлении в COVID-отделение и на 7‑е сутки госпитализации.
Отделение сыворотки осуществлялось центрифугированием венозной крови в течение 10 минут при частоте 3000 об/мин.
Определение лабораторных показателей
Сывороточная концентрация IL-1β определялась методом иммуноферментного анализа с использованием тест-системы «Интерлейкин-1 бета-ИФА-БЕСТ» (артикул А-8766; АО «Вектор-Бест», Россия) в соответствии с инструкцией производителя. Единицы измерения — пг/мл; аналитическая чувствительность — <1 пг/мл.
Концентрация СРБ оценивалась турбидиметрическим методом на анализаторе Architect c8000 (Abbott, США) с использованием набора «CRP Vario» (Abbott Laboratories, США). Единицы измерения — мг/л; аналитическая чувствительность — 0,2 мг/л, диапазон измерений — 0,2–320 мг/л.
Концентрация ферритина определялась методом иммунохемилюминесценции на микрочастицах с использованием анализатора Architect i2000 (Abbott, США) и набора «ARCHITECT Ferritin 7K59» (Abbott Laboratories, США) согласно протоколу производителя. Единицы измерения — нг/мл; аналитическая чувствительность — <1 нг/мл.
Изучаемые клинико-анамнестические характеристики
В качестве дополнительных переменных учитывались: наличие коморбидных состояний (сахарный диабет, артериальная гипертензия, хроническая обструктивная болезнь легких, ожирение при индексе массы тела ≥30 кг/м²); особенности сопутствующей терапии (прием ингибиторов ангиотензинпревращающего фермента — ИАПФ, антагонистов рецепторов ангиотензина II — АРА, статинов, метформина).
Оценка переносимости транскраниальной электростимуляции
Также регистрировались индивидуальные реакции пациентов на проведение процедуры ТЭС (субъективный дискомфорт, нарушения сна, головная боль и др.) с последующей качественной оценкой переносимости метода.
Рандомизация
В исследование были приглашены 57 пациентов, соответствующих критериям включения. Персональные данные пациентов (возраст, пол, анамнез заболевания, сведения о сопутствующих патологиях и др.) вносились в электронные таблицы Microsoft Excel (Microsoft, США). Каждому участнику присваивался уникальный идентификационный номер, не связанный с его персональными данными.
Рандомизация проводилась с использованием встроенной функции генерации случайных чисел =RAND () в Microsoft Excel, обеспечивающей равновероятное распределение участников по двум группам: группа ТЭС-терапии (n = 28), получавшая в дополнение к стандартному лечению транскраниальную электростимуляцию; группа сравнения (n = 29), получавшая только стандартное лечение.
В течение исследования осуществлялся ежедневный мониторинг клинического состояния пациентов и динамики течения COVID-19. При ухудшении состояния, развитии бактериальной коинфекции либо необходимости назначения специфической противоцитокиновой терапии пациент исключался из исследования.
В итоговый статистический анализ были включены данные 35 пациентов: 15 в группе ТЭС-терапии и 20 в группе сравнения.
Обеспечение анонимности данных
Получение и последующая обработка данных пациентов проводились обезличенно. Распределение пациентов на группы и анализ результатов проводился авторами без привлечения сторонних лиц.
Статистический анализ
Принципы расчета размера выборки
Предварительный расчет размера выборки не проводился, поскольку исследование имело пилотный (разведочный) характер, направленный на оценку тенденций изменений концентрации интерлейкина-1β, С-реактивного белка и ферритина при применении транскраниальной электростимуляции у пациентов с COVID-19. Полученные результаты предполагались как основание для планирования последующих исследований с априорным определением мощности выборки и расчетом необходимого числа участников.
Методы статистического анализа данных
Анализ и визуализация данных выполнены в среде4 R [23]. Нормальность распределения количественных данных проверялась с помощью критерия Шапиро — Уилка. Так как большинство параметров не подчинялось нормальному распределению, описательная статистика представлена в виде Me (Q1; Q3) — медианы и квартилей.
Межгрупповое сравнение количественных показателей (группа ТЭС против группы сравнения) выполнялось с использованием критерия Манна — Уитни. Для оценки размера эффекта межгрупповых различий применялась оценка вероятности превосходства (probability of superiority, PS) с помощью пакета Rcompanion5 [24].
Интерпретация PS:
— PS = 0,5 — отсутствие различий (эквивалентность групп);
— PS → 0 или PS → 1 — максимальный размер эффекта (вероятность того, что значение показателя в одной группе выше, чем в другой, стремится к 0 или 100 %).
Оценка внутригрупповой динамики (до и после лечения) проводилась с использованием критерия Вилкоксона в модификации Пратта (Wilcoxon signed-rank test with Pratt correction) с применением пакета Coin [25].
Размер эффекта для зависимых выборок выражался в виде рангового бисериального коэффициента корреляции (matched-pairs rank biserial correlation coefficient, rc), рассчитанного с использованием пакета Rcompanion.
Интерпретация rc [26][27]:
— |rc| < 0,1 — пренебрежимо малый эффект,
— 0,1 ≤ |rc| < 0,3 — малый эффект,
— 0,3 ≤ |rc| < 0,5 — средний эффект,
— |rc| ≥ 0,5 — крупный эффект.
Различия считались статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
Участники исследования
В период с 24.06.2021 по 23.02.2022 в исследование были приглашены 57 пациентов. Случайным образом из них были сформированы 2 группы исследования: группа ТЭС-терапии (n = 28), получавшая в дополнение к стандартному лечению транскраниальную электростимуляцию, и группа сравнения (n = 29), получавшая стандартное лечение. При проведении ежедневного мониторинга течения коронавирусной инфекции COVID-19 из исследования было исключено 13 человек из группы ТЭС-терапии (из них антицитокиновая терапия понадобилась 12 пациентам, один был исключен из-за присоединения бактериальной коинфекции), и 9 человек из группы сравнения (необходимость проведения антицитокиновой терапии). Таким образом, окончательный анализ данных осуществлялся у 15 пациентов в группе ТЭС-терапии и 20 пациентов в группе сравнения (блок-схема дизайна исследования, рис. 1).
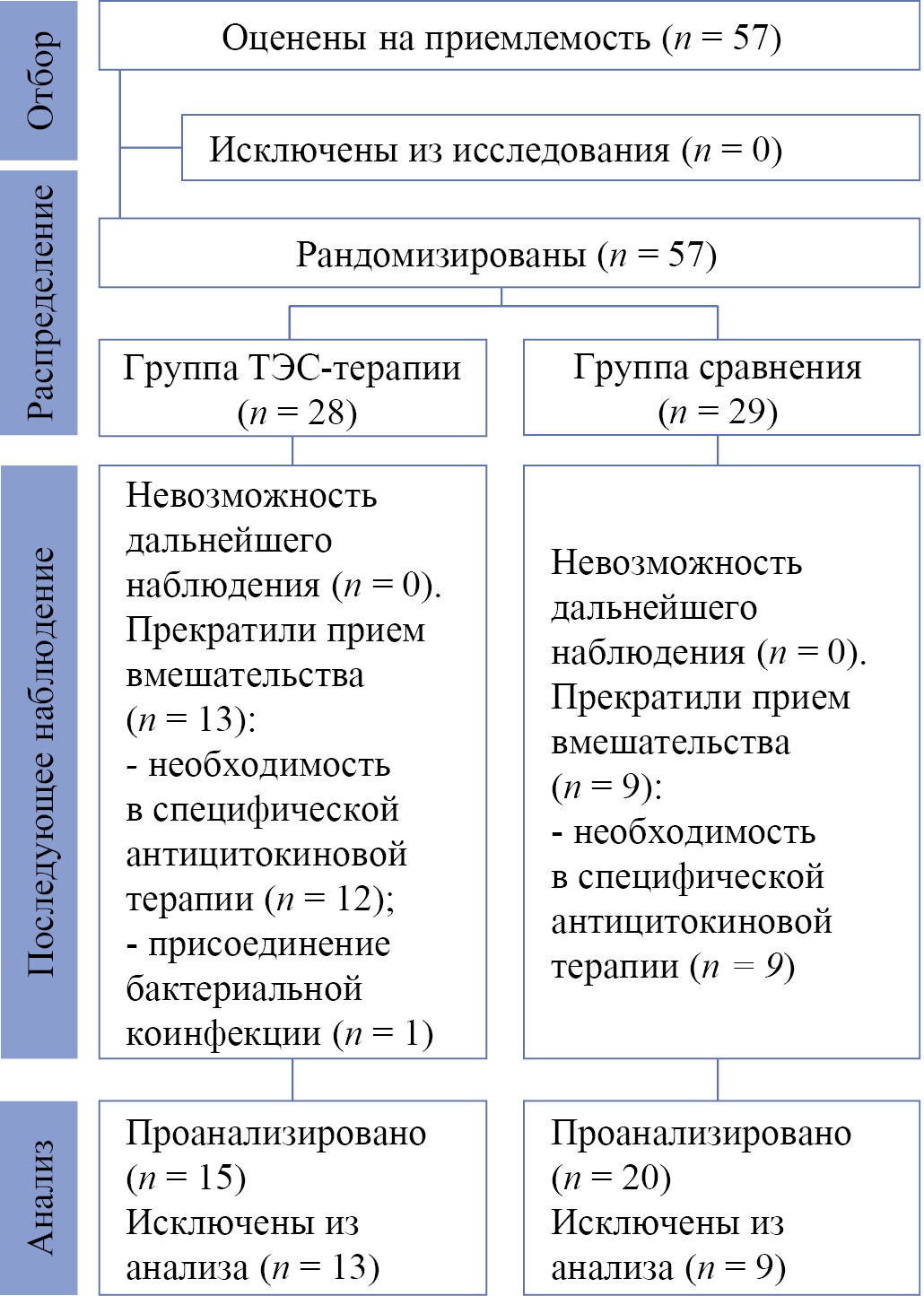
Рис. 1. Блок-схема дизайна исследования
Примечание: блок-схема выполнена авторами (согласно рекомендациям CONSORT). Сокращение: ТЭС — транскраниальная электростимуляция.
Fig. 1. Block diagram of the study design
Note: The block diagram was created by the authors (as per CONSORT recommendations). Abbreviation: ТЭС — transcranial electrical stimulation.
У всех пациентов было среднетяжелое течение при поступлении, за исключением двух пациентов из группы сравнения. При поступлении степень тяжести у них была оценена как тяжелая на основании сатурации (92 и 90 %). После первого дня лечения сатурация стабильно превышала 93 %, соответствуя критерию среднетяжелого течения (табл.).
Таблица. Демографические, антропометрические и клинико-анамнестические показатели пациентов исследуемых групп
Table. Demographic, anthropometric, and clinical history characteristics of patients in the study groups
|
Параметр |
Группа сравнения (n = 20) |
Группа ТЭС-терапии (n = 15) |
Уровень статистической значимости различий¹, р |
|
Возраст, лет; Me (Q1; Q3) |
41,5 (34,7; 54,5) |
48 (36,0; 55,5) |
0,10 (КМУ) |
|
Пол, абс. (%) |
|||
|
Женщины |
11 (55 ) |
6 (40 ) |
0,38 (КФ) |
|
Мужчины |
9 (45 ) |
9 (60 ) |
|
|
Степень тяжести при поступлении, абс. (%) |
|||
|
Среднетяжелое |
18 (90 ) |
15 (100 ) |
0,21 (КФ) |
|
Тяжелое |
2 (10 ) |
- |
|
|
Терапия основного заболевания |
|||
|
Глюкокортикоиды, абс. (%) |
19 (95 ) |
14 (93,3 ) |
0,83 (КФ) |
|
Антикоагулянты, абс. (%) |
20 (100 ) |
15 (100 ) |
- |
|
Сопутствующие нозологии |
|||
|
Сахарный диабет, абс. (%) |
2 (10 ) |
0 (0 ) |
0,21 (КФ) |
|
Индекс массы тела, превышающий 30 кг/м², абс. (%) |
1 (5 ) |
1 (6,7 ) |
0,83 (КФ) |
|
Артериальная гипертензия, абс. (%) |
6 (30 ) |
2 (13,3 ) |
0,25 (КФ) |
|
Хроническая обструктивная болезнь легких, абс. (%) |
0 (0 ) |
0 (0 ) |
- |
|
Терапия сопутствующих заболеваний |
|||
|
Прием иАПФ или АРА, абс. (%) |
0 (0 ) |
1 (6,7 ) |
0,24 (КФ) |
|
Прием статинов, абс. (%) |
0 (0 ) |
0 (0 ) |
- |
|
Прием метформина, абс. (%) |
0 (0 ) |
0 (0 ) |
- |
|
Исходные уровни изучаемых лабораторных показателей крови |
|||
|
ИЛ-1β, пг/мл; Me (Q1; Q3) |
1,7 (1,1; 2,9) |
2,4 (1,0; 3,7) |
0,70 (КМУ) |
|
С-реактивный белок, мг/л; Me (Q1; Q3) |
55,2 (17,9; 67,6) |
46,1 (26,7; 85,5) |
0,90 (КМУ) |
|
Ферритин, нг/мл; Me (Q1; Q3) |
316,0 (212,3; 433,0) |
349,8 (156,4; 567,9) |
0,80 (КМУ) |
Примечания: таблица составлена авторами; ¹ КМУ — критерии Манна — Уитни, КФ — точный критерий Фишера. Сокращения: АРА — антагонисты рецепторов к ангиотензину II, иАПФ — ингибиторы ангиотензинпревращающего фермента, ТЭС — транскраниальная электростимуляция.
Notes: The table was compiled by the authors; ¹ КМУ — Mann—Whitney U test, КФ — Fisher’s exact test. Abbreviations: АРА — angiotensin II receptor blockers; иАПФ — angiotensin-converting enzyme inhibitors; ТЭС — transcranial electrical stimulation.
Таким образом, две группы пациентов, включенных в работу, были сопоставимы по основному исследованному показателю в дополнение к их сопоставимости по степени тяжести основного заболевания, демографическим показателям, коморбидности, терапии сопутствующих патологий и стандартному лечению собственно инфекции (согласно действующим на момент госпитализации временным методическим рекомендациям: профилактике, диагностике и лечению новой коронавирусной инфекции (COVID-19) (табл.).
Основные результаты исследования
Сывороточная концентрация ИЛ-1β до начала лечения в группе транскраниальной электростимуляции и в группе сравнения представлена на рисунке 2 (1‑е измерение). Медиана данного показателя в группе транскраниальной электростимуляции: 2,4 (1,0; 3,7) пг/мл — была несколько выше (на 41,2 %), чем в группе сравнения: 1,7 (1,1; 2,9) пг/мл, однако при этом различие между группами не было статистически значимым (p = 0,7; размер эффекта — PS = 0,5, (95 % доверительный интервал (ДИ) от 0,3 до 0,7)).
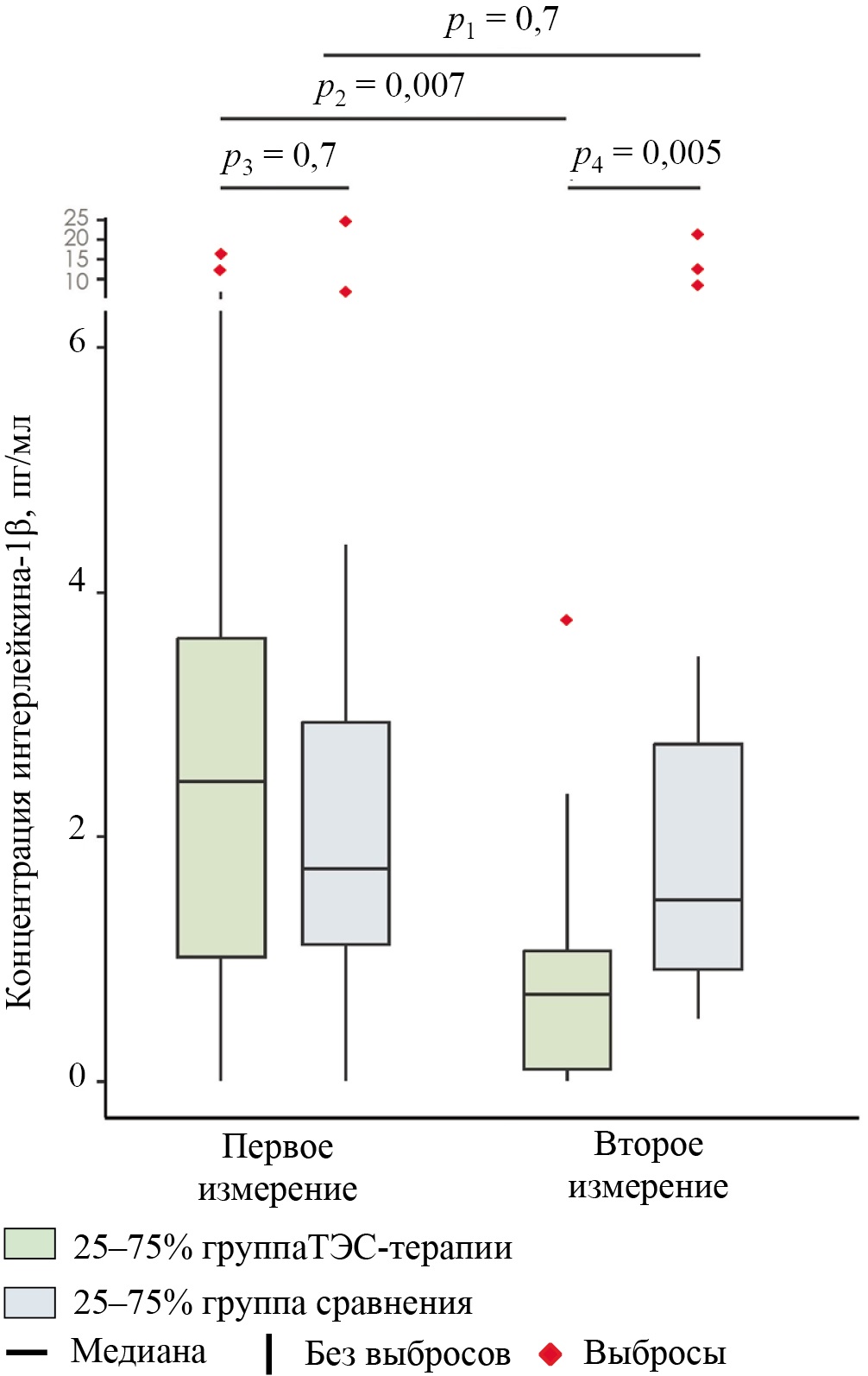
Рис. 2. Значение медиан сывороточной концентрации интерлейкина-1β, 1‑е (первое измерение) и 7‑е (второе измерение) сутки госпитализации в исследуемых группах
Примечание: рисунок выполнен авторами. Обозначения уровней значимости: p1 — уровень значимости различий в группе ТЭС-терапии между 1-м и 7-м сутками (внутригрупповое сравнение); p2 — уровень значимости различий в группе сравнения между 1-м и 7-м сутками (внутригрупповое сравнение); p3 — уровень значимости различий между группами (ТЭС-терапия и сравнение) до начала лечения (1‑е сутки); p4 — уровень значимости различий между группами (ТЭС-терапия и сравнение) на 7‑е сутки госпитализации. Пояснение: Внутригрупповые сравнения (p1, p2) выполнены с помощью критерия Вилкоксона с поправкой Пратта (для зависимых выборок). Межгрупповые сравнения (p3, p4) — с помощью критерия Манна — Уитни (для независимых выборок). Размер эффекта при межгрупповом сравнении выражен через probability of superiority (PS), а при внутригрупповом — через ранговый бисериальный коэффициент корреляции (rc). Сокращение: ТЭС — транскраниальная электростимуляция.
Fig. 2. Median serum levels of interleukin-1β in the study groups at days 1 (first measurement) and 7 (second measurement) of hospitalization
Note: The figure was created by the authors. Significance levels: p1 — significance level of differences between days 1 and 7 in the group receiving transcranial electrical stimulation (intra-group comparison); p2 — significance level of differences between days 1 and 7 in the comparison group (intra-group comparison); p3 — significance level of differences between the comparison group and the group receiving transcranial electrical stimulation before treatment (day 1); p4 — significance level of differences between the comparison group and the group receiving transcranial electrical stimulation at day 7 of stay. The intragroup comparisons (p1, p2) were performed using the Wilcoxon test with Pratt correction (for dependent samples). The intergroup comparisons (p3, p4) were performed using the Mann—Whitney U test (for independent samples). In the intergroup comparison, the effect size is expressed in terms of the probability of superiority (PS), whereas in the intragroup comparison, it is expressed in terms of the rank-biserial correlation coefficient (rc). Abbreviation: ТЭС — transcranial electrical stimulation.
При изучении динамики концентрации обсуждаемого показателя в группе сравнения (рис. 2; 2‑е измерение) отмечается незначимая статистически тенденция к снижению с 1,7 (1,1; 2,9) пг/мл до 1,5 (0,9; 2,8) пг/мл (на 11,8 %) (p = 0,7; размер эффекта — rc = 0,09 (95 % ДИ от –0,4 до 0,6)) к 7-му дню госпитализации.
Напротив, в группе транскраниальной электростимуляции к моменту второго измерения (рис. 2) концентрация ИЛ-1β составила 0,7 (0,1; 1,1) пг/мл, таким образом, снизившись на 70,8 % от исходного уровня (2,4 (1,0; 3,7) пг/мл) (p = 0,007; размер эффекта — rc = 0,8 (95 % ДИ 0,4–1)). При сравнении между группами к концу периода наблюдения в группе транскраниальной электростимуляции изучаемый показатель был меньше на 53,3 % (1,5 (0,9; 2,8) пг/мл в группе сравнения против 0,7 (0,1; 1,1) пг/мл в группе ТЭС-терапии) (p = 0,005; размер эффекта — PS = 0,2 (95 % ДИ 0,06–0,4)).
Применение транскраниальной электростимуляции было сопряжено с более выраженным снижением концентрации цитокина в крови, что, по-видимому, отражает антивоспалительный эффект данного лечебного метода. Так, уровень ИЛ-1β уменьшился у 12 пациентов из 15. Максимальное значение данного показателя в группе транскраниальной электростимуляции к моменту второго измерения составило 3,8 пг/мл (исходная концентрация у данного пациента была равна 12,3 пг/мл). В группе сравнения максимальная концентрация цитокина была равна 20,9 пг/мл (исходный показатель у данного пациента — 7,1 пг/мл). Среди трех пациентов группы транскраниальной электростимуляции, у которых концентрация цитокина возросла, максимальное ее значение при втором измерении равнялось 3,7 пг/мл
Концентрация СРБ до начала лечения (рис. 3) в группе сравнения составила 55,2 (17,9; 67,6) мг/л, тогда как в группе транскраниальной электростимуляции — 46,1 (26,7; 85,5) мг/л. Межгрупповые различия на исходном этапе были статистически незначимыми (p = 0,9; размер эффекта — probability of superiority (PS) = 0,5; 95 % ДИ: 0,288–0,719).Таким образом, у обеих групп пациентов наблюдался выраженный избыток С-реактивного белка относительно стандартного референсного интервала 0–5 мг/л6. Подобный гиперсинтез белка острой фазы характерен для новой коронавирусной инфекции (COVID-19) и широко используется как показатель тяжести воспаления, необходимости коррекции терапии и прогноза [21].

Рис. 3. Значение медиан концентрации С-реактивного белка, 1‑е (первое измерение) и 7‑е сутки (второе измерение) госпитализации в исследуемых группах
Примечание: рисунок выполнен авторами. Обозначения уровней значимости: p1 — уровень значимости различий в группе ТЭС-терапии между 1-м и 7-м сутками (внутригрупповое сравнение); p2 — уровень значимости различий в группе сравнения между 1-м и 7-м сутками (внутригрупповое сравнение); p3 — уровень значимости различий между группами (ТЭС-терапия и сравнение) до начала лечения (1‑е сутки); p4 — уровень значимости различий между группами (ТЭС-терапия и сравнение) на 7‑е сутки госпитализации. Пояснение: Внутригрупповые сравнения (p1, p2) выполнены с помощью критерия Вилкоксона с поправкой Пратта (для зависимых выборок). Межгрупповые сравнения (p3, p4) — с помощью критерия Манна — Уитни (для независимых выборок). Размер эффекта при межгрупповом сравнении выражен через probability of superiority (PS), а при внутригрупповом — через ранговый бисериальный коэффициент корреляции (rc). Сокращение: ТЭС — транскраниальная электростимуляция.
Fig. 3. Median serum levels of C-reactive protein in the study groups at days 1 (first measurement) and 7 (second measurement) of hospitalization
Note: The figure was created by the authors. Significance levels: p1 — significance level of differences between days 1 and 7 in the group receiving transcranial electrical stimulation (intra-group comparison); p2 — significance level of differences between days 1 and 7 in the comparison group (intra-group comparison); p3 — significance level of differences between the comparison group and the group receiving transcranial electrical stimulation before treatment (day 1); p4 — significance level of differences between the comparison group and the group receiving transcranial electrical stimulation at day 7 of stay. The intragroup comparisons (p1, p2) were performed using the Wilcoxon test with Pratt correction (for dependent samples). The intergroup comparisons (p3, p4) were performed using the Mann–Whitney U test (for independent samples). In the intergroup comparison, the effect size is expressed in terms of the probability of superiority (PS), whereas in the intragroup comparison, it is expressed in terms of the rank-biserial correlation coefficient (rc). Abbreviation: ТЭС — transcranial electrical stimulation.
К моменту второго измерения концентрация С-реактивного белка в группе сравнения составила 3,4 (1,5; 5,7) мг/л, что соответствует снижению уровня данного маркера на 93,8 % относительно исходного значения (55,2 (17,9; 67,6) мг/л) (p = 0,0003; размер эффекта — ранговый бисериальный коэффициент корреляции rc = 0,95; 95 % ДИ: 0,8–1). В группе транскраниальной электростимуляции концентрация С-реактивного белка на 7‑е сутки составила 3,3 (2,2; 5,5) мг/л, что отражает снижение показателя на 92,8 % по сравнению с исходным уровнем (46,1 (26,7; 85,5) мг/л) (p = 0,0006; размер эффекта — rc = 1). При межгрупповом сравнении на 7‑е сутки концентрация данного маркера воспалительной реакции статистически значимо не различалась (p = 0,6; probability of superiority PS = 0,5; 95 % ДИ: 0,3–0,7). У всех пациентов группы транскраниальной электростимуляции наблюдалась положительная динамика показателя. В группе сравнения снижение С-реактивного белка зарегистрировано у 19 из 20 пациентов; у одного участника концентрация белка острой фазы увеличилась с 14,6 до 31 мг/л. Полученные результаты свидетельствуют о выраженном снижении интенсивности воспалительной реакции в обеих группах к 7-му дню наблюдения, что может рассматриваться как благоприятный прогностический признак при новой коронавирусной инфекции (COVID-19). Однако следует учитывать, что, согласно литературным данным, возможен вторичный (поздний) пик повышения С-реактивного белка, возникающий после 11-х суток заболевания, что может затруднять оценку тяжести и выбор оптимальной тактики лечения [21].
Уровень ферритина (рис. 4) в группе сравнения до лечения составил 316 (212,3; 433) нг/мл. В группе транскраниальной электростимуляции данный показатель был сопоставим и составлял 349,8 (156,4; 567,9) нг/мл. При сравнении между группами до начала лечения статистически значимых различий не выявлено (p = 0,8; PS = 0,45). Следует отметить, что в обеих группах концентрация ферритина была повышена относительно референсных значений (21,8–274,6 нг/мл7). Повышенный уровень ферритина широко рассматривается в литературе как значимый диагностический и прогностический биомаркер при новой коронавирусной инфекции (COVID-19) [22]. Гиперферритинемия отражает совокупность патологических процессов, индуцируемых инфекцией: и как усиленный синтез ферритина гепатоцитами в ответ на действие провоспалительных цитокинов (в первую очередь ИЛ-6), и как по меньшей мере два дополнительных механизма, которые будут подробно рассмотрены далее.

Рис. 4. Значение медиан концентрации ферритина, 1‑е (первое измерение) и 7‑е сутки (второе измерение) госпитализации в исследуемых группах.
Примечание: рисунок выполнен авторами. Обозначения уровней значимости: p1 — уровень значимости различий в группе ТЭС-терапии между 1-м и 7-м сутками (внутригрупповое сравнение); p2 — уровень значимости различий в группе сравнения между 1-м и 7-м сутками (внутригрупповое сравнение); p3 — уровень значимости различий между группами (ТЭС-терапия и сравнение) до начала лечения (1‑е сутки); p4 — уровень значимости различий между группами (ТЭС-терапия и сравнение) на 7‑е сутки госпитализации. Пояснение: Внутригрупповые сравнения (p1, p2) выполнены с помощью критерия Вилкоксона с поправкой Пратта (для зависимых выборок). Межгрупповые сравнения (p3, p4) — с помощью критерия Манна — Уитни (для независимых выборок). Размер эффекта при межгрупповом сравнении выражен через probability of superiority (PS), а при внутригрупповом — через ранговый бисериальный коэффициент корреляции (rc). Сокращение: ТЭС — транскраниальная электростимуляция.
Fig. 4. Median serum levels of ferritin in the study groups at days 1 (first measurement) and 7 (second measurement) of hospitalization
Note: The figure was created by the authors. Significance levels: p1 — significance level of differences between days 1 and 7 in the group receiving transcranial electrical stimulation (intra-group comparison); p2 — significance level of differences between days 1 and 7 in the comparison group (intra-group comparison); p3 — significance level of differences between the comparison group and the group receiving transcranial electrical stimulation before treatment (day 1); p4 — significance level of differences between the comparison group and the group receiving transcranial electrical stimulation at day 7 of stay. The intragroup comparisons (p1, p2) were performed using the Wilcoxon test with Pratt correction (for dependent samples). The intergroup comparisons (p3, p4) were performed using the Mann–Whitney U test (for independent samples). In the intergroup comparison, the effect size is expressed in terms of the probability of superiority (PS), whereas in the intragroup comparison, it is expressed in terms of the rank-biserial correlation coefficient (rc). Abbreviation: ТЭС — transcranial electrical stimulation.
При повторном измерении концентрация ферритина в группе сравнения составила 361,5 (286,7; 498,4) нг/мл. По сравнению с исходным уровнем медиана показателя увеличилась на 14,4 % (исходный уровень — 316 (212,3; 433) нг/мл), однако изменения не достигли статистической значимости (p = 0,6; rc = 0,2). В группе транскраниальной электростимуляции данный показатель также возрос и составил 387,9 (192,5; 563) нг/мл. Прирост медианы к концу первой недели составил 10,9 % (исходный уровень — 349,8 (156,4; 567,9) нг/мл) и также не был статистически значимым (p = 0,7; rc = 0,2). При межгрупповом сравнении в этой временной точке концентрация ферритина статистически значимо не различалась (p = 0,8; PS = 0,45).
В отличие от динамики С-реактивного белка, уровень ферритина повысился у значительной доли пациентов к концу первой недели лечения как в группе транскраниальной электростимуляции, так и в группе сравнения. Эти результаты могут косвенно указывать на патогенетическую значимость нарушения метаболизма железа и процессов цитолиза (см. обсуждение ниже), динамика которых не обязательно синхронизируется с течением воспалительной реакции.
Таким образом, добавление транскраниальной электростимуляции к стандартному лечению заболевания не приводило к увеличению концентрации ИЛ-1β, не провоцировало развития синдрома выброса цитокинов (рис. 2) и не утяжеляло лабораторные проявления острой фазовой реакции (табл.). Стандартная терапия, не включающая таргетного противоцитокинового вмешательства, оказывала слабое влияние на концентрацию ИЛ-1β (рис. 2). В группе стандартного лечения наблюдалось снижение концентрации С-реактивного белка, но не ферритина. В отличие от этого, добавление транскраниальной электростимуляции к стандартной терапии значительно влияло на динамику концентрации ИЛ-1β, которая превышала уровень 3 пг/мл лишь у одного пациента этой группы к концу наблюдения (рис. 2).
Дополнительные результаты исследования
Не получены.
Нежелательные явления
Летальные случаи отсутствовали в обеих группах. Нежелательных явлений, связанных с применением транскраниальной электростимуляции, не зарегистрировано.
ОБСУЖДЕНИЕ
Резюме основного результата исследования
В настоящем исследовании у пациентов, получавших стандартную терапию (без включения таргетных противоцитокиновых препаратов), не наблюдалось статистически значимого снижения концентрации ИЛ-1β в период наблюдения. Применение ТЭС-терапии не сопровождалось развитием осложнений у пациентов с новой коронавирусной инфекцией (COVID-19). В группе ТЭС-терапии отмечено выраженное снижение сывороточной концентрации ИЛ-1β. Уровень С-реактивного белка значительно снижался в обеих группах, тогда как положительная динамика концентрации ферритина отсутствовала.
Обсуждение основного результата исследования
Гиперпродукция цитокинов лежит в основе синдрома выброса цитокинов при обсуждаемой инфекции [1]. Это явление неблагоприятно отражается на прогнозах пациентов и требует поиска путей лечебного воздействия. Среди ключевых провоспалительных цитокинов следует отметить ИЛ-1β, который играет главную роль в развертывании мальадаптивного иммунного ответа. В лабораторных исследованиях подтверждена способность вируса SARS-CoV-2 индуцировать сборку инфламмасомы, которая отвечает за частичный протеолиз (ферментом каспазой-1) проинтерлейкина-1β до активного ИЛ-1β (а также про-ИЛ-18 до ИЛ-18), приводя к его гиперпродукцию [2][3]. Механизм, по-видимому, включает непосредственную активацию функционально смежных белков (NLRP3, TRAF3, ASC) вирусными протеинами (нуклеокапсидным протеином (N), виропорином Orf3a) [2][28]. Кроме амплификации иммунного ответа описанные процессы оказывают иные цитопатические эффекты. Важный пример — активация гасдермина D (GSDMD), который повышает проницаемость клеточной мембраны, что является центральным событием в патогенезе запрограммированной клеточной гибели путем пирроптоза [2]. Последний, во-первых, дополнительно усугубляет жизнеугрожающую мультиорганную недостаточность. Во-вторых, разрушение клеток сопряжено с высвобождением тканевого тромбопластина и запуском прокоагулянтных каскадов. В дополнение к этому интерлейкин-1β способствует тромбовоспалению многообразными другими путями: стимулирует созревание мегакариоцитов, адгезию тромбоцитов, высвобождение нейтрофильных экстрацеллюлярных ловушек (что, в свою очередь, ведет к аутоактивации фактора Хагемана, подавляет антитромбин и ингибитор пути тканевого фактора), воздействует на эндотелий [3][29]. Последнее исключительно важно, так как активированный эндотелий, во-первых, сам становится источником цитокинов, эйкозаноидов, свободных радикалов, проагрегантных/прокоагулянтных субстанций (фактора фон Виллебранда), а продукция антикоагулянтов (тромбомодулина) ослабевает [3]. Во-вторых, эндотелиоциты усиленно экспрессируют адгезионные молекулы (P-селектины, межклеточные молекулы адгезии (intercellular adhesion molecule, ICAM), сосудистые молекулы адгезии (vascular cell adhesion molecule, VCAM)), к которым присоединяются поверхностные белки лейкоцитов, что ведет к активации последних [1][3].
Гиперпродукция ИЛ-1β (наряду с ФНО и ИЛ-6) является одним из главных механизмов в основе патогенеза реакции острой фазы, которая включает ряд системных эффектов воспаления (лихорадку, синтез острофазных протеинов/пептидов, системную перестройку обмена железа, стимуляцию лейкопоэза и стрессового селезеночного эритропоэза, пострецепторное подавление трансдукции сигнала от инсулинового рецептора и пр.) [1][30]. Сверхвысокий уровень данных цитокинов оказывает прямое цитопатическое системное действие на жизненно важные органы, дополнительно способствуя полиорганной недостаточности. Особую смежную проблему представляет вторичный гемофагоцитарный лимфогистиоцитоз (синдром активации макрофагов), сопряженный с «цитокиновым штормом» и дополнительно повреждающий органы [1].
C-реактивный белок и ферритин относятся к числу острофазных протеинов, а их продукция печенью стимулируется провоспалительными цитокинами (особенно ИЛ-6) [1][21][22]. Ферритин, однако, также является ключевым участником системного обмена железа. При воспалении данный обмен нарушается соответственно тяжести заболевания, что патогенетически связано с дисбалансом регуляторных субстанций (гепцидина, эритроферона, костного морфогенетического белка 6, фактора роста и дифференцировки 15), прямым воздействием цитокинов на красный костный мозг, системной дисфункцией CD163-позитивных клеток системы фагоцитирующих мононуклеаров [22][30–32]. Последние также являются источником гиперферритинемии при воспалении. Наконец, ферритин внутри клеток обеспечивает депонирование железа, следовательно, при цитолизе внеклеточное содержание данного белка растет [22]. Цитолиз же, в свою очередь, может быть обусловлен дыхательной, ишемической (например, вследствие тромбообразования) гипоксией тканей, цитопатическими эффектами вируса, медиаторов воспаления, прочих субстанций (например, катехоламинов в рамках «адренергического/симпатического шторма») при COVID-19 [33]. Таким образом, можно выделить не менее трех механизмов повышения концентрации ферритина вследствие воспаления.
Как мы показали в данной работе, стандартное лечение, включающее глюкокортикоидную терапию без таргетных противоцитокиновых препаратов, не воздействовало на сывороточную концентрацию ИЛ-1β и на концентрацию ферритина. Аналогичный результат воспроизводился и в других работах. Так, J. Alonso-Domínguez и соавт. (2023 г.) показали, что уровень IL-1β, ФНО и макрофагального воспалительного белка 1α (macrophage inflammatory protein, MIP-1α) может оставаться повышенным через месяц после начала инфекции [28]. Более того, такая динамика лишь этих трех показателей, но не остальных в длинном списке изучавшихся (ИЛ-3, ИЛ-6, ИЛ-8, ИЛ-18, интерферон-γ (ИФН-γ), ИФН-γ индуцируемый белок 10, ИФН-γ индуцируемый монокин (MIP) 1β) ассоциирована с риском долгосрочных последствий инфекции и длительного COVID-19 (long COVID-19). В качестве прогностического порогового уровня J. Alonso-Domínguez и соавт. (2023 г.) предлагают концентрацию IL-1β более 7,36 пг/мл. При этом прогностическая ценность данного показателя выше, чем концентрации ФНО и MIP-1α: площадь под характеристической кривой составляет 0,709 против 0,682 и 0,691 соответственно [28].
Как мы показали в настоящей работе, у пациентов группы сравнения наблюдалось выраженное снижение уровня СРБ к концу периода наблюдения, что, вероятно, объясняется успешной элиминацией возбудителя иммунной системой и эффектом лечения. Несоответствие динамики СРБ и ИЛ-1β спекулятивно можно объяснить ведущей ролью ИЛ-6 в стимуляции синтеза белков острой фазы. Интересным нам представляется изучить, как соотносятся динамика ИЛ-6 с изменениями СРБ и ИЛ-1β. Также мы предполагаем, что СРБ не может быть лабораторным отражением дисфункции ИЛ-1β (хотя клиническое значение этого не ясно). Уровень ферритина, как было указано выше, обусловлен совокупностью нескольких патологических процессов. В этом контексте было бы интересным сопоставление динамики данного показателя с изменениями концентрации ИЛ-6 (для оценки вклада острофазной реакции в возникновение гиперферритинемии) и маркеров цитолиза, например аминотрансфераз.
При добавлении ТЭС-терапии к стандартному лечению наблюдалось выраженное снижение концентрации ИЛ-1β (рис. 2). При этом в данной группе у всех пациентов с исходно высоким уровнем цитокина имело место выраженное снижение его уровня к концу первой недели. Лишь у нескольких пациентов с исходно низкой концентрацией ИЛ-1β она незначительно возросла, не превысив в итоге 1,2 пг/мл. Так же как и в группе сравнения, наблюдалось выраженное снижение СРБ, но не ферритина. Транскраниальная электростимуляция не провоцировала тяжелых осложнений, в частности синдрома выброса цитокинов. Подобные результаты, по нашему мнению, патогенетически обосновывают возможность дальнейшего изучения лечебного метода при новой коронавирусной инфекции.
Полученные данные сопрягаются с предшествующими работами, показавшими воздействие ТЭС-терапии на нейроиммуноэндокринную дисрегуляцию в животном эксперименте и в клинике. Данный эффект был изучен в контексте разнообразных патологий. Некоторые из исследований касались и влияния ТЭС-терапии на продукцию ИЛ-1β. В частности, применение метода благоприятно влияло на концентрацию цитокина у животных при моделирования тяжелого комбинированного стресса, острого нарушения мозгового кровообращения и пр. [19][34]. В клинических работах показана способность ТЭС-терапии снижать концентрацию ИЛ-1β у пациентов с ишемической болезнью сердца, острым панкреатитом, при реабилитации после лечения злокачественного новообразования [18][20].
Считается, что подобный эффект в первую очередь обусловлен активацией антиноцицептивных систем организма: опиоидергической (стимуляция продукции β-эндорфина), дофаминергической, серотонинергической [35][36]. Впрочем, функции данных систем выходят далеко за рамки подавления боли и включают, например, стресс-лимитирующий эффект, регуляцию энергетического обмена, иммунитета, оксидативного статуса [7][37]. Транскраниальная электростимуляция способствует эндогенной продукции β-эндорфина и оказывает ингибирующий эффект на гиперпродукцию провоспалительных медиаторов, как показала эта работа и ряд предшествующих.
Ограничения исследования
Количество участников было небольшим. Работа имеет патофизиологическую направленность, поэтому, согласно поставленным целям, не рассматривались клинические параметры, таким образом, клиническое значение снижения концентрации ИЛ-1β в группе транскраниальной электростимуляции неясно (особенно если учесть результаты испытаний таргетных препаратов против ИЛ-1β) [38][39].
ЗАКЛЮЧЕНИЕ
Применение ТЭС-терапии снижало сывороточную концентрацию ИЛ-1β у пациентов с новой коронавирусной инфекцией (COVID-19) среднетяжелого течения, не получавших таргетные противоцитокиновые препараты. Динамика концентрации С-реактивного белка и ферритина у данных пациентов, получавших ТЭС-терапию в дополнение к стандартному лечению, статистически значимо не отличалась от таковой у пациентов группы сравнения.
1. Министерство здравоохранения Российской Федерации. Временные методические рекомендации: профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19) COVID. Версия 11 (07.05.2021). Available: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/055/735/original/B%D0%9C%D0%A0_COVID-19.pdf
Министерство здравоохранения Российской Федерации. Временные методические рекомендации: профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 12 (21.09.2021). Available: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/058/075/original/%D0%92%D0%9C%D0%A0_COVID-19_V12.pdf
Министерство здравоохранения Российской Федерации. Временные методические рекомендации: профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 13 (14.10.2021). Available: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/058/211/original/BMP-13.pdf
Министерство здравоохранения Российской Федерации. Временные методические рекомендации: профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 14 (27.12.2021). Available: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/059/041/original/%D0%92%D0%9C%D0%A0_COVID-19_V14_27-12-2021.pdf
Министерство здравоохранения Российской Федерации. Временные методические рекомендации: профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 15 (22.02.2022). Available: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/059/392/original/%D0%92%D0%9C%D0%A0_COVID-19_V15.pdf
2. Там же.
3. Там же.
4. R Core Team. R: A Language and Environment for Statistical Computing. R Foundation for Statistical Computing, Vienna, Austria. 2024 Available: https://www.R-project.org/
5. Mangiafico S. rcompanion: Functions to Support Extension Education Program Evaluation. version 2.4.36. Rutgers Cooperative Extension. New Brunswick, New Jersey. 2024. Available: https://CRAN.R-project.org/package=rcompanion
6. Референсные значения, установленные лабораторией государственного бюджетного учреждения здравоохранения «Краевая клиническая больница № 2» Министерства здравоохранения Краснодарского края.
7. Референсные значения, установленные лабораторией государственного бюджетного учреждения здравоохранения «Краевая клиническая больница № 2» Министерства здравоохранения Краснодарского края.
Список литературы
1. Darif D, Hammi I, Kihel A, El Idrissi Saik I, Guessous F, Akarid K. The pro-inflammatory cytokines in COVID-19 pathogenesis: What goes wrong? Microb Pathog. 2021;153:104799. https://doi.org/10.1016/j.micpath.2021.104799
2. Bittner Z.A., Schrader M., George S.E., Amann R. Pyroptosis and Its Role in SARS-CoV-2 Infection. Cells. 2022;11(10):1717. https://doi.org/10.3390/cells11101717
3. Potere N, Abbate A, Kanthi Y, Carrier M, Toldo S, Porreca E, Di Nisio M. Inflammasome Signaling, Thromboinflammation, and Venous Thromboembolism. JACC Basic Transl Sci. 2023;8(9):1245–1261. https://doi.org/10.1016/j.jacbts.2023.03.017
4. Moreno-Duarte I, Gebodh N, Schestatsky P, Guleyupoglu B, Reato D, Bikson M, Fregni F. Transcranial Electrical Stimulation: Transcranial Direct Current Stimulation (tDCS), Transcranial Alternating Current Stimulation (tACS), Transcranial Pulsed Current Stimulation (tPCS), and Transcranial Random Noise Stimulation (tRNS). In: Cohen Kadosh R., editor. The Stimulated Brain: сognitive Enhancement Using Non-Invasive Brain Stimulation. 2014;35–59. https://doi.org/10.1016/B978-0-12-404704-4.00002-8
5. Shen Y, Liu J, Zhang X, Wu Q, Lou H. Experimental study of transcranial pulsed current stimulation on relieving athlete’s mental fatigue. Front Psychol. 2022;13:957582. https://doi.org/10.3389/fpsyg.2022.957582
6. Тарасова Д.Н., Скворцов В.В., Левитан Б.Н. Транскраниальная электростимуляция в терапии язвенной болезни желудка и двенадцатиперстной кишки. Лечащий Врач. 2024;27(2):21–24. https://doi.org/10.51793/OS.2024.27.2.004
7. Каде А.Х., Казанчи Д.Н., Поляков П.П., Занин С.А., Гаврикова П.А., Катани З.О., Черныш К.М. Гиперкатехоламинемия при стрессовом недержании мочи и возможности его патогенетического лечения: экспериментальное нерандомизированное исследование. Кубанский научный медицинский вестник. 2022;29(2):118–130. https://doi.org/10.25207/1608-6228-2022-29-2-118-130
8. Занин С.А., Чабанец Е.А., Каде А.Х., Поляков П.П., Трофименко А.И., Занина Е.С. Адипонектин как основной представитель адипокинов: роль в патологии, возможности ТЭС-терапии. Медицинский вестник Северного Кавказа. 2022;17(4):455–461. https://doi.org/10.14300/mnnc.2022.17110
9. Pinto TP, Inácio JC, de Aguiar E, Ferreira AS, Sudo FK, Tovar-Moll F, Rodrigues EC. Prefrontal tDCS modulates autonomic responses in COVID-19 inpatients. Brain Stimul. 2023:16(2):657–666. https://doi.org/10.1016/j.brs.2023.03.001
10. Andrade SM, Cecília de Araújo Silvestre M, Tenório de França EÉ, Bezerra Sales Queiroz MH, de Jesus Santana K, Lima Holmes Madruga ML, Torres Teixeira Mendes CK, Araújo de Oliveira E, Bezerra JF, Barreto RG, Alves Fernandes da Silva SM, Alves de Sousa T, Medeiros de Sousa WC, Patrícia da Silva M, Cintra Ribeiro VM, Lucena P, Beltrammi D, Catharino RR, Caparelli-Dáquer E, Hampstead BM, Datta A, Teixeira AL, Fernández-Calvo B, Sato JR, Bikson M. Efficacy and safety of HD-tDCS and respiratory rehabilitation for critically ill patients with COVID-19 The HD-RECOVERY randomized clinical trial. Brain Stimul. 2022;15(3):780–788. https://doi.org/10.1016/j.brs.2022.05.006
11. Fawzy NA, Abou Shaar B, Taha RM, Arabi TZ, Sabbah BN, Alkodaymi MS, Omrani OA, Makhzoum T, Almahfoudh NE, Al-Hammad QA, Hejazi W, Obeidat Y, Osman N, Al-Kattan KM, Berbari EF, Tleyjeh IM. A systematic review of trials currently investigating therapeutic modalities for post-acute COVID-19 syndrome and registered on WHO International Clinical Trials Platform. Clin Microbiol Infect. 2023;29(5):570–577. https://doi.org/10.1016/j.cmi.2023.01.007.
12. Несина И.А., Головко Е.А., Шакула А.В., Фигуренко Н.Н., Жилина И.Г., Хомченко Т.Н., Смирнова Е.Л., Чурсина В.С., Королева А.В. Опыт амбулаторной реабилитации пациентов, перенесших пневмонию, ассоциированную с новой коронавирусной инфекцией COVID-19. Вестник восстановительной медицины. 2021;20(5):4– 11. https://doi.org/10.38025/2078-1962-2021-20-5-4-11
13. Pilloni G, Bikson M, Badran BW, George MS, Kautz SA, Okano AH, Baptista AF, Charvet LE. Update on the Use of Transcranial Electrical Brain Stimulation to Manage Acute and Chronic COVID-19 Symptoms. Front Hum Neurosci. 2020;14:595567. https://doi.org/10.3389/fnhum.2020.595567
14. Alharthy A, Faqihi F, Memish ZA, Karakitsos D. Lung Injury in COVID-19-An Emerging Hypothesis. ACS Chem Neurosci. 2020;11(15):2156–2158. https://doi.org/10.1021/acschemneuro.0c00422
15. Finsterer J. Neurological Perspectives of Neurogenic Pulmonary Edema.Eur Neurol. 2019;81(1-2):94–102. https://doi.org/10.1159/000500139
16. Angelini P, Postalian A, Hernandez-Vila E, Uribe C, Costello B. COVID-19 and the Heart: Could Transient Takotsubo Cardiomyopathy Be Related to the Pandemic by Incidence and Mechanisms? Front Cardiovasc Med. 2022;9:919715. https://doi.org/10.3389/fcvm.2022.919715.
17. Каде А.Х., Кравченко С.В., Трофименко А.И., Чаплыгина К.Ю., Ананьева Е.И., Поляков П.П., Липатова А.С. Эффективность ТЭС-терапии для купирования тревогоподобного поведения и моторных нарушений у крыс с экспериментальной моделью паркинсонизма. Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(9):91–96. https://doi.org/10.17116/jnevro201911909191
18. Пенжоян А.Г., Пенжоян Г.А., Ахеджак-Нагузе С.К., Абушкевич В.Г., Бурлуцкая А.Л. Повышение стрессоустойчивости транскраниальной электростимуляцией у пациентов после различных методов лечения злокачественных новообразований предстательной железы. Ульяновский медико-биологический журнал. 2022;1;75–86. https://doi.org/10.34014/2227-1848-2022-1-75-86
19. Липатова А.С., Каде А.Х., Трофименко А.И., Поляков П.П. Коррекция стресс-индуцированных нейроиммуноэндокринных нарушений у самцов крыс с низкой устойчивостью к стрессу применением транскраниальной электростимуляции. Курский научно-практический вестник «Человек и его здоровье». 2018;3:58– 68. https://doi.org/10.21626/vestnik/2018-3/09
20. Клиндухова М.О., Каде А.Х. Влияние транскраниальной электростимуляции на динамику интерлейкинов у больных острым панкреатитом. Вестник новых медицинских технологий. Электронное издание. 2024;18(2):93–97. https://doi.org/10.24412/2075-4094-2024-2-3-3
21. Билалова А.Р., Моисеева С.В., Шакирова В.Г., Хаертынова И.М., Гатауллин М.Р., Созинова Ю.М., Фаткуллин Б.Ш. Клинико-лабораторная характеристика больных коронавирусной инфекцией. Практическая медицина. 2023;21(1):30–37. https://doi.org/10.32000/2072-1757-2023-1-30-37
22. Полушин Ю.С., Шлык И.В., Гаврилова Е.Г., Паршин Е.В., Гинзбург А.М. Роль ферритина в оценке тяжести COVID-19. Вестник анестезиологии и реаниматологии. 2021;18(4):20–28. https://doi.org/10.21292/2078-5658-2021-18-4-20-28
23. Xu S, Chen M, Feng T, Zhan L, Zhou L, Yu G. Use ggbreak to Effectively Utilize Plotting Space to Deal With Large Datasets and Outliers. Front Genet. 2021;12:774846. https://doi.org/10.3389/fgene.2021.774846
24. Uanhoro JO. Probability of superiority for comparing two groups of clusters. Behav Res. 2023:55:646–656. https://doi.org/10.3758/s13428-022-01815-6
25. Hothorn T, Hornik K, van de Wiel MA, Zeileis A. Implementing a class of permutation tests: The coin package. J Stat Soft. 2008;28(8):1–23. https://doi.org/10.18637/jss.v028.i08
26. In J, Lee DK. Alternatives to the P value: connotations of significance. Korean J Anesthesiol. 2024;77(3):316–325. https://doi.org/10.4097/kja.23630
27. Ordak M. Multiple comparisons and effect size: Statistical recommendations for authors planning to submit an article to Allergy. Allergy. 2023;78(5):1145–1147. https://doi.org/10.1111/all.15700
28. Alonso-Domínguez J, Gallego-Rodríguez M, Martínez-Barros I, Calderón-Cruz B, Leiro-Fernández V, Pérez-González A, Poveda E. High Levels of IL-1β, TNF-α and MIP-1α One Month after the Onset of the Acute SARS-CoV-2 Infection, Predictors of Post COVID-19 in Hospitalized Patients. Microorganisms. 2023;11(10):2396. https://doi.org/10.3390/microorganisms11102396
29. Нестерова И.В., Атажахова М.Г., Тетерин Ю.В., Матушкина В.А., Чудилова Г.А., Митропанова М.Н. Роль нейтрофильных экстрацеллюлярных сетей (NETs) в иммунопатогенезе тяжелого COVID-19: потенциальные иммунотерапевтические стратегии, регулирующие процесс формирования и активность NETs. Инфекция и иммунитет. 2023;13(1):9–28. https://doi.org/10.15789/2220-7619-TRO-2058
30. Volfovitch Y, Tsur AM, Gurevitch M, Novick D, Rabinowitz R, Mandel M, Achiron A, Rubinstein M, Shoenfeld Y, Amital H. The intercorrelations between blood levels of ferritin, sCD163, and IL-18 in COVID-19 patients and their association to prognosis. Immunol Res. 2022;70(6):817–828. https://doi.org/10.1007/s12026-022-09312-w
31. Schmidtner N, Utrata A, Mester P, Schmid S, Müller M, Pavel V, Buechler C. Reduced Plasma Bone Morphogenetic Protein 6 Levels in Sepsis and Septic Shock Patients. Biomedicines. 2024;12(8):1682. https://doi.org/10.3390/biomedicines12081682
32. Rochette L, Zeller M, Cottin Y, Vergely C. GDF15: an emerging modulator of immunity and a strategy in COVID-19 in association with iron metabolism. Trends Endocrinol Metab. 2021;32(11):875–889. https://doi.org/10.1016/j.tem.2021.08.011
33. Al-Kuraishy HM, Al-Gareeb AI, Mostafa-Hedeab G, Kasozi KI, Zirintunda G, Aslam A, Allahyani M, Welburn SC, Batiha GE. Effects of β-Blockers on the Sympathetic and Cytokines Storms in COVID-19. Front Immunol. 2021;12:749291. https://doi.org/10.3389/fimmu.2021.749291
34. Занин С.А., Каде A.Х., Трофименко A.И., Байкова E.E., Оноприев В.В. Эффекты транскраниальной электростимуляции при экспериментальном ишемическом инсульте и черепно-мозговой травме. Анналы клинической и экспериментальной неврологии. 2016;10(3):45–49. https://doi.org/10.17816/psaic43
35. Кравченко С.В., Каде А.Х., Вчерашнюк С.П., Поляков П.П., Булатова В.В., Мищенко А.С. Влияние ТЭС-терапии на динамику тревожного состояния крыс с моделью ротенонового паркинсонизма. Современные проблемы науки и образования. 2019;3:144. https://doi.org/10.17513/spno.28903
36. Каде А.Х., Поляков П.П., Агумава А.А., Гусарук Л.Р., Цымбалов О.В., Алиметов А.Я., Липатова А.С., Вчерашнюк С.П., Кравченко С.В., Шаркова А.В., Черных Н.Ю., Белякова И.С. Влияние ТЭС-терапии на характер стресс-индуцированной экспрессии гена c-fos мононуклеарными лейкоцитами крыс различной стрессоустойчивости. Современные проблемы науки и образования. 2018;1:65. https://doi.org/10.17513/spno.27389
37. Pandey V, Yadav V, Singh R, Srivastava A, Subhashini. β-Endorphin (an endogenous opioid) inhibits inflammation, oxidative stress and apoptosis via Nrf-2 in asthmatic murine model. Sci Rep. 2023;13(1):12414. https://doi.org/10.1038/s41598-023-38366-5
38. Davidson M, Menon S, Chaimani A, Evrenoglou T, Ghosn L, Graña C, Henschke N, Cogo E, Villanueva G, Ferrand G, Riveros C, Bonnet H, Kapp P, Moran C, Devane D, Meerpohl JJ, Rada G, Hróbjartsson A, Grasselli G, Tovey D, Ravaud P, Boutron I. Interleukin-1 blocking agents for treating COVID-19. Cochrane Database Syst Rev. 2022;1(1):CD015308. https://doi.org/10.1002/14651858.CD015308
39. Lan SH, Hsu CK, Chang SP., Lu LC, Lai CC Clinical efficacy and safety of interleukin-1 blockade in the treatment of patients with COVID-19: a systematic review and meta-analysis of randomized controlled trials. Ann Med. 2023;55(1):2208872. https://doi.org/10.1080/07853890.2023.2208872
Об авторах
М. Ю. ИгнатенкоРоссия
Игнатенко Марина Юрьевна — аспирант кафедры общей и клинической патологической физиологии
ул. им. Митрофана Седина, д. 4, г. Краснодар, 350063
Е. В. Кочкарова
Россия
Кочкарова Екатерина Викторовна — ассистент кафедры общей и клинической патологической физиологии
ул. им. Митрофана Седина, д. 4, г. Краснодар, 350063
Н. В. Измайлова
Россия
Измайлова Наталия Викторовна — биолог клинико-диагностической лаборатории
ул. Красных Партизан, д. 6, к. 2, г. Краснодар, 350012
С. А. Занин
Россия
Занин Сергей Александрович — кандидат медицинских наук, доцент, исполняющий обязанности заведующего кафедрой общей и клинической патологической физиологии
ул. им. Митрофана Седина, д. 4, г. Краснодар, 350063
Рецензия
Для цитирования:
Игнатенко М.Ю., Кочкарова Е.В., Измайлова Н.В., Занин С.А. Влияние транскраниальной электростимуляции на сывороточную концентрацию интерлейкина-1-бета при COVID-19: рандомизированное проспективное исследование. Кубанский научный медицинский вестник. 2025;32(6):41-55. https://doi.org/10.25207/1608-6228-2025-32-6-41-55
For citation:
Ignatenko M.Yu., Kochkarova E.V., Izmaylova N.V., Zanin S.A. Effect of transcranial electrical stimulation on serum interleukin-1β levels in COVID-19 patients: A randomized prospective study. Kuban Scientific Medical Bulletin. 2025;32(6):41-55. https://doi.org/10.25207/1608-6228-2025-32-6-41-55
JATS XML








































